Методические рекомендации фармакотерапии хронического болевого синдрома
«Федеральный медицинский исследовательский центр имени П.А. Герцена» Министерства здравоохранения Российской Федерации
ФАРМАКОТЕРАПИЯ ХРОНИЧЕСКОГО БОЛЕВОГО СИНДРОМА У ВЗРОСЛЫХ ПАЦИЕНТОВ
ПРИ ОКАЗАНИИ ПАЛЛИАТИВНОЙ МЕДИЦИНСКОЙ ПОМОЩИ
В СТАЦИОНАРНЫХ И АМБУЛАТОРНО-ПОЛИКЛИНИЧЕСКИХ УСЛОВИЯХ
МЕТОДИЧЕСКИЕ РЕКОМЕНДАЦИИ
МОСКВА 2015

ФАРМАКОТЕРАПИЯ ХРОНИЧЕКОГО БОЛЕВОГО СИНДРОМА
У ВЗРОСЛЫХ ПАЦИЕНТОВ
ПРИ ОКАЗАНИИ ПАЛЛИАТИВНОЙ ПОМОЩИ
В СТАЦИОНАРНЫХ И АМБУЛАТОРНО-ПОЛИКЛИНИЧЕСКИХ УСЛОВИЯХ
Методические рекомендации
Москва 2015
Всоответствии с рекомендациями Всемирной организации здравоохранения и международными рекомендациями по паллиативной медицине, основным методом контроля хронического болевого синдрома является фармакотерапия на основе неинвазивных форм опиоидных анальгетиков. Она применяется в амбулаторнополиклинических условиях и в стационарах независимо от стадии заболевания. Полноценный контроль боли должен осуществляться на этапах противоопухолевой терапии, при оказании симптоматической паллиативной помощи, а также в терминальной стадии болезни. При соблюдении основных принципов ВОЗ этот метод обеспечивает достаточный уровень обезболивания у 70–90% онкологических больных.
Вметодических рекомендациях приведены правила фармакотерапии болевого синдрома неинвазивными и инвазивными методами с учетом особенностей перечня опиоидных анальгетиков, зарегистрированных в России.
Методические рекомендации предназначены для врачей общей практики, врачейонкологов, врачей-гематологов, врачей-терапевтов.
Учреждение-разработчик: ФГБУ «МНИОИ им. П.А. Герцена» – филиал ФГБУ «ФНИМЦ им. П.А. Герцена» Минздрава России.
Авторы: член-корр. РАН, проф. Каприн А.Д., д.м.н. Абузарова, д.м.н. Хороненко В.Э., д.м.н. Алексеева Г.С., проф. Костин А.А., проф. Старинский В.В., проф. Алексеев Б.Я.
2

Оглавление
1. Введение ……………………………………………………………………………………………………………………………. | 4 |
2.Определение понятия боли, классификация и диагностика типов хронического болевого
синдрома ………………………………………………………………………………………………………………………………….. | 4 |
3. Общие принципы терапии хронической боли в онкологии …………………………………………….. | 9 |
4.Алгоритм терапии хронического болевого синдрома у взрослых онкологических
больных ………………………………………………………………………………………………………………………………….. | 17 | |
5. | Контроль прорывов боли ……………………………………………………………………………………………….. | 31 |
6. | Парентеральное введение анальгетиков ………………………………………………………………………… | 31 |
7. | Лечение нейропатической боли………………………………………………………………………………………. | 32 |
8. | Адъювантная терапия хронического болевого синдрома ………………………………………………. | 34 |
ЛИТЕРАТУРА ……………………………………………………………………………………………………………………….. | 39 | |
Приложения …………………………………………………………………………………………………………………………… | 42 | |
3

1.Введение
Боль является одним из основных симптомов, причиняющих страдания при злокачественных новообразованиях (ЗНО). Несмотря на выдающиеся успехи, достигнутые в диагностике и терапии опухолей, по прогнозам экспертов Всемирной Организации Здравоохранения (ВОЗ) в ближайшем обозримом будущем заболеваемость и смертность от рака будет увеличиваться, соответственно будет расти число пациентов с болевыми синдромами, обусловленными опухолевым процессом.
ВРоссии насчитывается свыше 3 млн 090 тыс. человек с установленным диагнозом ЗНО, из них ежегодно умирает около 300 тыс., и выявляется более 500 тыс. новых случаев заболеваний. На начальных стадиях опухолевого процесса 35–50% больных жалуются на боль, при прогрессировании ЗНО их число увеличивается до 75%, а в терминальной стадии – до 95–100%. Таким образом, число онкологических больных, нуждающихся в обезболивающей терапии, значительно превышает число умерших от ЗНО и только в нашей стране составляет не менее 433 тыс. пациентов [1].
В90% случаев болевой синдром связан с опухолевым процессом и его лечением, и
лишь в 10% причиной боли являются сопутствующие заболевания. В 70% боль возникает из-за поражения костей, прорастания или сдавления нервных структур, обструкции протоков, сосудов и поражения слизистых, 20% болевого синдрома связано с диагностическими и лечебными процедурами (биопсия, послеоперационная боль, боль после лучевой и химиотерапии) и около 10% – с паранеопластическим процессом,
пролежнями, запорами и спазмами гладкомышечных органов [2].
2. Определение понятия боли, классификация и диагностика
типов хронического болевого синдрома
Согласно определению экспертов Международной ассоциации по изучению боли:
«Боль – неприятное ощущение и эмоциональное переживание, связанное с реальным или потенциальном повреждением тканей или описываемое в терминах такого повреждения»
(IASP 1992 г.).
Боль является проявлением или симптомом какого-либо заболевания или состояния,
поэтому при оформлении медицинской документации используется код по МКБ-10,
соответствующий основному заболеванию, который может быть дополнен кодами,
свидетельствующими о существовании у пациента боли. Это является важным моментом при дифференциальной диагностике сложных случаев, когда причину боли выявить сразу не удается. В разделе R52 «Боль, не классифицированная в других рубриках» по МКБ-10
определены следующие виды боли:
4

R52.0 – острая боль;
R52.1 – постоянная некупирующаяся боль;
R52.2 – другая постоянная боль;
R52.9 – боль неуточненная.
2.1.Патофизиология болевых синдромов. Типы болевых синдромов
Диагностика, а также последующая тактика терапии боли взаимосвязана с
патофизиологической классификацией онкологической боли (табл. 1).
Таблица 1
Патофизиологическая классификация онкологической боли
Типы боли | Характеристики | Пример | Лечение |
Локализованная, имеет | Боль при ЗНО | ||
четкие границы; | |||
мягких тканей, | |||
постоянная или | |||
Ноцицептивная | метастатическом | ||
приступообразная, | |||
соматическая | поражении костей, | ||
ноющая, | |||
врастании | Противоопухолевая | ||
пульсирующая, | |||
опухолей | терапия, | ||
грызущая | |||
миорелаксанты, | |||
Плохо локализованная, | |||
спазмолитики, | |||
не имеет четких | |||
Боль при опухолях | НПВП, центральные | ||
границ, разлитая; | |||
поджелудочной | анальгетики, | ||
постоянная, ноющая, | |||
Ноцицептивная | железы, желудка, | блокады нервов | |
давящая, | |||
висцеральная | при | ||
схваткообразная, | |||
гепатомегалии, | |||
спастическая; часто | |||
при асците | |||
сопровождается | |||
тошнотой | |||
Внезапная, | Противоопухолевая | ||
терапия, | |||
стреляющая, подобная | Компрессия | ||
антиконвульсанты, | |||
электрическому | корешков, | ||
антидепрессанты, | |||
Нейропатическая | разряду, жгучая, | нервных | |
центральные | |||
колющая, с | сплетений или их | ||
анальгетики, | |||
ощущением жара и/или | ветвей | ||
блокады нервов, | |||
онемения | |||
нейролептики | |||
Онкологическая боль имеет отчасти ту же природу и те же патофизиолологические механизмы, какие формируются при воспалении и повреждении тканей. Общим является раздражение специфических болевых рецепторов – ноцицепторов, распределенных в различных органах и тканях. Особенностью формирования онкологической боли является дополнительная стимуляция болевых рецепторов не только в ответ на взаимодействие с воспалительными альгогенами, но и при специфическом воздействии опухолевых
5

факторов, что способствует усиленному проведению потока болевых импульсов в ЦНС.
Ноцицепторы взаимодействуют с продуктами метаболизма опухолевых клеток,
медиаторами повреждения или воспаления, в результате изменяется биоэлектрический потенциал нейронов, которые передают болевую информацию в спинной мозг, а затем в высшие отделы ЦНС [3].
Ноцицептивная соматическая боль появляется в результате инвазии опухоли и активизации ноцицепторов в месте ее локализации, а именно: в костях, коже, подкожной клетчатке, в мышцах и мягких тканях и пр. Эта боль хорошо локализована, может быть приходящей или постоянной, имеет различные описательные характеристики: тупая или острая, давящая, пульсирующая, дергающая, сверлящая, грызущая, распирающая и пр.
Ноцицептивная висцеральная боль возникает при повреждении симпатически иннервируемых органов (при опухолевом поражении поджелудочной железы, стенок желудка и кишечника, растяжении капсулы печени и пр.). Эта боль плохо локализована,
имеет разлитой характер (тупая с приступами обострения, сжимающая, схваткообразная,
тянущая, изнуряющую и пр.).
Нейропатическая боль является результатом прямого повреждения нервной системы или патологического процесса в соматосенсорной системе. Возникает при у 15– 40% онкологических больных на разных этапах лечения. Зачастую сопровождает тяжелые ноцицептивные болевые синдромы, но иногда встречается как самостоятельный вид боли после хирургического лечения (постмастэктомический болевой синдром), при проведении химиотерапии (токсическая полиневропатия), после лучевой терапии (лучевой миелит) [4, 5, 6].
Характеристики боли обычно – острая, жгучая, «как удар электротоком»,
пронзающая насквозь, жалящая, леденящая, сопровождается неврологической симптоматикой: сенсорного дефицита (онемения) и усиления/возникновения болевых ощущений на неболевые стимулы (прикосновение, холод, тепло), проявляющейся как дизэстезия, аллодиния др.
Прорывная боль. Онкологические боли имеют непостоянную интенсивность в течение суток. Даже у больных, которые получают пролонгированные опиоидные анальгетики, эпизодически (до 4–5 раз в сутки) возникают внезапные острые приступы боли (от умеренных до нестерпимых по интенсивности) продолжительностью от нескольких минут до 2 часов и более. Эти приступы прорывных болей могут быть 3-х
видов:
6

ситуационно | обусловленная | боль, | которая | вызвана | естественными |
физиологическими причинами (опорожнение мочевого пузыря или кишечника, ходьба,
кашель);
спонтанная боль, которая непредсказуема, возникает неожиданно без определенной причины, которую можно предвидеть;
боль в результате окончания действия дозы основного анальгетика, возникает при нарастании толерантности к препарату.
Прорывные боли могут быть ноцицептивными и/или нейропатическими по своему генезу. Своевременное лечение прорывов боли короткодействующими препаратами способствует лучшему контролю боли, снижает неоправданную эскалацию доз пролонгированных опиоидных препаратов. [7].
2.2.Диагностика интенсивности болевого синдрома
1.Оценка интенсивности боли проводится врачом при каждом визите и осмотре онкологического больного.
2.Интенсивность боли оценивается по нумерологической оценочной шкале
(НОШ) или по визуально-аналоговой шкале (ВАШ), которая не содержит градуировки
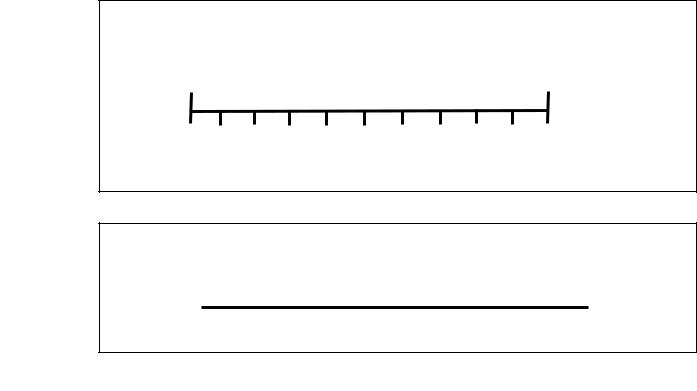
(рис. 1). Больному предлагается на шкале отметить свое восприятие боли на шкале (от минимальной до нестерпимой), что позволяет затем количественно выразить оценку в процентах от 0 до 100% [8].
3. Оценку интенсивности боли проводят отдельно при движении и в состоянии
покоя.
Рисунок 1
Шкалы для оценки интенсивности боли
нумерологическая оценочная шкала
визуально – аналоговая шкала | |
Нет | Нестерпимая |
боли | боль |
7

Для получения дополнительной информации необходимо расспросить больного,
собрать анамнез боли:
1.число и локализацию очагов боли;
2.длительность предшествующего болевого анамнеза;
3.применяемые анальгетики;
4.эффективность предшествующей терапии боли;
5.влияние боли на физическую активность;
6.влияние боли на продолжительность ночного сна;
7.влияние боли на возможность приема пищи и проч.
Сопоставив полученные сведения с данными, приведенными в табл.2, следует определить степень интенсивности боли.
Таблица 2
Диагностические критерии интенсивности боли в зависимости от симптомов
Интенсивность | ||||
болевого | ВАШ | Проявление боли, симптомы | ||
синдрома | ||||
Боли нет | Жалоб нет | |||
1 ступень | Больной спокойно сообщает о своей боли, которая | |||
хорошо купируется на 4–6 часов парацетамолом, | ||||
слабая боль | до 40% | |||
анальгином или средними дозами НПВП, ночной | ||||
сон не нарушен из-за боли | ||||
2 ступень | Парацетамол, анальгин или средние дозы НПВП | |||
40–70% | малоэффективны (не более 1–3 часов), ночной сон | |||
умеренная боль | ||||
нарушен приступами боли | ||||
3 ступень | Трамадол | в | комбинации с парацетамолом или | |
анальгином или НПВП – малоэффективен, боль | ||||
сильная боль | более 70% | |||
вызывает страдание у пациента при воспоминании | ||||
о ней, нарушает его ночной сон | ||||
3 ступень | Больной | на | момент осмотра | мечется, стонет, |
страдает | от | сильнейшей | боли, принимает | |
нестерпимая | 100% | |||
вынужденное положение | ||||
боль | ||||
НЕОБХОДИМА НЕОТЛОЖНАЯ ПОМОЩЬ | ||||
2.3 Выявление нейропатического компонента боли
Диагностическими дескрипторами нейропатической боли являются жалобы на необычно сильные простреливающие, жгучие, ланцирующие (режущие) боли, приступы подобные электрическому разряду, сопровождаются, как правило, сенсорными расстройствами гиперили гипоестезией, аллодинией, дизэстезией, наличие локальных зон патологического зуда или полного отсутствия чувствительности (анестезии).
8

Диагностика нейропатической боли представляет определенные трудности, но для врачей лечебных специальностей, не являющихся неврологами, разработан специальный опросник выявления нейропатического компонента боли – DN4 (Neuropathic pain diagnostic questionnaire – French Neuropathic Pain Group – D. Bouhassiraa – 2004), который может применяться в дифференциальной диагностике и при онкологической боли
(Приложение 1).
Дифференцированная диагностика типов боли, оценка предыдущего и настоящего лечения и их побочных эффектов и осложнений позволяет найти наилучшую безопасную и эффективную комбинацию анальгетиков, добиться наиболее высокого качества жизни пациента при минимуме препаратов и побочных эффектов.
3.Общие принципы терапии хронической боли в онкологии
3.1Рекомендации ВОЗ
Принципы терапии онкологической боли, провозглашенные ВОЗ в 1996 г., остаются неизменными и актуальными до сих пор, хотя периодически проводится обновление эссенциального списка рекомендуемых анальгетиков [9]. Лекарственная терапия опиоидными препаратами является основным методом лечения боли в онкологии. Она проводится в соответствии с пятью принципами:
1. «через рот» – означает, что следует исключить все инъекционные формы анальгетиков, проводить терапию с использованием неинвазивных лекарственных форм
(таблетки, капсулы, сиропы, трансдермальные терапевтические системы, ректальные формы препаратов и проч.);
2. «по часам» – анальгетики следует назначать регулярно по схеме, в
соответствии с длительностью эффекта препарата, не дожидаясь развития сильной боли,
исключая возможность «прорывов» боли;
3.«по восходящей» – подбор препаратов для обезболивания осуществляется от неопиоидных анальгетиков при слабой боли, «мягкими опиоидами» при умеренной боли и сильными опиоидными анальгетиками при сильной боли, по мере нарастания интенсивности боли, в соответствии с «лестницей обезболивания ВОЗ» (рис. 2);
4.«индивидуальный подход» – предполагает необходимость
«индивидуального» подбора анальгетика и основан на селективном выборе наиболее эффективного анальгетика в нужной дозе с наименьшими побочными эффектами для каждого конкретного пациента с учетом особенностей его физического состояния;
9

5. «с вниманием к деталям» – предполагает учет особенностей и деталей каждого пациента, безусловно, назначение коанальгетиков и адъювантных средств, по мере возникновения необходимости в них, проведение мониторинга за больными.
Рисунок 2
«Лестница обезболивания ВОЗ»
3-я ступень сильные опиоиды + неопиаты ±
адъювантная терапия (по требованию)
2-я ступень слабый опиодный анальгетик + неопиоиды
± адъювантная терапия (по требованию)
1-я ступень неопиоидные анальгетики (НПВП, парацетамол)
адъювантная терапия
Методика ВОЗ была разработана для обучения медицинских специалистов,
работающих в различных странах и условиях, способам снятия болевого синдрома с помощью легкодоступных средств, поэтому она представлена в виде простой и понятной всем схемы. Использование символов лестницы упрощает сложную систему титрования фармакологических препаратов. Обезболивание при помощи опиоидов имеет наивысшую эффективность, если пациентам обеспечивается индивидуальный уход и тщательное наблюдение, именно поэтому были включены в концепцию ключевые фразы
«индивидуально» и «с вниманием к деталям».
В ежедневной практике врачей, проводящих терапию боли у онкологических пациентов в амбулаторных условиях, трехступенчатая схема ВОЗ позволяет врачам безопасно осуществлять контроль боли с использованием сильнодействующих препаратов на дому, постепенно повышая дозы и меняя анальгетики по мере ослабления их эффективности [9]. Эффективность этого метода составляет 70–90%. Перечень препаратов, рекомендованных ВОЗ для боли различной интенсивности приведен в табл.3.
Таблица 3
Анальгетики, рекомендованные ВОЗ для фармакотерапии боли у
онкологических больных
10
Источник
Схемы и принципы фармакотерапии ХБС.На протяжении длительного времени лекарственное лечение боли при запущенных формах злокачественных новообразований сводилось к назначению наркотических препаратов и часто не приносило желаемого обезболивающего эффекта.
В 1986 г. Комитетом экспертов ВОЗ были утверждены принципы анальгезирующей терапии хронического болевого синдрома нарастающей интенсивности, получившие название трехступенчатой схемы (рис. 3.2). Согласно трехступенчатой схемы ВОЗ назначают:
при слабой боли (1-я ступень) – ненаркотические анальгетики,
при умеренной боли (2-я ступень) – слабые опиаты,
при сильной боли (3-я ступень) – сильные опиаты.
В качестве базовых лекарственных препаратов рекомендованы:
при слабой боли – аспирин,
умеренной – кодеин,
сильной -морфин.
Создание новых анальгезирующих препаратов, обладающих преимуществами перед базовыми, позволило МНИОИ им. П.А. Герцена выделить понятие о нестерпимой боли и предложить четырехступенчатую схему (рис. 3.2). В этой схеме в качестве базовых препаратов используются:
при умеренной боли – трамадол,
при сильной боли – бупренорфин,
при нестерпимой боли – морфин.
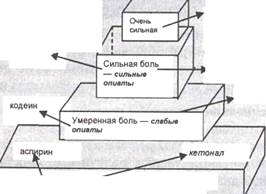
Рис. 3.2. Схемы противоболевой терапии ВОЗ и МНИОИ
В основу обеих схем положены одинаковые принципы:
О борьбу с хроническим болевым синдромом следует начать
возможно раньше, при появлении даже незначительной боли;
вид и дозу анальгетика нужно подбирать индивидуально,
обеспечивая устранение или значительное облегчение боли в
течение 2-3 дней;
принимать анальгетики нужно не «по требованию» (чтобы
уменьшить боль), а строго «по часам», вводя очередную дозу
препарата до прекращения действия предыдущей (чтобы
предотвратить появление боли);
по мере уменьшения обезболивающего эффекта анальгетики следует изменять «по восходящей линии», переходя от максимальной дозы слабо действующего препарата к минимальной дозе сильно действующего, а не к замене на другой препарат такой же активности;
предпочтение следует отдавать оральному приему препаратов, как наиболее простому, эффективному и наименее болезненному пути введения для большинства пациентов.
Способы оценки интенсивности боли и эффективности обезболивания.Непременным условием успешного лечения является объективная оценка интенсивности болевого синдрома и постоянный контроль эффективности препаратов и побочных влияний медикаментозной терапии. Это позволяет врачу своевременно вносить изменения в систему лечения.
Оценку интенсивности хронической боли производят различными способами. Наиболее простой является оценка по 5-бальной словесной шкале:
0 — боли нет;
1 — слабая боль (чуть-чуть болит);
2 — умеренная боль (болит терпимо);
3 — сильная боль (очень больно);
4 — невыносимая боль (невозможно терпеть).
Более точной и наглядной является оценка по визуально-аналоговой шкале в виде линейки с делениями от 0 до 10 или до 100. Пациенту предлагают самому оценить по такой линейке интенсивность болевых ощущений до начала лечения. Повторная оценка в процессе терапии позволяет судить об эффективности лечебных мер.
Лечение слабой боли.Для первой ступени лечения используют нестероидные противовоспалительные средства (НПВС). Эти препараты тормозят синтез простагландинов Е1 и Е2, сенсибилизирующих болевые рецепторы, обладают противовоспалительным и анальгезирующим действием.
НПВС эффективны при метастазах в кости, опухолях мягких тканей, раке тела поджелудочной железы, а также при вызванном новообразованием механическом растяжении тканей и при воспалительных процессах в окружности опухоли, сопровождающихся отеком. Они не угнетают дыхательный и кашлевой центры, не вызывают эйфории и не приводят к возникновению психической или физической зависимости.
Побочное действие НПВС обусловлено токсическим воздействием на слизистую оболочку желудка, функцию почек, гемостаз и коагуляцию. При длительном применении они могут вызвать эрозивный гастрит, вплоть до желудочных кровотечений.
Базовый препарат схемы ВОЗ – аспирин – назначают по 250-650 мг 6 раз в день. Чаще применяют кетонал илиибупрофен. Используют индометацин, пироксиками другие. Полезен парацетамол, не обладающий выраженным противовоспалительным действием, но и не оказывающий токсического 92
Глава 3. Лечение
воздействия на желудок и кровь. Целесообразно использовать комбинированные препараты на основе парацетамола – панадол-экстра и солпадеин.
Лечение умеренной боли.Базовым анальгетиком второй ступени по схеме ВОЗ является слабый опиат – кодеин.
Применяется в дозах от 30 до 130 мг 4-6 раз в сутки. Доза кодеина в 30 мг по обезболивающему эффекту соответствует 650 мг аспирина.
• Запомните обязательно!
Совместное применение обоих препаратов в этих дозировках вдвое повышает обезболивающий эффект.
По схеме МНИОИ базовым анальгетиком считается трамадол (трамал, традол). Он вдвое превосходит кодеин по анальгезирующему действию, не вызывает тяжелых запоров, не обладает угнетающим влиянием на дыхание и кровообращение.
Для справки
Трамадол выпускается в таблетках, капсулах, каплях, свечах и ампулах. Разовая доза — 50-100 мг, вводится каждые 4-6 ч; максимальная суточная – 400 мг. Анальгетический эффект развивается к 30-й минуте и продолжается 5-6 часов.
Лекарственная зависимость к препарату не развивается, анальгезирующий эффект при ХБС может сохраняться в течение длительного времени.
При снижении эффекта от лечения трамадолом рекомендуют прием защечных таблеток наркотического анальгетика просидела, который хорошо устраняет умеренную и даже сильную боль. Его побочные влияния (тошнота, рвота, головокружение, затрудненное мочеиспускание) мало выражены и обычно ликвидируются самостоятельно в течение недели.
Для справки
Просидол по эффективности близок к промедолу. Защечные таблетки (по 20 мг) быстро всасываются слизистой полости рта. Действие непродолжительно. Прием 4-6 раз в сутки. Разовые дозы 20-80 мг, суточные 80-300 мг/сут.
Лечение сильной и очень сильной боли.По схеме ВОЗ базовым препаратом является морфин, по схеме МНИОИ – бупренорфин.
Бупренорфин (сангезик, темгезик, торгезик и др.) – опиоид центрального действия.
По анальгетической активности несколько уступает морфину, но повышает физическую активность больных, а побочные эффекты менее выражены и не опасны. В меньшей степени, чем морфин, вызывает привыкание и лекарственную зависимость. Одна и та же доза может оставаться эффективной в течение длительного времени.
Для справки
Бупренорфин выпускается в таблетках по 0,2 мг и ампулах по 0,3 и 0,6 мг. Принимается внутрь, в/в, в/м, сублингвально. Максимальная концентрация в плазме через 1 ч. Разовая доза для взрослых при в/в и в/м введении — 0,15-0,3 мг/кг. Инъекции повторяют каждые 3-4 ч. Сублингвальный прием по 0,2-ОД мгс интервалом 6-8 ч. Побочные явления: головная боль, головокружение, потливость, сухость во рту, тошнота, рвота.
С помощью бупренорфина удается достичь хорошего противоболевого эффекта даже у больных, длительно получавших морфин, при этом пациенты не испытывают синдрома отмены.
• Запомните обязательно!
Преимущества бупренорфина позволяют назначать его тяжелым больным на дому.
Морфин среди анальгетиков занимает особое место, поскольку с ним принято сравнивать силу действия и побочные эффекты всех обезболивающих
лекарств.
Препараты группы морфина характеризуются недостатками, существенно затрудняющими их использование, особенно в амбулаторных условиях.
• Оказывают выраженное побочное действие.
Они угнетают дыхание и кашлевой рефлекс, обладают снотворным действием, повышают тонус кишечника и мочевого пузыря, могут вызывать тошноту, рвоту, запор и др.
• К препаратам развивается резистентность.
Первоначальные дозы спустя 2-3 недели оказываются недостаточными для снятия боли или продолжительность действия их укорачивается. Это требует увеличения доз. Параллельно нарастают и побочные эффекты. Лечение больных большими дозами морфина на дому чревато опасными осложнениями.
• При длительном лечении убольных возникает физическая и психическая зависимость от наркотика.
Морфин выпускается в виде гидрохлорида и сульфата. Морфин сульфат обладает продленным действием. Лечение рекомендуют начинать с морфина гидрохлорида, а после подбора оптимальной дозы переходить на лечение морфином сульфатом. Обезболивающее действие морфина проявляется через 10-15 минут после подкожного введения и через 20-30 минут после перорального. Продолжается в течение 3-5 часов у морфина гидрохлорида и 12-ти часов у морфина сульфата.
По мере развития резистентности дозу постепенно повышают. Основными симптомами передозировки являются сонливость, адинамия, рвота, запоры, дезориентация, галлюцинации.
Эти явления требуют снижения дозы или отмены наркотика.
Одновременно с началом терапии морфином следует назначить противорвотные и слабительные средства. К рвотному действию морфина у больных постепенно развивается резистентность, поэтому антиэметики применяют не более 2 недель. Для предупреждения запоров рекомендуют диету с большим количеством жидкости, соков, фруктов, лекарств, стимулирующих перистальтику и опорожнение кишечника. Запоры требуют назначения слабительных, а иногда и клизм в течение некоторого периода терапии морфином.
Таблетированная форма морфина сульфата (МСТ континус) обладает продленным действием. Полный эффект наступает через 2 часа, анальгезия продолжается 12 часов. Побочные действия (тошнота, рвота и др.) возникают редко и купируются противорвотными препаратами.
Многих недостатков, свойственных морфину и опиатам, лишены синтетические опиоиды. К их числу относится буторфанол.
Буторфанол – синтетический анальгетик фенантренового ряда с агонистической и антагонистической активностью. По анальгетической активности и продолжительности действия близок к морфину. Применяется для лечения хронической боли умеренной и высокой интенсивности.
Для справки
Буторфанол (стадол) – выпускается в ампулах по 1,0 мл. вводится в/в, в м. интраназально. При интраназальном введении анальгезия через 1-2 часа, продолжительность действия 4-5 часов.
Меньше морфина угнетает дыхание, реже наблюдается привыкание, не вызывает эйфории и лекарственной зависимости. Возможны тошнота, рвота, усиленное потоотделение, сонливость, головокружение.
Буторфанол у больных с ХБС рассматривают как резервный препарат. Применяют при плохой переносимости опиоидов и опиатов.
Фентанил – синтетический опиоид, по анальгезирующему эффекту превосходит морфин в 100 раз. Способен диффундировать через кожу. Создана специальная трансдермальная система в виде многослойного пластыря, который наклеивается на кожу. Пластырь с фентанилом выпускается под названием «Дюрогезик». Из него препарат постепенно, на протяжении трех суток, поступает в кровь.
Для справки
Диффузия фентанила начинается через 2 часа, анальгезирующий эффект развивается в среднем через 12-13 часов и продолжается в течение 72 часов. После удаления пластыря обезболивающий эффект сохраняется еще на протяжении 12 часов. Новый пластырь наклеивают на другое место.
Дюрогезик удобен для использования в домашних условиях, но возможна брадикардия, угнетение дыхания.
Адъювантные лекарственные средства.Учитывая сложный патогенез ХБС при злокачественных новообразованиях, наркотические препараты следует сочетать с нестероидными анальгетиками периферического действия и дополнительными т. н. «адъювантными» средствами. В противоположность этому не рекомендуется одновременно применять два наркотических препарата, поскольку слабый опиат может блокировать клеточные рецепторы, препятствуя воздействию более сильного.
Адъювантные препараты применяют
• для усиления действия анальгетиков;
• терапии осложнений, связанных с прогрессирующим опухолевым процессом;
• коррекции побочных эффектов обезболивающих препаратов.
Арсенал адъювантных средств широк. Используют кортикостероиды, противосудорожные и антигистаминные препараты, транквилизаторы и нейролептики, антидепрессанты и др.
Кортикостероиды снижают продукцию простагландинов, уменьшают воспаление и отек. Полезны при метастазах в кости, в головной и спинной мозг, при сдавлении опухолью и метастазами нервных стволов.
Противосудорожные препараты (карбамазепин, валъпромид и др.) показаны при сдавлении или прорастании опухолью нервных стволов. Они также оказывают антидепрессивное влияние, улучшают психическое состояние и настроение больных.
Транквилизаторы и нейролептики используют при тревоге, беспокойстве, агрессивности больных.
Антидепрессанты (амитриптилин) назначают при выраженной депрессии. С их помощью удается повысить настроение и улучшить сон.
Терапию нейролептиками, антидепрессантами и противосудорожными препаратами начинают с минимальных доз. Дозы повышают до максимальных, а затем постепенно снижают до полной отмены в течение несколько недель или месяцев в зависимости от конкретной ситуации.
По мере прогрессирования опухоли интенсивность ХБС изменяется, чаще в сторону нарастания. Это требует тщательного наблюдения за больным и периодической смены анальгетиков и адъювантных препаратов.
Вопросы тестового контроля
34. Под термином «радикальная» операция понимают
а) удаление основной массы опухоли
б) удаление части или всего пораженного органа без регионарных лимфатических узлов
в) удаление части или всего пораженного органа в пределах анатомической зоны
г) удаление части или всего пораженного органа с регионарными лимфатическими узлами, но с оставлением отдаленных метастазов
Источник
