Наджелудочковая тахикардия и впв синдром

АВ-узловая пароксизмальная тахикардия при синдроме Вольфа-Паркинсона-Уайта (WPW)
Наджелудочковая тахикардия, как уже было сказано, является наиболее часто встречающимся нарушением ритма сердца (70%) при синдроме WPW. Различают два механизма возникновения АВ-узловой тахикардии: ортодромный и антидромный.
I. Ортодромная АВ-узловая тахикардия при синдроме Вольфа-Паркинсона-Уайта (WPW)
Эта форма АВ-узловой тахикардии встречается чаще (90%). Возбуждение сначала распространяется антеградно по АВ-узлу и затем ретроградно по дополнительному пути проведения (пучку Кента).
Направление и последовательность распространения возбуждения таковы: предсердия —> АВ-узел —> желудочки —> пучок Кента —> предсердия. В результате возникает круговое возбуждение.
Дельта-волна отсутствует. Узкие комплексы QRS быстро следуют друг за другом; зубец Р вследствие задержки возбуждения предсердий «попадает» на комплекс QRS и потому неразличим или появляется сразу после комплекса QRS, попадая на сегмент ST, что обусловливает феномен RP<PR.
Круговое возбуждение при синдроме Вольфа-Паркинсона-Уайта (WPW) является типичным примером механизма повторного входа волны возбуждения (re-entry).
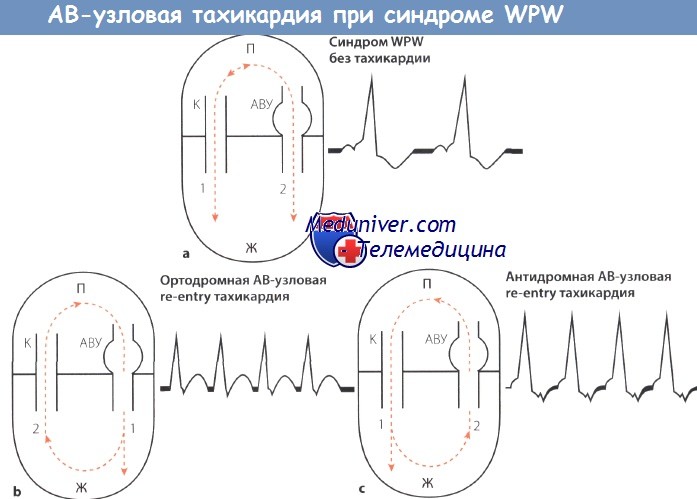
Схема АВ-узловой тахикардии при синдроме WPW.
АВУ – АВ-узел; П – предсердие, Ж -желудочек;
К – пучок Кента (дополнительный пучок проведения);
1,2- последовательность возбуждения; стрелки “вверх-вниз”- направление возбуждения.
II. Антидромная АВ-узловая тахикардия при синдроме Вольфа-Паркинсона-Уайта (WPW)
При другом механизме, который лежит в основе более редкой формы АВ-узловой тахикардии возбуждение распространяется в обратном направлении, т.е. сначала антеградно по дополнительному проводящему пучку (пучку Кента), затем ретроградно через АВ-узел, но только тогда, когда эффективный рефрактерный период пучка Кента оказывается короче, чем АВ-узла.
В этом случае направление и последовательность распространения возбуждения таковы: предсердия —> пучок Кента —> желудочки —> АВ-узел —> предсердия.
В целом появляются уширенные комплексы QRS, напоминающие блокаду ножки ПГ, но с дельта-волной, так что синдром WPW можно диагностировать, несмотря на тахикардию.
Как и при желудочковой тахикардии, зубец Р на ЭКГ в этих случаях трудно идентифицировать. Однако при тщательном анализе кривой его часто можно обнаружить на сегменте ST сразу после зубца S.
Из-за формального сходства эту форму синдрома Вольфа-Паркинсона-Уайта (WPW) ранее называли псевдожелудочковой тахикардией, хотя истинная желудочковая тахикардия при синдроме WPW наблюдается крайне редко.
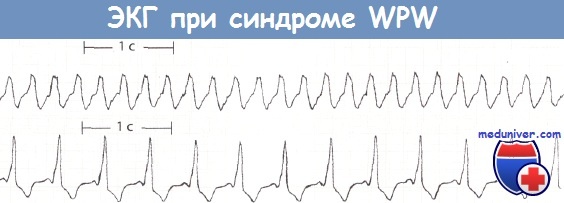
Синдром Вольфа-Паркинсона-Уайта (WPW).
Вверху: пароксизмальная наджелудочковая тахикардия. Антидромная АВ-узловая тахикардия. Частота желудочковых сокращений 155 ударов в минуту. Комплекс QRS уширен и составляет 0,12 с.
Внизу: синусовый ритм при синдроме WPW. Скорость движения бумажной ленты 25 мм/с.
III. Мерцание предсердий при синдроме Вольфа-Паркинсона-Уайта (WPW)
Мерцание предсердий занимает особое место среди нарушений ритма при синдроме WPW и составляет по частоте примерно 20%. При быстрой форме мерцания предсердий (тахиаритмия) существует опасность быстрого распространения возбуждения по дополнительному пути проведения из предсердий в желудочки. Это может привести к уширению комплексов QRS, изменению их конфигурации, напоминающей таковую при блокаде ножек ПГ, и стать причиной развития фибрилляции желудочков и смерти.
При тахиаритмической форме мерцания предсердий назначать препараты наперстянки и верапамил нельзя, так как эти препараты, с одной стороны, замедляют проведение возбуждения, с другой – еще больше укорачивают рефрактерный период пучка Кента, что приводит к облегчению проведения частых импульсов от предсердий к желудочкам.
Учебное видео ЭКГ при синдроме WPW (Вольфа-Паркинсона-Уайта)

– Также рекомендуем “Признаки гипокалиемии на ЭКГ”
Оглавление темы “Расшифровка ЭКГ (электрокардиограммы)”:
- Расшифровка холтеровского мониторинга электрокардиограммы (ЭКГ)
- Признаки перикардита на ЭКГ
- Признаки миокардита на ЭКГ
- Признаки хронического легочного сердца на ЭКГ
- Признаки ТЭЛА (тромбоэмболии легочной артерии, острого легочного сердца) на ЭКГ
- Признаки синдрома Вольфа-Паркинсона-Уайта (WPW) на ЭКГ
- Классификация синдрома Вольфа-Паркинсона-Уайта (WPW): типы А и В
- АВ-узловая пароксизмальная тахикардия при синдроме Вольфа-Паркинсона-Уайта (WPW)
- Признаки гипокалиемии на ЭКГ
- Синдром удлиненного интервала QT на ЭКГ
Источник
Синдром Вольфа-Паркинсона-Уайта (синдром WPW) – клинико-электрокардиографический синдром, характеризующийся предвозбуждением желудочков по дополнительным атриовентрикулярным путям проведения и развитием пароксизмальных тахиаритмий. Синдром WPW сопровождается различными аритмиями: наджелудочковой тахикардией, фибрилляцией или трепетанием предсердий, предсердной и желудочковой экстрасистолией с соответствующей субъективной симптоматикой (ощущением сердцебиения, одышкой, гипотензией, головокружением, обмороками, болями в грудной клетке). Диагностика синдрома WPW основана на данных ЭКГ, суточного ЭКГ-мониторирования, ЭхоКГ, ЧПЭКС, ЭФИ. Лечение синдрома WPW может включать антиаритмическую терапию, чреспищеводную электрокардиостимуляцию, катетерную РЧА.
Общие сведения
Синдром Вольфа-Паркинсона-Уайта (синдром WPW) – синдром преждевременного возбуждения желудочков, обусловленный проведением импульсов по добавочным аномальным проводящим пучкам, соединяющим предсердия и желудочки. Распространенность синдрома WPW, по данным кардиологии, составляет 0,15-2%. Синдром WPW чаще встречается среди мужчин; в большинстве случаев манифестирует в молодом возрасте (10-20 лет), реже – у лиц старшего возраста. Клиническое значение синдрома WPW заключается в том, что при его наличии часто развиваются тяжелые нарушения сердечного ритма, которые представляют угрозу для жизни больного и требуют особых подходов к лечению.

Синдром WPW
Причины синдрома WPW
По мнению большинства авторов, синдром WPW, обусловлен сохранением добавочных атриовентрикулярных соединений в результате незавершенного кардиогенеза. При этом происходит неполная регрессия мышечных волокон на этапе формирования фиброзных колец трикуспидального и митрального клапанов.
В норме дополнительные мышечные пути, соединяющие предсердия и желудочки, существуют у всех эмбрионов на ранних стадиях развития, но постепенно они истончаются, сокращаются и полностью исчезают после 20-й недели развития. При нарушении формирования фиброзных атриовентрикулярных колец мышечные волокна сохраняются и составляют анатомическую основу синдрома WPW. Несмотря на врожденный характер дополнительных АВ-соединений, синдром WPW может впервые проявиться в любом возрасте. При семейной форме синдрома WPW чаще имеют место множественные добавочные атриовентрикулярные соединения.
В 30% случаев синдром WPW сочетается с врожденными пороками сердца (аномалией Эбштейна, пролапсом митрального клапана, дефектами межпредсердной и межжелудочковой перегородки, тетрадой Фалло), дизэмбриогенетическими стигмами (дисплазией соединительной ткани), наследственной гипертрофической кардиомиопатией.
Классификация синдрома WPW
По рекомендации ВОЗ, различают феномен и синдром WPW. Феномен WPW характеризуется электрокардиографическими признаками проведения импульса по дополнительным соединениям и предвозбуждением желудочков, но без клинических проявлений АВ реципрокной тахикардии (re-entry). Под синдромом WPW подразумевается сочетание предвозбуждения желудочков с симптоматической тахикардией.
С учетом морфологического субстрата выделяют несколько анатомических вариантов синдрома WPW.
I. С добавочными мышечными АВ-волокнами:
- идущими через добавочное левое или правое париетальное АВ-соединение
- идущими через аортально-митральное фиброзное соединение
- идущими от ушка правого или левого предсердия
- связанными с аневризмой синуса Вальсальвы или средней вены сердца
- септальными, парасептальными верхними или нижними
II. Со специализированными мышечными АВ-волокнами («пучками Кента»), происходящими из рудиментарной, аналогичной структуре атриовентрикулярного узла, ткани:
- атрио-фасцикулярными – входящими в правую ножку пучка Гиса
- входящими в миокард правого желудочка.
Выделяют несколько клинических форм синдрома WPW:
- а) манифестирующую – с постоянным наличием дельта-волны, синусовым ритмом и эпизодами атриовентрикулярной реципрокной тахикардии.
- б) интермиттирующую – с преходящим предвозбуждением желудочков, синусовым ритмом и верифицированной атриовентрикулярной реципрокной тахикардией.
- в) скрытую – с ретроградным проведением по дополнительному атриовентрикулярному соединению. Электрокардиографические признаки синдрома WPW не выявляются, имеются эпизоды атриовентрикулярной реципрокной тахикардии.
Патогенез синдрома WPW
Синдром WPW обусловлен распространением возбуждения от предсердий к желудочкам по дополнительным аномальным путям проведения. В результате этого возбуждение части или всего миокарда желудочков происходит раньше, чем при распространении импульса обычным путем – по АВ-узлу, пучку и ветвям Гиса. Предвозбуждение желудочков отражается на электрокардиограмме в виде дополнительной волны деполяризации – дельта-волны. Интервал P-Q(R) при этом укорачивается, а длительность QRS увеличивается.
Когда в желудочки приходит основная волна деполяризации, их столкновение в сердечной мышце регистрируется в виде так называемого сливного комплекса QRS, который становится несколько деформированным и уширенным. Нетипичное возбуждение желудочков сопровождается нарушением последовательности процессов реполяризации, что находит выражение на ЭКГ в виде дискордантного комплексу QRS смещения RS-T сегмента и изменения полярности зубца T.
Возникновение при синдроме WPW пароксизмов суправентрикулярной тахикардии, мерцания и трепетания предсердий связано с формированием круговой волны возбуждения (re-entry). В этом случае импульс по AB-узлу движется в антероградном направлении (от предсердий к желудочкам), а по дополнительным путям – в ретроградном направлении (от желудочков к предсердиям).
Симптомы синдрома WPW
Клиническая манифестация синдрома WPW происходит в любом возрасте, до этого его течение может быть асимптомным. Синдром WPW сопровождается различными нарушениями сердечного ритма: реципрокной наджелудочковой тахикардией (80%), фибрилляцией предсердий (15-30%), трепетанием предсердий (5%) с частотой 280-320 уд. в мин. Иногда при синдроме WPW развиваются менее специфичные аритмии – предсердная и желудочковая экстрасистолия, желудочковая тахикардия.
Приступы аритмии могут возникать под влиянием эмоционального или физического перенапряжения, злоупотребления алкоголем или спонтанно, без видимых причин. Во время аритмического приступа появляются ощущения сердцебиения и замирания сердца, кардиалгии, чувство нехватки воздуха. Мерцание и трепетание предсердий сопровождается головокружением, обмороками, одышкой, артериальной гипотензией; при переходе в фибрилляцию желудочков может наступить внезапная сердечная смерть.
Пароксизмы аритмии при синдроме WPW могут длиться от нескольких секунд до нескольких часов; иногда они купируются самостоятельно или после выполнения рефлекторных приемов. Затяжные пароксизмы требуют госпитализации больного и вмешательства кардиолога.
Диагностика синдрома WPW
При подозрении на синдром WPW проводится комплексная клинико-иснтрументальная диагностика: ЭКГ в 12 отведениях, трансторакальная эхокардиография, мониторирование ЭКГ по Холтеру, чреспищеводная электрокардиостимуляция, электрофизиологическое исследование сердца.
К электрокардиографическим критериям синдрома WPW относятся: укорочение PQ-интервала (менее 0,12 с), деформированный сливной QRS-комплекс, наличие дельта-волны. Суточное ЭКГ мониторирование применяется для обнаружения преходящих нарушений ритма. При проведении УЗИ сердца выявляются сопутствующие пороки сердца, кардиомиопатию.
Проведение чреспищеводной электрокардиостимуляции при синдроме WPW позволяет доказать наличие дополнительных путей проведения, индуцировать пароксизмы аритмии. Эндокардиальное ЭФИ позволяет точно определить локализацию и количество дополнительных путей, верифицировать клиническую форму синдрома WPW, выбрать и оценить эффективность лекарственной терапии или РЧА. Дифференциальную диагностику синдрома WPW проводят с блокадами ножек пучка Гиса.
Лечение синдрома WPW
При отсутствии пароксизмов аритмии синдром WPW не требует специального лечения. При гемодинамически значимых приступах, сопровождающихся синкопэ, стенокардией, гипотензией, нарастанием признаков сердечной недостаточности, требуется выполнение незамедлительной наружной электрической кардиоверсии или чреспищеводной электрокардиостимуляции.
В некоторых случаях для купирования пароксизмов аритмий эффективными оказываются рефлекторные вагусные маневры (массаж каротидного синуса, проба Вальсальвы), внутривенное введение АТФ или блокаторов кальциевых каналов (верапамила), антиаритмических препаратов (новокаинамида, аймалина, пропафенона, амиодарона). В дальнейшем пациентам с синдромом WPW показана постоянная антиаритмическая терапия.
В случае резистентности к антиаритмическим препаратам, развития фибрилляцией предсердий проводится катетерная радиочастотная абляция добавочных путей проведения трансаортальным (ретроградным) или транссептальным доступом. Эффективность РЧА при синдроме WPW достигает 95%, риск рецидивов составляет 5-8 %.
Прогноз и профилактика синдрома WPW
У пациентов с бессимптомным течением синдрома WPW прогноз благоприятный. Лечение и наблюдение требуется только лицам, имеющим отягощенный семейный анамнез в отношении внезапной смерти и профессиональные показания (спортсменам, летчикам и др.). При наличии жалоб или жизнеугрожающих аритмий необходимо проведение полного комплекса диагностического обследования для выбора оптимального метода лечения.
Пациенты с синдромом WPW (в том числе, перенесшие РЧА) нуждаются в наблюдении кардиолога-аритмолога и кардиохирурга. Профилактика синдрома WPW носит вторичный характер и заключается в проведении противоаритмической терапии для предотвращения повторных эпизодов аритмий.
Источник
- 1 Наджелудочковые тахикардии при синдромах преждевременного возбуждения желудочков (синдромы преждевременного возбуждения, синдромы предвозбуждения)
- 1.1 Определение и классификация
- 1.2 Эпидемиология, этиология
- 1.3 Патогенез
- 1.4 Диагностика, дифференциальная диагностика
Наджелудочковые тахикардии при синдромах преждевременного возбуждения желудочков (синдромы преждевременного возбуждения, синдромы предвозбуждения)
Определение и классификация
Синдромы предвозбуждения включают в себя группу нарушений сердечного ритма, возникающих в результате наличия аномального, как правило, атриовентрикулярного дополнительного проводящего пути (ДПП) с возможностью антероградного и/или ретроградного распространения электрических импульсов в обход и, как правило, в опережение нормальной проводящей системы сердца, что и создаёт феномен преждевременного возбуждения (предвозбуждения) желудочков и/или предсердий (рис. 1)
Традиционно принято выделять два морфофункциональных субстрата, лежащих в основе синдромов предвозбуждения: т.н. «быстрые» ДПП, которые представлены исключительно пучками Кента и т.н. «медленные» ДПП, среди которых выделяют медленно проводящие пучки Кента, а также волокна Махайма.

Рис. 1. Схема формирования электрокардиографических признаков предвозбуждения желудочков при синдроме Вольфа-Паркинсона-Уайта.Обозначения: Пунктирной линией обозначена форма комплекса QRST в норме.
Наличие предвозбуждения желудочков лежит в основе формирования симптомокомплекса, названного по имени авторов синдромом Вольфа-Паркинсона-Уайта (ВПУ). Данный синдром включает три электрокардиографических признака (см. рис. 1):
- укорочение интервала PQ/PR менее 120 мс
- расширение желудочкового комплекса более 120 мс
- регистрация на начальном отклонении зубца R так называемой дельта-волны
а также один клинический признак – приступы сердцебиений, которым соответствуют по ЭКГ нижеперечисленные виды наджелудочковых тахикардий:
- пароксизмальная ортодромная реципрокная тахикардия (ПОРТ),
- пароксизмальная антидромная реципрокная тахикардия (ПАРТ),
- пароксизмальная фибрилляция/трепетание предсердий с проведением на желудочки по ДПП.
При отсутствии этих тахиаритмий у больных с признаками предвозбуждения желудочков говорят об электрокардиографическом феномене ВПУ.
Наиболее частым видом ДПП является пучок Кента, проводящий импульсы в обоих направлениях: из предсердий в желудочки (антероградно) и из желудочков в предсердия (ретроградно). Однако у 20-25% пациентов с ДПП при проведении внутрисердечного ЭФИ может быть выявлено однонаправленное, исключительно ретроградное проведение электрических импульсов по пучку Кента. Такое состояние обозначается как скрытый ДПП. Несмотря на отсутствие признаков предвозбуждения желудочков по данным ЭКГ, скрытый пучок Кента, как правило, проявляется возникновением приступов ортодромной реципрокной тахикардии.
При т.н. «латентном» ДПП признаки предвозбуждения желудочков также не регистрируются на ЭКГ в обычных условиях, однако они всегда проявляются в случае естественного или ятрогенного замедления проведения импульсов по АВ-узлу (см. ниже).В отличие от пучков Кента, скорость проведения по которым постоянна, волокна Махайма являются ДПП с т.н. «декрементальными» характеристиками (проведение по волокнам может замедляться при определённых условиях). Другими характерными свойствами волокон Махайма являются:
- локализация волокон в переднебоковой стенке правого желудочка,
- латентный характер предвозбуждения желудочков,
- однонаправленный, предсердно-желудочковый характер предвозбуждения.
Однонаправленный характер предвозбуждения желудочков у больных с волокнами Махайма исключает возникновение ПОРТ у этих пациентов, а наиболее частым вариантом тахикардии является ПАРТ. Существенно реже регистрируется пароксизмальная фибрилляция/трепетание предсердий с проведением по волокнам Махайма.
Эпидемиология, этиология
Синдромы предвозбуждения являются второй после АВУРТ наиболее частой причиной наджелудочковых тахикардий (около 25% всех НЖТ). Наличие аномального дополнительного проводящего пути (ДПП), как причины предвозбуждения желудочков, регистрируется у 1-3 промилей населения и выявляется преимущественно в молодом возрасте. Существует наследственная предрасположенность к синдромам предвозбуждения (ДПП выявляются у 3,4% близких родственников этих пациентов). Функционирование ДПП является результатом нарушения внутриутробного развития фиброзных колец митрального и/или трикуспидального клапана, в результате которого сохраняется одно или несколько мышечных соединений между предсердным и желудочковым миокардом. Наличие синдромов предвозбуждения ассоциировано с более частым выявлением врождённых пороков сердца, гипертрофической кардиомиопатии и скелетной миопатии. Однако у большинства пациентов с ДПП структурной патологии сердца и мышечной системы не выявляется.
Патогенез
По своей структуре пучки Кента представляют собой атриовентрикулярные мышечные волокна, проникающие из предсердий в желудочки через дефекты в фиброзном атриовентрикулярном кольце, наличие которых является результатом незавершённого внутриутробного развития. Топографически ДПП могут располагаться практически в любом месте вокруг левого или правого атриовентрикулярных отверстий, однако чаще всего встречаются пучки Кента левой боковой локализации.
К волокнам Махайма относят несколько различных типов ДПП. В клинической практике наиболее часто встречаются атриофасцикулярные (соединяющие предсердия с дистальными отделами ножки пучка Гиса) или атриовентрикулярные ДПП. Более редкими анатомическими субстратами волокон Махайма являются нодофасцикулярные (соединяющие АВ-узел с правой ножкой пучка Гиса) и нодовентрикулярные (соединяющие АВ-узел с миокардом желудочков) тракты. Волокна Махайма имеют существенные анатомо-функциональные отличия от пучков Кента. Они характеризуются большей протяжённостью, состоят клеток близких по своим свойствам клеткам АВ-соединения, а также могут пересекать кольцо атриовентрикулярного клапана не перпендикулярно, а под острым углом.
Наличие в сердце помимо нормальной предсердно-желудочковой проводящей системы (АВ-соединения) аномального ДПП является электрофизиологической основой для циркуляции электрических импульсов по механизму повторного входа (re-entry) с участием данных структур.
Диагностика, дифференциальная диагностика
Характерная электрокардиографическая картина при синдроме/феномене ВПУ формируется на основе сливного механизма деполяризации желудочков. Так как скорость проведения по пучку Кента, как правило, значительно превосходит таковую у АВ-узла, волна возбуждения, распространяясь по ДПП, приводит к раннему (преждевременному) возбуждению части миокарда желудочков (рис. 1-А). Это проявляется на ЭКГ дельта-волной и укорочением интервала PQ/PR (рис. 1-Б). Параллельно с этим импульс, проведенный с задержкой в АВ-узле, охватывает возбуждением остальную часть миокарда желудочков, завершая процесс их деполяризации. Аномальная деполяризация миокарда желудочков, как правило, приводит к нарушению процессов их реполяризации, что может проявляться на ЭКГ (рис. 1-Б) депрессией сегмента ST и инверсией зубца T.
В отличие от пучка Кента, скорость проведения по АВ-узлу может существенно изменяться в зависимости от частоты возбуждения предсердий и колебаний тонуса вегетативной нервной системы. Эта особенность широко используется для выявления так называемых «латентных» пучков Кента и волокон Махайма, при которых предвозбуждение желудочков не выявляется на ЭКГ в обычных условиях вследствие относительно медленного проведения импульсов по ДПП или относительно быстрого по АВ-узлу. Для демаскирования предвозбуждения в этих случаях требуется провокация дополнительной задержки проведения в АВ-узле, например, при выполнении “вагусных проб” или при частой электростимуляции предсердий, что закономерно приводит у больных с синдромом ВПУ к постепенному увеличению степени предвозбуждения желудочков: укорочению интервала PR, усилению выраженности дельта-волны и расширению комплексов QRS (рис. 2).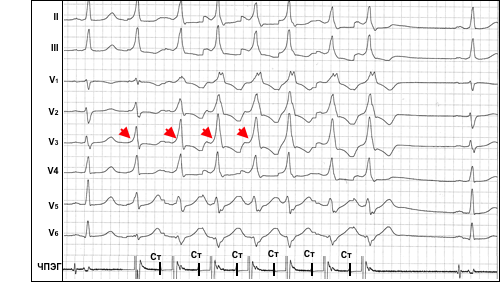 Рис. 2. Латентный синдром ВПУ. Эффект «концертино» при частой стимуляции предсердий. Обозначения: ЧПЭГ – чреспищеводная электрограмма, Ст – артефакты стимулов. Стрелками отмечено нарастание признаков предвозбуждения желудочков (укорочение интервала стимул-дельта, увеличение амплитуды дельта-волны, расширение QRS).
Рис. 2. Латентный синдром ВПУ. Эффект «концертино» при частой стимуляции предсердий. Обозначения: ЧПЭГ – чреспищеводная электрограмма, Ст – артефакты стимулов. Стрелками отмечено нарастание признаков предвозбуждения желудочков (укорочение интервала стимул-дельта, увеличение амплитуды дельта-волны, расширение QRS).
Этот феномен получил название эффекта “концертино” и имеет важное диагностическое значение.Приблизительно в 10-12% случаев у больных могут иметь место несколько ДПП, причём предвозбуждение с участием одних пучков Кента может демонстрировать явный, двунаправленный характер, в то время как с участием других ДПП – носить скрытые и/или латентные свойства. На наличие нескольких ДПП указывает изменение характера предвозбуждения желудочков (изменение полярности дельта-волн и конфигурации комплексов QRS по ЭКГ), регистрируемое во время приступов фибрилляции/трепетания предсердий или при проведении программной стимуляции предсердий во время ЭФИ.Анатомическое расположение пучка Кента предопределяет характер электрокардиографических проявлений феномена и синдрома ВПУ. Существуют специальные алгоритмы, с помощью которых, на основании анализа полярности дельта-волны и/или комплекса QRS в 12 отведениях ЭКГ можно установить ориентировочную локализацию пучка Кента. Для точного определения локализации пучка Кента необходимо проведение внутрисердечного ЭФИ.
Наиболее часто встречающейся формой наджелудочковой тахикардии при синдроме ВПУ является пароксизмальная ортодромная реципрокная тахикардия (ПОРТ). В ее основе лежит циркуляция импульсов между предсердиями и желудочками, антероградно по АВ-узлу и ретроградно по пучку Кента (рис. 3-А). Для возникновения тахикардии необходимо, чтобы преждевременный предсердный импульс (предсердная экстрасистола, а в условиях ЭФИ – предсердный экстрастимул) имели ту критическую величину интервала сцепления, при которой пучок Кента находится в состоянии рефрактерности, а АВ-узел – нет. При возникновении блока проведения по ДПП, атриовентрикулярное проведение осуществляется только по АВ-узлу и системе Гиса-Пуркинье. На ЭКГ этот момент проявляется исчезновением признаков предвозбуждения желудочков и нормализацией комплекса QRS(исчезновение дельта-волны и расширения). Рис. 3. Схема механизмов реципрокных тахикардий при синдроме Вольфа-Паркинсона-Уайта. А. – Пароксизмальная ортодромная реципрокная тахикардия; Б. – Пароксизмальная антидромная реципрокная тахикардия.
Рис. 3. Схема механизмов реципрокных тахикардий при синдроме Вольфа-Паркинсона-Уайта. А. – Пароксизмальная ортодромная реципрокная тахикардия; Б. – Пароксизмальная антидромная реципрокная тахикардия.
Ключевым моментом в развитии ПОРТ является критическая задержка проведения в АВ-узле, достаточная для достижения импульсом желудочкового окончания пучка Кента к тому моменту, когда ДПП уже вышел из состояния рефрактерности. Волна возбуждения возвращается в предсердия по пучку Кента, замыкая тем самым цепь re-entry. ПОРТ представляет собой устойчивую циркуляцию импульса по описанному пути. Так как перед возвращением в предсердия волна возбуждения при ПОРТ вынуждена пройти относительно протяжённый путь по системе Гиса-Пуркинье и миокарду желудочков, зубцы P (на рис. 4 обозначены стрелками) регистрируются всегда после комплексов QRS. При этом они инвертированы в отведениях II, III, aVF. Интервал RP<PR. Величина интервала RP (интервала VA на чреспищеводной электрограмме, см. рис. 4), отражающая время проведения импульсов из желудочков в предсердия, превышает 70 мс. Этот признак принципиально отличает ПОРТ от типичной АВ-узловой реципрокной тахикардии, описанной выше.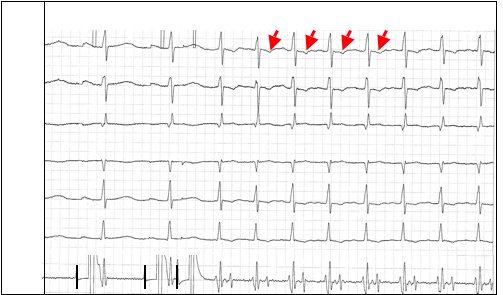 Рис. 4. Индукция пароксизмальной ортодромной тахикардии у больного со скрытым пучком Кента при проведении ЧПЭС. Обозначения: ЧПЭГ – чреспищеводная электрограмма, A – осцилляции предсердий, V – осцилляции желудочков. Интервал VA=140 мс – время ретроградного проведения (от желудочков к предсердиям) по пучку Кента, Ст1 и Ст2 – частая и программная стимуляция предсердий.
Рис. 4. Индукция пароксизмальной ортодромной тахикардии у больного со скрытым пучком Кента при проведении ЧПЭС. Обозначения: ЧПЭГ – чреспищеводная электрограмма, A – осцилляции предсердий, V – осцилляции желудочков. Интервал VA=140 мс – время ретроградного проведения (от желудочков к предсердиям) по пучку Кента, Ст1 и Ст2 – частая и программная стимуляция предсердий.
Относительно редким вариантом наджелудочковых тахикардий у больных с манифестирующим предвозбуждением желудочков по п.Кента, (но в то же время наиболее частым вариантом у пациентов с волокнами Махайма) является пароксизмальная антидромная реципрокная тахикардия (ПАРТ). В основе развития ПАРТ также как и при ПОРТ лежит механизм повторного входа волны возбуждения с участием АВ-соединения и ДПП, но движение импульса по цепи re-entry имеет противоположную направленность. При ПАРТ импульс проводится из предсердий в желудочки по ДПП, а обратно – по АВ-узлу (рис. 3-Б). Вследствие этого возникновение ПАРТ невозможно при скрытых ДПП, когда проведение от предсердий к желудочкам отсутствует. Спонтанное развитие ПАРТ инициируется, как предсердными, так и желудочковыми экстрасистолами, а в условиях внутрисердечного ЭФИ – предсердными и желудочковыми экстрастимулами по механизму, аналогичному описанному для ПОРТ.
Электрокардиографически ПАРТ проявляется тахикардией с «широкими» комплексами QRS, конфигурация которых имеет картину резко выраженного предвозбуждения желудочков в результате их аномальной активации через ДПП (рис. 5). Важно отметить, что морфология комплексов QRS по 12 отведениям ЭКГ во время ПАРТ практически идентична той, которая регистрируется у того же самого больного при проведении тестов, направленных на замедление проведения по АВ-узлу, например, при частой стимуляции предсердий с развитием эффекта “концертино”. В связи с тем, что деполяризация предсердий во время ПАРТ осуществляется ретроградно через АВ-соединение, зубцы Р на ЭКГ во время пароксизма регистрируются после желудочковых комплексов, а интервал RP существенно больше интервала PR, при этом зубцы Р инвертированы в отведениях II, III, aVF. 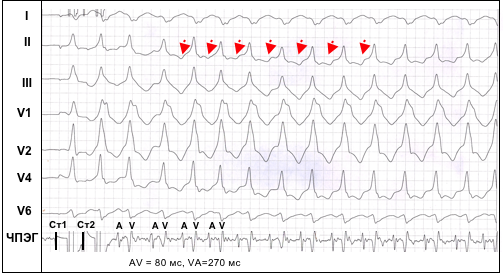
Рис. 5. Синдром ВПУ. Индукция пароксизмальной антидромной тахикардии одиночным экстрастимулом (Ст2) при проведении ЧПЭС.Обозначения: ЧПЭГ – чреспищеводная электрограмма, A – осцилляции предсердий, V – осцилляции желудочков. Антероградное проведение по п. Кента (AV=80 мс), ретроградное по АВ-соединению (VA= 270 мс). Ретроградные Р зубцы во II отведении показаны стрелками.
Электрокардиографическая картина при наличии волокон Махайма аналогична описанной для латентных пучков Кента. Диагноз предвозбужения желудочков по волокнам Махайма ставится исключительно при внутрисердечном ЭФИ. В связи с односторонним предсердно-желудочковым проведением импульсов по этим ДПП, наиболее частым вариантом тахикардии, возникающим у больных с волокнами Махайма, является ПАРТ. Реже у пациентов регистрируется пароксизмальная фибрилляция/трепетание предсердий с проведением по волокнам Махайма. Однонаправленный характер предвозбуждения желудочков исключает возникновение ПОРТ у данных больных. Так как волокна Махайма имеют преимущественно правостороннюю передне-боковую локализацию приступам ПАРТ у этой категории больных обычно свойственно расширение комплекса QRS по типу блокады левой ножки пучка Гиса с отклонением электрической оси сердца влево.
ПОРТ и ПАРТ у больных с синдромами предвозбуждения проявляются пароксизмами с частотой ритма 150-200 в минуту, которая иногда может достигать 250 в минуту. В этих случаях пароксизмы обычно сопровождаются снижением артериального давления, коллапсами, обмороками, появлением симптомов острой левожелудочковой недостаточности. Непароксизмальное течение данных тахикардий ограничивается единичными наблюдениями.
Источник
