Наследственный нефрит код мкб
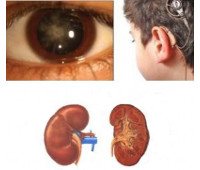
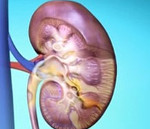
Наследственный нефрит — это генетически обусловленная неиммунная гломерулопатия, часто приводящая к возникновению почечной недостаточности. Проявляется астеническим, интоксикационным синдромами, задержкой физического развития у детей, макрогематурией, полиурией, никтурией, отеками, артериальной гипертензией. Диагностируется с помощью общего анализа мочи, пункционной биопсии, электронной микроскопии. Рекомендована симптоматическая терапия ингибиторами АПФ, блокаторами рецепторов ангиотензина, иммуномодуляторами, анаболиками, ингибиторами кальциневрина. При терминальной ХПН показаны заместительная терапия, трансплантация почки.
Общие сведения
Распространенность наследственного нефрита, по данным зарубежных специалистов в сфере нефрологии, составляет 0,01-0,02%. В России заболевание выявляется у 0,017% детей. Первые наблюдения за пациентами с семейными формами гломерулопатий, приводящими к уремии, проводились в 1902-1923 годах.
В 1927 году британский ученый Артур Альпорт выявил вариант наследственного сочетания уремии и тугоухости, который впоследствии был назван его именем – синдром Альпорта. Генетическая основа наследуемых вариантов нефрита была установлена в 1985 году. Более чем в 80% случаев заболевание дебютирует в возрасте 3-10 лет и протекает более тяжело у пациентов мужского пола, что связано с преобладанием Х-сцепленного типа наследования.
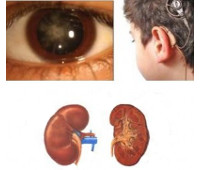
Наследственный нефрит
Причины
Заболевание передается по наследству и связано с генетическим дефектом, при котором нарушается биосинтез коллагеновых волокон IV типа, входящих в состав базальных мембран нефронов и ряда других органов. За кодирование цепей коллагена, которые формируют гломерулярные мембраны, отвечает несколько генов (C0L4A5, C0L4A3, C0L4A4), расположенных в разных хромосомах.
Наследственные формы нефрита генетически гетерогенны, что сказывается на выраженности клинической симптоматики, темпах развития болезни, времени наступления декомпенсации. Чаще всего делециям, точковым мутациям, нарушениям сплайсинга подвергается ген COL4A5, кодирующий α-5 цепь коллагеновых волокон. У 80% пациентов заболевание наследуется по Х-сцепленному типу, у 15% — по аутосомно-рецессивному, у 5% — по аутосомно-доминантному.
Патогенез
Механизм развития патологических изменений при наследственном нефрите основан на нарушении нормальной структуры базальных мембран в тканях почек и некоторых других органов. При мутации гена C0L4A5, который расположен в локусе Xq21.3 на длинном плече Х-хромосомы, изменяется строение α-5 цепи коллагена 4 типа. Повреждение генов C0L4A3, C0L4A4, локализованных во 2-й хромосоме, сопровождается нарушением синтеза α-3 и α-4 цепей коллагеновых волокон.
Аномалии любой из этих цепей влияют на формировании базальных мембран гломерул, дистальных канальцев, собирательных трубочек. Из-за более плотного многослойного переплетения или неправильного пространственного распределения волокон базальные мембраны утолщаются, расслаиваются, истончаются. В почечных тельцах происходит пролиферация мезангиоцитов, накапливается мезангиальный матрикс, клубочки склерозируются, при этом локальный гломерулосклероз сменяется сегментарным, глобальным и усугубляется гиалинозом.
Одновременно атрофируются канальцы, развивается интерстициальный фиброз, кроме нормальных клеток интерстиция появляются пенистые клеточные элементы. Патоморфологические изменения клинически проявляются нарушением функций фильтрации и реабсорбции. Поскольку аналогичные волокна коллагена входят в состав специфических мембран хрусталика и кортиева органа, у пациентов, кроме урологической патологии, отмечаются наследственные формы нарушения зрения, слуха.
Классификация
При систематизации форм наследственного нефрита учитывают характер и выраженность клинических проявлений нефрологической патологии, динамику развития заболевания, время появления почечной недостаточности, наличие признаков поражения других органов. Существование различных вариантов патологии обусловлено типом и степенью экспрессии мутировавших генов. Специалисты в сфере клинической урологии и медицинской генетики выделяют следующие формы наследственной нефропатии:
- Тип I: ювенильный нефрит с поражением почек, тугоухостью и нарушениями зрения (синдром Альпорта). Проявляется при повреждении гена C0L4A5 (сцепленное с Х-хромосомой доминантное наследование). Манифестирует рано, отличается прогредиентным течением с развитием ХПН. У 50% пациентов терминальные стадии почечной недостаточности возникают до 25 лет, у 90% — до 40 лет.
- Тип II: наследственная форма нефрита без тугоухости. Передается по аутосомно-рецессивному механизму. Мутации выявляются в обоих аллелях генов COL4A3 или COL4A4. В клинической картине проявляется почечная симптоматика. Заболевание имеет прогрессирующее течение, терминальная почечная недостаточность формируется к 30 годам.
- Тип III: доброкачественная семейная гематурия. Наследуется по аутосомно-доминантному типу и связана с мутацией одного из генов 2-й хромосомы (COL4A3 либо COL4A4). Проявляется позже, иногда во взрослом возрасте. Отличается малопрогредиентным течением с умеренно выраженной нефрологической симптоматикой и низкой вероятностью развития ХПН.
Симптомы наследственного нефрита
На раннем этапе заболевания клиническая картина характеризуется общими нарушениями: замедлением темпов роста и физического развития, интоксикационным синдромом, проявляющимся слабостью, быстрой утомляемостью, головокружениями, бледностью и сухостью кожных покровов, ухудшением аппетита, снижением мышечного тонуса, частыми головными болями, шумом в ушах, бессонницей.
При прогрессировании нефрита возникают такие симптомы, как частое мочеиспускание, увеличение объема мочи, выделяемого ночью, боль в области живота или таза, появление утренних отеков, видимой крови в моче (макрогематурия), стойкое повышение артериального давления. Кроме того, у пациента с наследственными гломерулопатиямии могут выявляться стигмы (малые аномалии эмбриогенеза) – деформация ушных раковин, эпикант, высокое небо, асимметрия грудной клетки, синдактилия (сращивание двух и более пальцев).
У 30-50% больных определяются признаки нарушения слуха — от незначительных изменений, выявляемых на аудиограмме, до полной нейросенсорной глухоты. В 15-30% случаев диагностируются аномалии строения хрусталика и нарушения зрения в виде переднего лентиконуса, миопии, гиперметропии, астигматизма, катаракты, кератоконуса, сферофакии, пигментного ретинита, амавроза, нистагма и др.
Осложнения
При длительном течении наследственного нефрита происходит постепенная гибель нефронов, вследствие чего заболевание обычно осложняется нарастающей почечной недостаточностью. При ювенильных формах нефропатии ХПН возникает к 16-20 годам и при отсутствии адекватного лечения приводит к смерти пациента до 30-летнего возраста. Генетически детерминированный нефрит, сопровождающийся нарушением метаболических процессов, может приводить к избыточному образованию и отложению солей, вследствие чего развивается мочекаменная болезнь. При повышении функциональной нагрузки на почки возможно развитие ОПН с необходимостью проведения экстренной терапии.
Диагностика
Важную роль в постановке диагноза наследственного нефрита играет тщательное генеалогическое исследование. У 80% больных удается выявить в роду семейные формы урологической патологии, наследуемое снижение слуха, зрения с более выраженной симптоматикой у мужчин. При предполагаемой связи заболевания с генетическими аномалиями рекомендованы методы исследований, которые выявляют признаки повреждения базальных мембран, функциональной недостаточности почек, морфологические изменения паренхимы, характерные для наследственных форм нефрита:
- Общий анализ мочи. Не менее чем в двух пробах мочи, собранных в разное время, определяются измененные эритроциты в количестве от 3 единиц в поле зрения и больше. Характерны протеинурия (более 0,35 г/л), лейкоцитурия, цилиндрурия, нарастающие по мере развития заболевания.
- Пункционная биопсия почек. При гистологическом изучении биоптата почек в канальцах выявляются скопления эритроцитов, интерстициальная ткань инфильтрирована, клубочки уплотнены. При иммунофлюоресцентном анализе выявляется атипичный коллаген 4 типа.
- Электронная микроскопия. На начальных этапах нефрита гломерулярные базальные мембраны утончены, на более поздних стадиях они истончаются или утолщаются, становятся слоистыми, расщепленными. Характерна пролиферация мезангиоцитов, расширение мезангия.
Методы, направленные на выявление мутировавшего гена, в настоящее время применяются редко в связи с технической сложностью и высокой стоимостью исследования. О развитии почечной недостаточности, осложняющей течение нефрита наследственного типа, свидетельствуют изменения биохимии крови (нарастание уровней креатинина, мочевой кислоты, азота мочевины, снижение уровня общего белка) и соответствующие изменения в анализе мочи (положительные почечные пробы).
Заболевание дифференцируют с паранеопластической нефропатией, туберкулезом почек, острым и хроническим гломерулонефритом, пиелонефритом, мочекаменной болезнью, подагрическим интерстициальным нефритом, поражениями гломерул при системных заболеваниях соединительной ткани. Кроме осмотра нефролога или уролога пациенту рекомендованы консультации медицинского генетика, по показаниям — оториноларинголога, офтальмолога, терапевта, эндокринолога, ревматолога, иммунолога, онколога, онкогематолога.
Лечение наследственного нефрита
Эффективной этиопатогенетической терапии заболевания не предложено. Назначение гормонов и иммуносупрессоров обычно оказывается неэффективным. Пациентам с наследственной формой нефрита рекомендована ренопротекция: низкобелковая диета, ограничение физических нагрузок, санация очагов хронической инфекции, осторожность при проведении плановой вакцинации и назначении препаратов с нефротоксическим действием. Для предотвращения раннего развития интерстициального фиброза назначается активная антипротеинурическая терапия, предотвращающая повреждение и атрофию эпителиоцитов почечных канальцев:
- Ингибиторы ангиотензин-превращающего фермента (иАПФ). Являются препаратами первой линии; вызывают дилатацию сосудов, улучшают почечный кровоток, снижают повышенное внутриклубочковое давление, уменьшают реабсорбцию натрия и воды. За счет ингибиции ангиотензина II оказывают антифиброгенный эффект и тормозят развитие тубулоинтерстициального фиброза.
- Блокаторы рецепторов ангиотензина (БРА). Применяются как средства второй линии. Связывают АТ-1-рецепторы ангиотензина II, блокируя его действие. Хотя почечные эффекты БРА в целом сходны с иАПФ, лекарственные средства этой группы влияют более мягко и точечно, не воздействуют на ангиотензин-превращающую ферментную систему, ионные каналы, другие рецепторы.
Противопротеинурическое лечение дополняют витаминными комплексами, витаминоподобными препаратами, лекарственными средствами с иммуномодулирующим и анаболическим эффектом, ингибиторами кальциневрина, гипербарической оксигенацией. Появление признаков терминальной почечной недостаточности служит показанием для проведения заместительной почечной терапии — гемодиализа, перитонеального диализа, гемофильтрации.
Единственным способом радикального улучшения состояния больного является трансплантация почек, хотя проведение такой операции имеет специфические показания и противопоказания по сравнению с другими видами нефрологической патологии. При выборе донора-родственника необходимо учитывать, что у него также может быть бессимптомная наследственная предрасположенность к нефриту, которая декомпрессируется после удаления одной из почек. Кроме того, наличие нормальной альфа-цепи коллагена, присутствующей в базальных мембранах трансплантируемого органа, может спровоцировать иммунный ответ и отторжение почки.
Прогноз и профилактика
Болезнь характеризуется прогредиентным течением, ранним нарушением работы почек. Прогноз наследственного нефрита неблагоприятный: ХПН может формироваться даже у детей, вызывая раннюю инвалидизацию пациента. Однако проведение адекватной симптоматической или заместительной терапии позволяет замедлить прогрессирование патологического процесса. Важное звено профилактики — ранняя диагностика заболевания в медико-генетических лабораториях. При подозрении на наследственный характер гломерулопатии проводят скрининг всех членов семьи, особенно тех, кто имеет в анамнезе артериальную гипертензию, заболевания органов зрения и слуха, множественные малые аномалии развития.
Источник
Связанные заболевания и их лечение
Описания заболеваний
Национальные рекомендации по лечению
Стандарты мед. помощи
Содержание
- Синонимы диагноза
- Описание
- Дополнительные факты
- Причины
- Патогенез
- Классификация
- Симптомы
- Возможные осложнения
- Диагностика
- Лечение
- Список литературы
Другие названия и синонимы
Семейный гломерулонефрит.
Названия
Название: Наследственный нефрит.
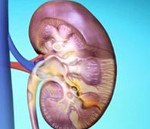
Наследственный нефрит
Синонимы диагноза
Семейный гломерулонефрит.
Описание
Потомственный Джейд. Это генетически обусловленная неиммунная гломерулопатия, обычно приводящая к почечной недостаточности. Это проявляется астеническими синдромами, интоксикацией, задержкой физического развития у детей, макрогематурией, полиурией, никтурией, отеками, артериальной гипертонией. Поставлен диагноз: общий анализ мочи, пункционная биопсия, электронная микроскопия. Рекомендуется симптоматическая терапия ингибиторами АПФ, блокаторами рецепторов ангиотензина, иммуномодуляторами, анаболиками и ингибиторами кальциневрина. При терминальной почечной недостаточности показаны заместительная терапия и трансплантация почки.

Наследственный нефрит
Дополнительные факты
Распространенность наследственного нефрита, по данным зарубежных экспертов в области нефрологии, составляет 0,01-0,02%. В России заболевание выявляется у 0,017% детей. Первые наблюдения за пациентами с семейными формами гломерулопатии, приводящими к уремии, были сделаны в 1902-1923 гг.
В 1927 году британский ученый Артур Альпорт выявил вариант наследственной комбинации уремии и потери слуха, который впоследствии был назван в его честь – синдром Альпорта. Генетическая основа наследственных вариантов нефрита была установлена в 1985 году. В более чем 80% случаев заболевание начинается в возрасте от 3 до 10 лет и является более тяжелым у пациентов мужского пола из-за преобладания л наследование связано с X.
Причины
Заболевание является наследственным и связано с генетическим дефектом, при котором нарушается биосинтез коллагеновых волокон типа IV, которые являются частью базальных мембран нефронов и многих других органов. Несколько генов (C0L4A5, C0L4A3, C0L4A4), расположенных на разных хромосомах, ответственны за кодирование цепей коллагена, которые образуют клубочковые мембраны.
Наследственные формы нефрита являются генетически неоднородными, что влияет на выраженность клинических симптомов, скорость развития заболевания, время, когда происходит декомпенсация. Чаще всего ген COL4A5, кодирующий α-5 цепь коллагеновых волокон, удаляется, точечные мутации и нарушения сплайсинга. У 80% пациентов заболевание наследуется по Х-сцепленному типу, у 15% – по аутосомно-рецессивному, у 5% – по аутосомно-доминантному.
Патогенез
Механизм развития патологических изменений при наследственном нефрите основан на нарушении нормальной структуры базальных мембран в тканях почек и некоторых других органов. Мутация в гене C0L4A5, который расположен в локусе Xq21,3 на длинном плече Х-хромосомы, изменяет структуру цепи α-5 коллагена типа 4. Повреждение генов C0L4A3, C0L4A4, расположенных на 2-й хромосоме сопровождаются нарушением синтеза α-3 и α-4 цепей коллагеновых волокон.
Аномалии одной из этих цепей влияют на формирование базальных мембран клубочков, дистальных канальцев и собирательных протоков. Из-за более плотного многослойного плетения или неправильного пространственного распределения волокон мембраны в основании утолщаются, отслаиваются и истончаются. В почечных органах происходит пролиферация мезангиоцитов, накапливается мезангиальный матрикс, клубочки склерозируются, а местный гломерулосклероз сменяется сегментарным гломерулосклерозом, глобальным и усугубляемым гиалинозом.
В то же время развивается атрофия канальцев, развивается интерстициальный фиброз, помимо нормальных интерстициальных клеток появляются пенистые клеточные элементы. Патоморфологические изменения клинически проявляются нарушением функций фильтрации и реабсорбции. Поскольку сходные коллагеновые волокна являются частью специфических мембран хрусталика и кортиева органа, у пациентов, помимо урологической патологии, отмечаются наследственные формы нарушения зрения и слуха.
Классификация
При систематизации форм наследственного нефрита учитываются характер и степень выраженности клинических проявлений нефрологической патологии, динамика развития заболевания, время начала почечной недостаточности, наличие признаков повреждения других органов. Наличие нескольких вариантов патологии определяется типом и степенью экспрессии мутированных генов. Специалисты в области клинической урологии и медицинской генетики выделяют следующие формы наследственной нефропатии: Ювенильный нефрит с поражением почек, потерей слуха и нарушением зрения (синдром Альпорта). Это проявляется, когда ген C0L4A5 поврежден (доминантное наследование связано с Х-хромосомой). Проявляется рано, отличается прогрессирующим течением с развитием хронической почечной недостаточности. У 50% пациентов терминальная стадия почечной недостаточности наступает до 25 лет, у 90% – до 40 лет. Наследственная форма нефрита без потери слуха. Он передается по аутосомно-рецессивному механизму. Мутации обнаруживаются в двух аллелях генов COL4A3 или COL4A4. В клинической картине появляются почечные симптомы. Заболевание имеет прогрессирующее течение, терминальная стадия заболевания почек формируется к 30 годам. Доброкачественная семейная гематурия. Он унаследован от аутосомно-доминантного типа и связан с мутацией в одном из генов 2-й хромосомы (COL4A3 или COL4A4). Появляется позже, иногда в зрелом возрасте. Он характеризуется медленным прогрессированием с умеренными нефрологическими симптомами и низкой вероятностью развития хронической почечной недостаточности.
Симптомы
На ранних стадиях заболевания клиническая картина характеризуется общими нарушениями: замедлением роста и физического развития, синдромом интоксикации, который приводит к слабости, усталости, головокружению, бледности и сухости кожи, плохому аппетиту, снижению мышечного тонуса, частым головным болям, шуму в ушах и бессоннице манифесты.
По мере прогрессирования нефрита появляются такие симптомы, как частое мочеиспускание, увеличение мочеиспускания по ночам, боль в области живота или таза, появление утреннего отека, видимая кровь в моче (макрогематурия) и постоянное повышение артериального давления. Кроме того, у пациента с наследственной гломерулопатией может быть выявлено клеймо (небольшие нарушения в эмбриогенезе) – деформация ушных раковин, эпикантуса, высокого неба, асимметрия грудной клетки, синдактилия (слияние двух или более пальцев).
У 30-50% пациентов наблюдаются признаки нарушения слуха – от небольших изменений, обнаруженных на аудиограмме, до полной глухоты. В 15-30% случаев диагностируются аномалии в строении хрусталика и нарушения зрения в виде передней чечевицы, миопия, гиперметропия, астигматизм, катаракта, кератоконус, сферофация, пигментный ретинит, амавроз, нистагм и др. ;
Недомогание. Шум в ушах.
Возможные осложнения
При длительном течении наследственного нефрита происходит постепенная гибель нефронов, что обычно осложняет заболевание с увеличением почечной недостаточности. При юношеских формах нефропатии хроническая почечная недостаточность возникает в возрасте от 16 до 20 лет и, при недостаточном лечении, приводит к смерти пациента в возрасте до 30 лет. Генетический нефрит, сопровождающийся метаболическими нарушениями, может привести к чрезмерному образованию соли и отложению, что вызывает развитие мочекаменной болезни. При увеличении функциональной нагрузки на почки возможно развитие острой почечной недостаточности с необходимостью экстренной терапии.
Диагностика
Точное генеалогическое исследование играет важную роль в диагностике наследственного нефрита. У 80% пациентов можно выявить семейные формы урологической патологии, наследственную потерю слуха и зрения с более тяжелыми симптомами у мужчин. При предполагаемой связи заболевания с генетическими отклонениями рекомендуются методы исследования, позволяющие выявить признаки повреждения базальных мембран, функциональную почечную недостаточность, морфологические изменения в паренхиме, характерные для наследственных форм нефрита:
• Общий анализ мочи. По меньшей мере, в двух образцах мочи, собранных в разное время, измененные эритроциты обнаруживаются в 3 единицах в поле зрения или более. Характерны протеинурия (более 0,35 г / л), лейкоцитурия, цилиндрурия, которые усиливаются по мере развития заболевания.
• Биопсия почки путем укола. При гистологическом исследовании почечных биопсий в канальцах выявляется накопление эритроцитов, инфильтрат интерстициальной ткани, клубочки сосредоточены. Иммунофлуоресцентный анализ выявляет атипичный коллаген типа 4.
• Электронная микроскопия. На ранних стадиях нефрита клубочковые базальные мембраны истончены; на более поздних стадиях они становятся тоньше или толще, они становятся слоистыми, разделенными. Пролиферация мезангиоцитов, характерно расширение мезангиев.
В настоящее время методы идентификации мутантного гена используются редко из-за технической сложности и высокой стоимости исследования. Изменения в биохимии крови (повышение уровня креатинина, мочевой кислоты, азота мочевины, снижение общего белка) и соответствующие изменения в анализе мочи (положительные тесты на почки) свидетельствуют о развитии почечной недостаточности, которая осложняет течение наследственного нефрита.
Заболевание дифференцируется с паранеопластической нефропатией, туберкулезом почек, острым и хроническим гломерулонефритом, пиелонефритом, мочекаменной болезнью, подагрическим интерстициальным нефритом, гломерулярными поражениями при системных заболеваниях соединительной ткани. В дополнение к осмотру нефролога или уролога пациенту рекомендуется проконсультироваться с медицинским генетиком по показаниям: отоларинголог, офтальмолог, врач общей практики, эндокринолог, ревматолог, иммунолог, онколог и гематолог.
Лечение
Эффективной этиопатогенетической терапии заболевания не предлагается. Администрация гормонов и иммунодепрессантов обычно неэффективна. Ренопротекция рекомендуется пациентам с наследственной формой нефрита: низкобелковая диета, ограничение физической активности, восстановление очагов хронической инфекции, осторожность при проведении плановых прививок и назначении препаратов с нефротоксичностью. Для предотвращения раннего развития интерстициального фиброза назначают активную антипротеинурическую терапию для предотвращения повреждения и атрофии эпителиальных клеток почечных канальцев:
• Ингибиторы ангиотензин-превращающего фермента (ингибитор АПФ). Это препараты первой линии; вызывают расширение кровеносных сосудов, улучшают почечный кровоток, снижают повышенное внутричерепное давление, уменьшают реабсорбцию натрия и воды. Благодаря ингибированию ангиотензина II они оказывают антифиброгенное действие и ингибируют развитие тубулоинтерстициального фиброза.
• Блокаторы рецепторов ангиотензина (ARBs). Используется в качестве второй строки носителя. Рецепторы ангиотензина II AT-1 связаны между собой, блокируя его действие. Хотя почечные эффекты БРА, как правило, аналогичны ингибиторам АПФ, препараты этой группы влияют более мягко и на специальной основе, не влияют на систему ангиотензинпревращающего фермента, ионные каналы и другие приемники.
Антипротеинурическую терапию дополняют витаминные комплексы, препараты, аналогичные витаминам, препараты с иммуномодулирующим и анаболическим действием, ингибиторы кальциневрина, гипербарическая оксигенация. Появление признаков терминальной стадии почечной недостаточности служит показанием для заместительной почечной терапии – гемодиализ, перитонеальный диализ, гемофильтрация.
Единственный способ радикально улучшить состояние пациента – это пересадка почки, хотя такая операция имеет определенные показания и противопоказания по сравнению с другими типами нефрологической патологии. При выборе относительного донора следует иметь в виду, что он также может иметь бессимптомную наследственную предрасположенность к нефриту, который декомпрессируется после удаления одной из почек. Кроме того, наличие нормальной альфа-цепи коллагена, присутствующего в базальных мембранах трансплантированного органа, может вызвать иммунный ответ и отторжение почки.
Список литературы
1. Детская нефрология. Практическое руководство/ Под редакцией Лойманна Э. , Цыгина А. Н. , Саркисяна А. А. – 2010.
2. Характеристика наследственного нефрита у детей/ Белькевич А. Г. , Козыро И. А. , Сукало А. В. // Актуальные вопросы педиатрии: сборник материалов межрегиональной научно-практической конференции с международным участием, Гродно, 19-20 апреля 2018 г.
3. Наследственные заболевания почек, протекающие с гематурией/ Игнатова М. С. , Длин В. В. // Российский вестник перинатологии и педиатрии. – 2014.
4. Диагноз и прогноз наследственного нефрита у детей с учетом его клинико-морфологического полиморфизма и генетической гетерогенности: Автореферат диссертации/ Цаликова Ф. Д. – 1997.
Источник
