Остеопения недоношенных код по мкб 10
Связанные заболевания и их лечение
Описания заболеваний
Содержание
- Описание
- Симптомы
- Причины
- Лечение
Названия
Остеопения.
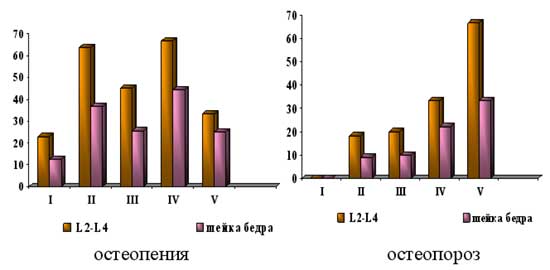
Частота выявления остеопении и остеопороза у пациенток с дисфункцией яичников
Описание
Остеопения относится к минеральной плотности костной ткани, которая ниже, чем нормальная максимальная минеральная плотность костной ткани, но не настолько низка, что может быть классифицирована как заболевание остеопорозом. Минеральная плотность костной ткани является измерением уровня содержания минералов в костях, что указывает на то, насколько они плотные и сильные. Если минеральная плотность вашей костной ткани низкая, по сравнению с нормальной максимальной минеральной плотностью костной ткани, у вас остеопения. Остеопения означает, что вы подвержены большому риску того, что, со временем, минеральная плотность вашей костной ткани станет настолько низкой, по сравнению с нормальным значением, что у вас разовьется остеопороз.
Симптомы
При остеопении симптомы не проявляются. У вас нет болей или изменений в то время. Хотя кость становится тоньше, и риск переломов кости повышается, с потерей костью своей плотности.
Причины
С возрастом у людей кости становятся тоньше естественным путём, это следствие достижения среднего возраста, так как существующие клетки костей реабсорбируются организмом быстрее, чем появляются новые кости. Когда это происходит, кости теряют минералы, вес (массу) и структуру, что делает их слабыми и повышает риск возникновения перелома. Все люди теряют костную массу после достижения максимальной минеральной плотности костной массы в возрасте, примерно, 30 лет. Чем толще ваши кости в возрасте 30 лет, тем дольше времени занимает процесс развития остеопении или остеопороза.
Некоторые люди, у которых остеопения, могут и не терять костную массу. Возможно, низкая плотность костной массы является естественной для них. Остеопения также может случиться в результате различных причин, болезни или лечения. У женщин большая вероятность развития остеопении и остеопороза, чем у мужчин. Так как у женщин максимальная минеральная плотность костной ткани ниже, и процесс потери костной массы происходит быстрее из-за гормональных изменений, которые происходят после менопаузы. Как у мужчин, так и у женщин следующие факторы приводят к развитию остеопении:
*Расстройства пищевого поведения или проблемы с метаболизмом, которые не дают возможности организму получать и усваивать достаточное количество витаминов и минералов.
*Химиотерапия, или приём медикаментов, таких как стероиды, для лечения ряда заболеваний, включая астму.
*Воздействие радиации.
Если в семейном анамнезе присутствуют заболевание остеопорозом, у вас худоба, вы европеоидного или азиатского происхождения, у вас ограничение физической активности, вы курите, злоупотребляете алкоголем, регулярно употребляете «Кока-Колу», то это повышает риск развития остеопении, и, со временем, остеопороза.
Лечение
Остеопения лечится путём принятия мер по предупреждению её прогрессирования и, у некоторых людей, путём принятия медикаментов. Образ жизни может сократить потерю костной массы, которая приводит к заболеванию остеопенией и остеопорозом.
Для развития скелета важную роль играет рацион питания. Наиболее важным минералом для костной массы является кальций. Источниками кальция являются молоко и другие молочные продукты, зелёные овощи и продукты питания, обогащенные кальцием.
Возможно, ваш врач посоветует вам принимать пищевые добавки с кальцием, часто в соединении с витамином D. Витамин D способствует усвоению кальция и других минералов вашим организмом. Он содержится в яйцах, лососе, сардинах, рыбе-меч и рыбьем жире. Его добавляют в молоко или принимают в виде пищевых добавок. Кроме этого вы можете получать его из продуктов питания, ваш организм также синтезирует витамин D вследствие воздействия солнечного света.
Физические упражнения также важны для поддержания силы вашего скелета, так как кость формируется в ответ на напряжение. Весовые упражнения, такие как ходьба, походы, танцы являются наилучшими для укрепления костей. Добавив упражнения по поднятию небольших тяжестей или с эластичной лентой, вы сможете укрепить кости верхней части тела. Проконсультируйтесь со своим врачом или физиотерапевтом касательно программы тренировок.
Кроме питания и физических упражнений, отказ от курения и избежание злоупотребления алкоголем и газированными напитками типа «Кока-Кола», помогут вам сократить риск потери костной массы.
Существуют лекарственные препараты, которые лечат процесс утончения костей, но они обычно принимаются в случае прогрессирования остеопении и перехода её в более тяжёлое состояние, то есть остеопороз. Лекарства, которые могут приниматься от остеопении, включают бифосфаты, ралоксифен и заменители гормонов.
Источник
Остеопения и рахит недоношенных новорожденных детей – клиника, диагностика, лечение
Заболевание вызвано сочетанным дефицитом кальция (и фосфора) и витамина D у недоношенных детей. Остеопения недоношенных — это метаболическое заболевание костной ткани, связанное с низкой минерализацией костей скелета. В патогенезе может иметь значение нарушение минерализации зон роста кости, поэтому термины «остеопения недоношенных» и «рахит недоношенных» в литературе часто используют как взаимозаменяемые.
У недоношенных детей после рождения скорость минерализации костей скелета замедлена по сравнению с таковой во внутриутробном периоде, подобно тому как замедляется во внеутробном периоде скорость роста. Наиболее тяжелое осложнение указанной патологии — переломы костей. Чаще всего отмечаются переломы ребер, но переломы длинных трубчатых костей встречаются редко.
Остеопения/рахит отмечается практически у каждого недоношенного ребенка, родившегося с массой тела менее 1500 г. Наиболее тяжелые по состоянию недоношенные дети имеют наиболее выраженную остеопению. Таким образом, частота возникновения рахита (иногда переломов костей) в целом обратно пропорциональна массе тела при рождении. Если тщательно проанализировать результаты рентгенографии, то частота переломов у недоношенных детей колеблется от 20 до 32%. У детей, имеющих массу тела при рождении менее 1000 г, она возрастает до 50-60%.
Описания гистологических изменений при данной патологии немногочисленны. Считается, что ее этиология предполагает участие многих факторов. Как уже было указано ранее, наиболее значимым фактором являются ограниченные запасы кальция (и фосфора) в костной ткани при рождении, а также сниженная скорость минерализации кости по сравнению с внутриутробным периодом.
Остеопения отмечается даже в тех случаях, когда недоношенные дети в качестве питания получают специально разработанные для младенцев с ОНМТ смеси с высоким содержанием минералов или фортификаторы грудного молока.
В опубликованных в последнее время обзорах есть доказательства роли сниженной нагрузки на кость в возникновении остеопении недоношенных. У данной категории младенцев нагрузка на кость ограничена выполнением пассивных или активных мышечных движений. Увеличение нагрузки на кость (например, в виде пассивных движений с вовлечением в работу суставов) способствует формированию костной ткани, в то время как снижение нагрузки (уменьшение физической активности) ведет к резорбции кости.
Две линии доказательств указывают на важность нагрузки на кость у недоношенных детей. Во-первых, было выявлено повышение уровня биохимических маркеров резорбции кости у недоношенных детей (гидроксипролина, телопептида коллагена типа 1, щелочной фосфатазы). Во-вторых, исследования показали, что внедрение программ, стимулирующих пассивную физическую нагрузку у недоношенных детей, улучшает параметры минерализации костной ткани. Удивительно, но программы пассивных упражнений показали свою эффективность, даже если применяли кратковременные упражнения (5-10 мин/сут).
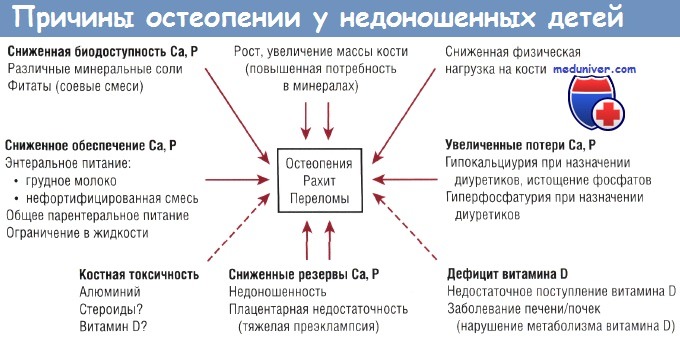
С другой стороны, дефицит витамина D не является частой причиной заболевания костной ткани у недоношенных детей в тех группах, где есть «насыщение» по витамину D. Недоношенные дети с остеопенией обычно имеют нормальные уровни 25(OH)D и повышенные уровни l,25(OH)2D. Пероральный прием витамина D в дозе 2000 ME/ сут в течение 6 нед не влияет на частоту возникновения остеопении у недоношенных детей, что позволяет говорить об адекватности дозы 200-400 МЕ/сут. Другие составляющие патогенеза остеопении недоношенных показаны на рисунке.

Диагноз «остеопения» ставят на основании результатов рентгенологического и лабораторного обследования. Физикальное обследование не столь значимо для выявления заболевания, за исключением тех стадий его развития, когда можно обнаружить крепитацию и припухлость в местах переломов длинных костей. В более старшем возрасте можно выявить рахитические четки в зонах костно-хрящевого соединения и краниотабес.
Поскольку опора на ноги в этом возрасте не столь значима, те очевидные симптомы рахита, которые проявляются искривлением нижних конечностей у детей старшего возраста, не имеют клинического значения.
В большинстве случаев остеопению диагностируют при проведении рутинной рентгенографии, когда выявляют выраженную гипо-минерализацию или признаки произошедших ранее переломов ребер. В случае более тяжелых форм заболевания на стандартных рентгенограммах костей запястья и коленей могут быть видны классические признаки рахита, но обычно они не заметны до двухмесячного возраста ребенка.
Следует указать, что стандартная рентгенография не способна выявить сниженную минерализацию костной ткани до того момента, пока не произойдет потеря 30-40% минерального состава костной ткани. Для проведения в исследовательских целях диагностики костных изменений у недоношенных детей более подходящими считают технологии, обладающие специфической чувствительностью, такие как одиночная фотонная абсорбциометрия, двойная энергетическая рентген-абсорбциометрия, количественная компьютерная томография и трансмиссионная ультразвуковая диагностика.
Для диагностики остеопении недоношенных применяют ряд биохимических маркеров сыворотки крови. Они включают кальций, фосфор, щелочную фосфатазу, паратиреоидный гормон, 25(OH)D, l,25(OH)2D и остеокальцин. Исследуя мочу, можно оценить фракционную экскрецию кальция и тубулярную реабсорбцию фосфата, а также отношение кальций/креатинин. Низкую концентрацию фосфора в сыворотке (менее 45 мг/л) можно считать наилучшим индикатором дефицита минералов у данной категории детей.
Согласно рекомендациям Комитета по питанию Американской академии педиатрии (American Academy of Pediatrics Committee on Nutrition) и некоторых других организаций, в США и Канаде младенцам с ОНМТ, имеющим остеопению, не рекомендуют назначение суточной дозы витамина D более 200-400 ME.
Высокие концентрации l,25(OH)2D и нормальные уровни 25(OH)D практически у всех детей, имеющих указанную патологию, подтверждают правильность упомянутых рекомендаций; детям с ОНМТ не следует назначать в качестве питания продукты, содержащие неадекватное количество кальция и фосфора, например нефортифицированное грудное молоко. Увеличение суточной дозы витамина D до 960 ME и выше не подтвердило эффективности. Потребности в витамине D при парентеральном его введении еще менее ясны.
Впрочем, при использовании современных мультивитаминных препаратов для парентерального введения сложно превысить суточную дозу витамина D 400 ME, не вызывая одновременно передозировки других витаминов-компонентов комплексного препарата. Тем не менее недоношенные дети, длительно получающие полное парентеральное питание, имеют адекватный статус по витамину D даже при получении его в дозе 30-35 МЕ/кг/сут.
Несмотря на то что получены доказательства пользы физической нагрузки (при выполнении пассивных мышечных движений), наиболее важным компонентом профилактики и лечения остается адекватное обеспечение ребенка кальцием и фосфором, без которого любые физические нагрузки на кость будут неэффективными. Вполне логично, что при расчете необходимой дозы минералов преследуют цель достижения скорости минерализации кости, характерной для таковой у плода.
Для этого ребенку необходимо получать энтеральным путем кальций в дозе примерно 200 мг/кг/сут и фосфор в дозе 90 мг/кг/сут, принимая во внимание, что усваивается только 65% кальция (в лучшем случае) и 80% фосфора.
Существуют специальные смеси для детей с ОНМТ, которые позволяют удовлетворить указанные потребности в минералах. Можно также использовать готовые фортификаторы грудного молока, содержащие определенное количество кальция и фосфора. Как уже было сказано ранее, у детей с ОНМТ в первые 8 нед жизни довольно сложно добиться скорости минерализации кости, соответствующей таковой во внутриутробном периоде.
Однако при назначении ребенку кальция и фосфора в указанных ранее дозах можно предотвратить развитие тяжелого рахита и остеопении с переломами костей. Следует отметить, что «наверстывание» минерализации кости будет происходить у этих младенцев еще в течение многих месяцев после выписки из стационара.
Как уже было сказано, профилактика и/или лечение остеопении у детей с ОНМТ, получающих полное парентеральное питание, служит основанием для более пристального внимания к введению некоторых внутривенных растворов. Концентрации кальция и фосфора в них не позволяют достигнуть внутриутробной скорости минерализации кости.
Однако используемые для парентерального питания препараты все же позволяют предупредить переломы костей и развитие рахита. Применение внутривенных препаратов, содержащих 15 ммоль (60 мг/дл) кальция и 15 ммоль (46 мг/дл) фосфора, может способствовать достижению желаемых показателей минерального гомеостаза (как биохимических маркеров, так и уровня кальциотропных гормонов).
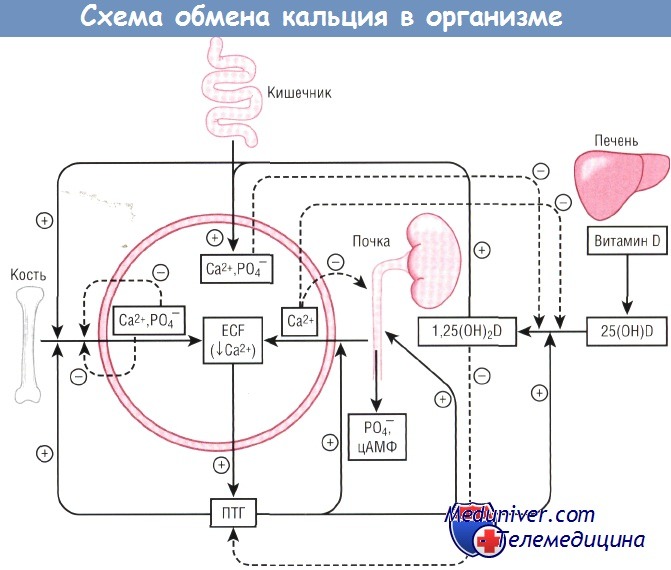
Схема гомеостаза кальция, демонстрирующая взаимодействия между кальцием, кальциотропными гормонами и системой органов.
1,25(OH)2D—1,25-дигидроксивитамин D;
25(OH)D—25-гидроксивитамин D;
ECF — эргокальциферол;
ПТГ — паратиреоидный гормон;
цАМФ — циклический аденозинмонофосфат.
Рахит, обусловленный дефицитом витамина D
В США встречаются случаи рахита у детей ранней возрастной группы, связанные с неадекватным поступлением в организм витамина D и дефицитом солнечного света. Обычно причиной служит выраженный гиповитаминоз D.
Большинство указанных случаев заболевания относились к детям, находящимся исключительно на грудном вскармливании без дополнительного введения витамина D. Следует отметить, что содержание витамина D в грудном молоке минимально. Анализируя случаи рахита у детей, можно отметить, что у этих младенцев часто наблюдалась повышенная пигментация кожи, а также они редко находились под воздействием солнечного света.
Вместе с тем на многих территориях США в зимние месяцы воздействие солнечного света не может считаться достаточно эффективным для синтеза витамина D в коже. Рекомендации по профилактике гиповитаминоза D заключаются в обеспечении всех детей, находящихся на грудном вскармливании, витамином D в дозе 200-400 МЕ/сут до тех пор, пока они не смогут получать адекватное количество витамина D из витамин D-фортифицированных смесей или другой пищи.
– Также рекомендуем “Потребность в витамине А у новорожденных детей”
Оглавление темы “Потребности в витаминах у детей”:
- Потребности в кальции и витамине Д у новорожденных детей
- Ранняя гипокальциемия недоношенных новорожденных детей – клиника, диагностика, лечение
- Остеопения и рахит недоношенных новорожденных детей – клиника, диагностика, лечение
- Потребность в витамине А у новорожденных детей
- Дефицит витамина А и его токсичность у новорожденных детей
- Влияние больших доз витамина А на недоношенных новорожденных детей
- Физиология обмена витамина Е и его эффекты
- Потребность в витамине Е у новорожденных детей
- Дефицит витамина Е у новорожденных детей – клиника, диагностика
- Влияние больших доз витамина Е на недоношенных новорожденных детей
Источник
Рахит — традиционно важная проблема в педиатрии [1]. Исходя из установленного вовлечения центральной и вегетативной нервной системы при этой патологии (c соответствующей сопутствующей симптоматикой), имеются основания рассматривать витамин D-дефицитный рахит в качестве соматоневрологического состояния [2]. В этой связи на протяжении более двух последних десятилетий в целом каскаде публикаций нами неоднократно рассматривались различные аспекты классического (витамин D-дефицитного) рахита у детей [3–18]. В частности, речь шла о критике Всемирного консенсуса по профилактике и лечению нутритивного рахита и предложениях по его совершенствованию [17, 18].
Необходимо признать, что, к сожалению, неклассические формы рахита знакомы педиатрам и представителям различных педиатрических специальностей в меньшей степени, чем витамин D-дефицитный рахит. Поэтому в предлагаемой вашему вниманию статье будут рассмотрены современные представления о рахите недоношенных детей.
Названия и определение болезни
В англоязычной литературе эта разновидность рахита известна как rickets of prematurity [1].
Другое название этой болезни — остеопения недоношенных детей (osteopenia of prematurity) [19].
В зарубежной литературе последних лет некоторые исследователи предпочитают называть рахит недоношенных «метаболической болезнью костей недоношенных детей» (metabolic bone disease of prematurity) [20].
Обратите внимание, что даже два предлагаемых выше термина акцентируют внимание на костных аспектах болезни, таким образом, игнорируя полиорганный характер этого вида патологии, включая поражение нервной системы недоношенных младенцев.
Рахит недоношенных детей — патологическое состояние, выявляемое у преждевременно родившихся младенцев с массой тела при рождении < 1500 г, обусловленное не только нехваткой витамина D, но и дефицитом кальция и фосфора (фосфатов) [1, 11–13, 15, 20, 21].
Этиология и патогенез
Болезнь обусловлена преимущественно отсутствием возможности обеспечить адекватные уровни поступления и утилизации в организме кальция и фосфора, которые соответствовали бы таковым во внутриутробном (антенатальном) периоде развития. Среди этиологических факторов, предрасполагающих к рахиту недоношенных, следует перечислить следующие:
- низкий гестационный возраст (ГВ) — обычно < 31 недели;
- низкая масса тела при рождении (< 1500 г);
- внутриутробная гипотрофия или задержка внутриутробного развития (ЗВУР);
- низкие запасы (эндогенный дефицит) минеральных веществ при рождении;
- алиментарные факторы: недостаточное поступление витамина D при оральном/энтеральном/парентеральном питании;
- экзогенный дефицит Са, РО4, Mg и Cu, поступающих в организм алиментарным путем;
- незрелость Са-регулирующих систем;
- перенесенная гипоксия/асфиксия;
- терапия антиконвульсантами (фенобарбитал и т. д.);
- неадекватная инсоляция;
- синдромы кишечной мальабсорбции/мальдигестии;
- почечная недостаточность и др. [1, 11–13, 15, 21, 22].
Чем меньше у недоношенных детей оказываются ГВ и масса тела при рождении, тем чаще у них выявляется это патологическое состояние. Так, уже к 28-му дню болезни среди младенцев с массой тела при рождении < 1000 г распространенность рахита недоношенных достигает 56%, а впоследствии приближается к 100% [11].
Вполне естественно, что все большая частота встречаемости рахита недоношенных детей, о которой сообщается в современной медицинской периодике, во многом обусловлена совершенствованием службы неонатальной реанимации/интенсивной терапии и, соответственно, лучшими показателями выживаемости преждевременно родившихся детей, включая глубоко недоношенных.
В настоящее время наибольшее значение в патогенезе рахита недоношенных детей придается неадекватному поступлению с пищей РО4, хотя определенная роль отводится также алиментарному дефициту Са, Сu и пищевых белков. Если в последнем триместре гестации человеческий плод получает ежедневно примерно 5 ммоль (150 мг), а также 75 ммоль (300 мг) Са, то, оказавшись во внеутробном окружении, глубоко недоношенный новорожденный уже не в состоянии получать и утилизировать указанные выше вещества в вышеприведенных количествах. Это обстоятельство неминуемо приводит к дефицитарной депозиции минеральных веществ в костной ткани младенца [11–13, 15, 21, 22].
При выраженном дефиците РО4 у маловесного недоношенного ребенка развивается гиперкальциемия — вследствие неспособности его организма к утилизации Са. Сопутствующий дефицит витамина D сопровождается пониженной абсорбцией Са в кишечнике и препятствует нормальному обмену Са в крови и костной системе [12, 13, 15].
Гипокальциемия обычно манифестирует у глубоко недоношенных детей в первые дни постнатальной жизни, характеризуется транзиторным характером и является отражением нечувствительности тканей к воздействию паратгормона (ПТГ) [1, 11].
Клинические проявления и течение болезни
Рахит недоношенных детей характеризуется выраженными симптомами поражения центральной нервной системы и костной системы, а также острым течением болезни, начиная с первых недель-месяцев жизни младенца. Ни в коем случае не следует считать, что рахит недоношенных детей является прямым эквивалентом классического (витамин D-дефицитного) рахита, развившегося у преждевременно родившихся младенцев [11–13].
Основные проявления болезни преимущественно напоминают таковые при классическом (витамин D-дефицитном) рахите (у недоношенных детей выявляются все «рахитические» признаки поражения костной, мышечной, вегетативной и центральной нервной систем) [1, 11–13, 15, 21, 22].
При рахите недоношенных детей в значительной мере страдают скелетные органы. Уже к концу неонатального периода у детей могут отмечаться увеличение размеров большого родничка и размягчение его краев, формирование избыточной выпуклости лобных отделов черепа с одновременным уплощением его височных отделов, возникновение рахитических «четок» с расширением концов костной части ребер, расширение дистальных отделов диафизов длинных костей, а также появление переломов и/или трещин ребер/длинных костей [1, 11–13, 15, 21, 22].
Существенным отличием от витамин D-дефицитного рахита при описываемой форме болезни можно считать отсутствие выраженной потливости (гипергидроза) [11].
Типичными осложнениями нелеченого рахита недоношенных детей являются гипостатура, гипотрофия (постнатальная), рахитические ателектазы легких, минералодефицитные формы анемии, а впоследствии — гипоплазии эмали зубов [11–13, 15, 21, 22]. Некоторые авторы относят к редким, но серьезным осложнениям рахита недоношенных детей такие состояния, как кардиомиопатия и миелофиброз [23].
Диагностика рахита недоношенных детей
В тех случаях, когда явные признаки болезни у маловесных недоношенных детей по той или иной причине отсутствуют, рекомендуется прибегать к использованию скрининг-тестов. В частности, они предусматривают еженедельное определение в крови содержания Са, PO4 и активности щелочной фосфатазы (ЩФ). Определенное значение имеет периодическое исследование кислотно-щелочного состава крови (метаболический ацидоз способствует разрушению костной ткани) [1, 20, 22].
Обратите внимание на то обстоятельство, что метаболиты витамина D3 (25-гидроксихолекальциферол и 1,25-дигидроксихолекальциферол) при рахите недоношенных детей не считаются обязательными диагностическими маркерами болезни.
При необходимости исследуют содержание в сыворотке крови ПТГ, осуществляют сонографическое исследование костей (метод так называемого «количественного УЗИ») [20].
По достижении детьми, относящимися к группе высокого риска по развитию рахита недоношенных детей, постнатального возраста 6–8 недель, им показано проведение соответствующего рентгенологического исследования для подтверждения/исключения болезни [1, 20].
Профилактика и лечение рахита недоношенных детей
При рахите недоношенных детей профилактика имеет не меньшее, а даже большее значение, чем лечение.
Антенатальная профилактика должна быть инициирована задолго до рождения ребенка. Так, при наличии факторов риска по наступлению преждевременных родов беременным женщинам следует рекомендовать прием препаратов витамина D и кальция (помимо специализированных витаминно-минеральных комплексов), начиная с 24-й недели гестации. Препараты витамина D назначаются в дозе 1000–1500 МЕ/сут или 10 000 МЕ/нед); эта практика сохраняется до момента рождения ребенка. Кроме того, беременным женщинам необходим систематический прием препаратов Са (в количестве не менее 1,5–2,0 г/сут) [11–13, 15, 21, 22].
Постнатальная профилактика рахита недоношенных детей предусматривает обязательное раннее назначение препаратов витамина D, начиная с возраста 7–14 дней. Впоследствии производится систематический прием витамина с обязательным подсчетом полученной курсовой дозы кальциферола. В целом дозы витамина D, используемые в целях адекватной постнатальной профилактики рахита недоношенных детей, существенно превышают таковые, применяемые у детей, родившихся в срок. Это связано как с чрезвычайной вариабельностью потребности недоношенных детей в витамине D (от 400 МЕ/сут до 5000 МЕ/сут), так и с необходимостью продолжительного приема ими препаратов кальциферола — на протяжении двух-трех лет жизни [11–13, 15, 21, 22].
Минимальная суточная потребность в витамине D у недоношенных детей соответствует 400–1000 МЕ, в связи с чем с превентивной целью кальциферол им назначается в количестве не менее 800–1600 МЕ/сут. Вполне возможным представляется назначение профилактических доз витамина D, сопоставимых с лечебными (2000–8000 МЕ/сут). Несмотря на то обстоятельство, что режимы профилактического назначения препаратов витамина D могут существенно различаться, важнейшим условием является обеспечение бесперебойного поступления кальциферола в организм недоношенного ребенка — до окончательной реализации приема полной курсовой дозы [11–13, 15, 21, 22].
Исходя из практического опыта, рекомендуемая курсовая профилактическая доза витамина D на первом году жизни должная составлять порядка 700 тысяч МЕ, а на втором году жизни предусмотрен прием еще 500 тысяч МЕ [11].
Поскольку начальные признаки рахита недоношенных детей зачастую могут возникать еще до завершения периода новорожденности, постнатальная профилактика болезни препаратами витамина D нередко трансформируется в лечение. Поэтому зачастую трудно бывает определить, с какой целью используются препараты витамина D — с профилактической или лечебной [11–13, 21].
К числу дополнительных методов неспецифической профилактики рахита недоношенных детей следует отнести массаж (при отсутствии противопоказаний к его применению), воздушные ванны, регулярные прогулки на свежем воздухе, а также рациональное вскармливание [11–13, 21].
Лечение рахита недоношенных детей предусматривает комплекс мероприятий:
- назначение витаминных препаратов (витамин D и поливитамины);
- применение минеральных добавок;
- диетотерапия [1, 11–13].
Хотя эффективность доз витамина D, превышающих 2000 МЕ/сут, оспаривается некоторыми зарубежными исследователями, применение кальциферола в более высокой дозировке не только является оправданным, но и позволяет добиться скорейшего клинического эффекта. В любом случае, минимальная суточная лечебная доза витамина D всегда должна составлять не менее 2000 МЕ/сут, но более высокая эффективность лечения достигается при назначении кальциферола в дозе от 4000 МЕ/сут до 15000 МЕ/сут [11–13, 15, 21].
Лечебная курсовая доза витамина D не превышает профилактическую и примерно соответствует терапевтической при витамин D-дефицитном рахите III степени (то есть порядка 1 млн МЕ за весь период лечения) [21, 22].
Поливитаминные препараты недоношенным детям назначают так же, как доношенным [11–13].
Назначение минеральных веществ (усиленная их дотация) должно осуществляться до момента набора недоношенными детьми массы тела порядка 3,0–3,5 кг, то есть на протяжении нескольких месяцев [20].
S. E. Rustico и соавт. (2014) сообщили о возможности применения кальцитриола (активной формы витамина D3) при лечении рахита недоношенных детей в сочетании с вторичным гиперпаратиреозом (подтвержденным лабораторно) [24].
Особенности питания при рахите недоношенных детей
Маловесные недоношенные дети не должны получать стандартные адаптированные смеси (заменители грудного молока), а также необогащенное материнское или донорское молоко. Материнское или донорское молоко предварительно обогащается специальными добавками — фортификаторами (последние в течение ряда лет представлены и являются доступными в РФ). При их отсутствии в грудное молоко добавляют нейтральный фосфор (10–15 мг/100 мл), а также Са (20–40 мг/100 мл) [11–13, 15].
При вскармливании недоношенных детей специализированными смесями (в достаточном ассортименте представленными в РФ) необходимости в дополнительном назначении им препаратов Са и/или PO4 не возникает, но детям с ГВ < 30 недель, получающим грудное молоко (материнское или донорское), показан дополнительный прием PO4 (2 ммоль/кг/сут или 60 мг/кг/сут). При гипокальциемии необходим дополнительный прием недоношенными младенцами Са (из расчета 3–4 ммоль/кг/сут или 120–160 мг/кг/сут). Хотя теоретически потребность в Са у маловесных недоношенных детей составляет около 75 мг/сут, доступные препараты кальция обычно назначают в гораздо больших количествах — в связи с относительно низкими уровнями абсорбции и утилизации этого макроэлемента. До 3-недельного возраста препараты Са вводить оральным путем недоношенным детям не рекомендуется, поскольку при этом может нарушаться всасывание пищевых жиров и жирорастворимых витаминов [11–13, 15, 21, 22].
В соответствии с рекомендациями Американской академии педиатрии (American Academy of Pediatrics, AAP) и Европейского общества детских гастроэнтерологов, гепатологов и нутрициологов (European Society for Paediatric Gastroenterology Hepatology and Nutrition, ESPGHAN) недоношенным детям с массой тела при рождении <1 500 г в различных клинических ситуациях предлагаются следующие виды дотации:
1) при проведении полного парентерального питания (ППП) в первые недели жизни: Са — 40–120 мг/кг/сут (AAP) или 1–3 ммоль/кг/сут (ESPGHAN), фосфор — 32–72 мг/кг/сут (AAP) или 1,0–2,2 ммоль/кг/сут (ESPGHAN), витамин D — 160–280 МЕ/сут (AAP);
2) при ППП после первых недель жизни (потребление жидкости 140–150 мл/кг/сут) Са — 75–90 мг/кг/сут (AAP) или 1,8–2,2 ммоль/кг/сут (ESPGHAN), фосфор — 60–70 мг/кг/сут (AAP) или 1,9–2,2 ммоль/кг/сут (ESPGHAN), витамин D — 160–180 МЕ/сут (AAP);
3) при полном энтеральном питании (грудное молоко и/или смесь): Са — 140–160 мг/100 ккал (AAP) или 70–140 мг/100 ккал (ESPGHAN), фосфор — 95–108 мг/100 ккал (AAP) или 50–86 мг/100 ккал (ESPGHAN), витамин D — 200–400 МЕ/сут (AAP) [20].
Заключение
Необходимо констатировать, что по проблематике рахита недоношенных детей имеется еще больше дискутабельных моментов, чем в отношении витамин D-дефицитного рахита. Этот касается определения приоритетного значения дотации минеральных веществ и витамина D (сроки начала антенатальной и постнатальной профилактики, дозы и т. д.). Так, сложно согласиться с мнением P. Alizadeh Taheri и соавт. (2014), считающих, что для профилактики рахита недоношенных детей достаточно назначения витамина D в количестве 200–400 МЕ/сут [25]. Аналогичным образом следует подвергнуть критике рассуждения A. T. Elidrissy (2016) о так называемом «врожденном» рахите [23]. И, наоборот, заслуживает полной поддержки мнение H. E. Karpen (2018) о патологическом влиянии низкого гестационного возраста, перенесенной асфиксии/гипоксии и продолжительном парентеральном питании на состояние костной ткани при рахите недоношенных детей [26].
Хочется выразить надежду, что проблема рахита недоношенных детей, к сожалению, нередко игнорируемая в прошлом, получит скорое решение — для этого необходимо тесное сотрудничество представителей различных педиатрических специальностей (неонатологов, педиатров, реаниматологов, гастроэнтерологов, диетологов, эндокринологов, неврологов и т. д.).
Литература
- Nelson textbook of pediatrics / Kliegman R. M., Stanton B. F., St. Geme III J. W. et al, eds. 20th ed. Philadelphia. Elsevier, 2016. 3474.
- Студеникин В. М., Николаев А. С. Витамин D-дефицитный рахит как соматоневрологическое заболевание // Совр. педиатрия. 2005; 3 (8): 130–135.
- Рахит. В кн.: Справочник педиатра / Под ред. М. Я. Студеникина. М.: Полиформ-3. Издатель-пресс, 1997. С. 370–372.
- Руководство по неонатологии / Под ред. Г. В. Яцык. М.: МИА, 1998. С. 197–201.
- Cтуденикин В. М. Витамин D-дефицитный рахит // Детский доктор. 2000. № 4. 43–46.
- Николаев А. С., Белова Е. М., Чумакова О. В., Студеникин В. М. Роль диеты в профилактике и лечении витамин D-дефицитного рахита // Вопр. детск. диетол. 2003; 1 (3): 44–47.
- Cтуденикин В. М. По поводу статьи Е. В. Неудахина и В. А. Агейкина «Спорные теоретические и практические вопросы рахита у детей на современном этапе» // Педиатрия. 2003; № 4. 110–111.
- Cтуденикин В. М., Рывкин А. И. Рахит, рахитоподобные состояния и спазмофилия. В кн.: Избранные лекции по педиатрии. М.: ИД «Династия», 2005. С. 485–507.
- Студеникин В. М. Витамин D-дефицитный рахит у детей // Детский врач. 2008; № 1: 9–11.
- Рахит у детей (МКБ-10: Е55.0). Глава 5. В кн.: Клиническая диетология детского возраста: руководство для врачей / Под ред. Боровик Т. Э., Ладодо К. С. М.: ООО «Медицинское информационное агентство», 2008. С. 98–123.
- Соматоневрология новорожденных и детей грудного и раннего возраста. В кн.: Неврология раннего детства: от 0 до 3 лет (коллективная монография) / Под ред. Шамансурова Ш. Ш. и Студеникина В. М. Ташкент: Издательско-полиграфический творческий дом «O’Qituvchi», 2010. С. 343–366.
- Рахит(ы) и другие витамин D-дефицитные состояния у детей. В кн.: Детская нейродиетология. Соматоневрологические аспекты: монография / В. Студеникин, С. Турсунхужаева. Saarbrücken (Germany): LAP — Lambert Academic Publishing GmbH &Co.KG, 2012. 105–133.
- Рахиты. В кн.: Нейродиетология детского возраста (коллективная монография) / Под ред. Студеникина В. М. М.: Династия, 2012. С. 520–534.
- Витамин D в нейродиетологии. B кн.: Новые мишени в детской нейродиетологии (коллективная монография) / Под ред. Студеникина В. М. М.: Династия, 2012. С. 186–203.
- Неонатальная неврология (коллективная монография) / Под ред. Студеникина В. М. и Шамансурова Ш. Ш. М.: Медфорум, 2014. С. 277–282.
- Клиническая диетология детского возраста: руководство для врачей / Под ред. Боровик Т. Э., Ладодо К. С. Изд-е 2-е, перераб. и доп. М.: ООО «Издательство «Медицинское информационное агентство», 2015. С. 99–135.
- Студеникин В. М. Рахит: соматоневрология и нейропедиатрия // Лечащий Врач. 2017; № 1: 20–23.
- Студеникин В. М., Казакова К. А., Акоев Ю. С., Мигали А. В. Рахит, недостаточность витамина D и Всемирный консенсус по профилактике и лечению нутритивного рахита: взгляд российских педиатров // Российский педиатрический журнал. 2017; 20 (2): 116–121.
- Çakir U., Tayman C. The effect of thyroid functions on osteopenia of prematurity in preterm infants // J. Pediatr. Endocrinol. Metabol. 2019; 32 (1): 65–70.
- Faienza M. F., D’Amato E., Natale M. P., Grano M., Chiarito M., Brunetti G., D’Amato G. Metabolic bone disease of prematurity: diagnosis and treatment // Front. Pediatr. 2019; 7: 143.
- Студеникин В. М. Рахит недоношенных детей // Вопр. cовр. педиатрии. 2002; 1 (2): 46–49.
- Рахит недоношенных детей. В ?
