Пузырева н и синдром дыхательных расстройств
История изучения гипервентиляционного синдрома (ГВС). Первое клиническое описание ГВС принадлежит Да Коста (1842), который обобщил свои наблюдения за солдатами, участвующими в гражданской войне. Он наблюдал нарушения дыхания и связанные с ними различные неприятные ощущения в области сердца, назвав их «солдатское сердце», «раздраженное сердце». Подчеркивалась связь патологических симптомов с физической нагрузкой, отсюда еще один термин — «синдром усилия». В 1918 г. Lewis предложил другое название — «нейроциркуляторная дистония», которым до сих пор широко пользуются терапевты. Были описаны такие проявления ГВС, как парестезии, головокружения, мышечные спазмы; подмечена связь усиления дыхания (гипервентиляции) с мышечно-тоническими и тетаническими нарушениями. Уже в 1930 г. было показано, что боли в области сердца при синдроме Да Коста имеют не только связь с физической нагрузкой, но и гипервентиляцией в результате эмоциональных нарушений. Эти наблюдения нашли свое подтверждение во время Второй мировой войны. Гипервентиляционные проявления были отмечены как у солдат, так и у мирного населения, что свидетельствовало о важном значении психологических факторов в генезе ГВС.
Этиология и патогенез. В 80–90 годы ХХ столетия было показано, что ГВС входит в структуру психовегетативного синдрома [1]. Основным этиологическим фактором являются тревожные, тревожно-депрессивные (реже — истерические) расстройства. Именно психические расстройства дезорганизуют нормальное дыхание и приводят к гипервентиляции. Дыхательная система, с одной стороны, обладает высокой степенью автономности, с другой — высокой степенью обучаемости и тесной связью с эмоциональным состоянием, особенно тревогой. Эти ее особенности и лежат в основе того факта, что ГВС имеет в большинстве случаев психогенное происхождение; крайне редко его вызывают органические неврологические и соматические заболевания — сердечно-сосудистые, легочные и эндокринные.
Важную роль в патогенезе ГВС играют сложные биохимические изменения, особенно в системе кальций-магниевого гомеостаза. Минеральный дисбаланс приводит к дисбалансу системы дыхательных ферментов, способствует развитию гипервентиляции.
Привычка неправильно дышать формируется под влиянием культуральных факторов, прошлого жизненного опыта, а также стрессовых ситуаций, перенесенных пациентом в детстве. Особенность детских психогений у пациентов с ГВС заключается в том, что в них часто фигурирует нарушение дыхательной функции: дети становятся свидетелями драматических проявлений приступов бронхиальной астмы, сердечно-сосудистых и других заболеваний. Сами пациенты в прошлом нередко имеют повышенную нагрузку на дыхательную систему: занятия бегом, плаванием, игра на духовых инструментах и др. В 1991 г. И. В. Молдовану [1] показал, что при ГВС наблюдается нестабильность дыхания, изменение соотношения между длительностью вдоха и выдоха.
Таким образом, патогенез ГВС представляется многоуровневым и многомерным. Психогенный фактор (чаще всего тревога) дезорганизует нормальное дыхание, в результате чего возникает гипервентиляция. Увеличение легочной, альвеолярной вентиляции ведет к устойчивым биохимическим сдвигам: избыточному выделению углекислого газа (СО2) из организма, развитию гипокапнии со снижением парциального давления СО2 в альвеолярном воздухе и кислорода в артериальной крови, а также респираторному алколозу. Эти сдвиги способствуют формированию патологических симптомов: нарушению сознания, вегетативным, мышечно-тоническим, алгическим, чувствительным и другим нарушениям. В результате происходит усиление психических расстройств, формируется патологический круг.
Клинические проявления ГВС. ГВС может носить пароксизмальный характер (гипервентиляционный криз), но чаще гипервентиляционные расстройства отличаются перманентностью. Для ГВС характерна классическая триада симптомов: дыхательные нарушения, эмоциональные нарушения и мышечно-тонические расстройства (нейрогенная тетания).
Первые представлены следующими типами:
- «пустое дыхание»;
- нарушение автоматизма дыхания;
- затрудненное дыхание;
- гипервентиляционные эквиваленты (вздохи, кашель, зевота, сопение).
- Эмоциональные нарушения проявляются чувствами тревоги, страха, внутреннего напряжения.
Мышечно-тонические расстройства (нейрогенная тетания) включают:
- чувствительные нарушения (онемения, покалывания, жжения);
- судорожные феномены (спазмы мышц, «рука акушера», карпопедальные спазмы);
- синдром Хвостека II–III степени;
- положительную пробу Труссо.
При первом типе дыхательных расстройств — «пустое дыхание» — основным ощущением является неудовлетворенность вдохом, ощущение нехватки воздуха, что приводит к глубоким вдохам. Больным постоянно недостает воздуха. Они открывают форточки, окна и становятся «воздушными маньяками». Дыхательные расстройства усиливаются в агорафобических ситуациях (метро) или социофобических (экзамен, публичное выступление). Дыхание у таких пациентов частое и/ или глубокое.
При втором типе — нарушении автоматизма дыхания — у больных появляется ощущение остановки дыхания, поэтому они непрерывно следят за актом дыхания и постоянно включаются в его регуляцию.
Третий тип — синдром затрудненного дыхания — отличается от первого варианта тем, что дыхание ощущается пациентами как трудное, совершается с большим напряжением. Они жалуются на «ком» в горле, непрохождение воздуха в легкие, зажатость дыхания. Этот вариант назван «атипичная астма». Объективно отмечаются усиленное дыхание, неправильный ритм. В акте дыхания используются дыхательные мышцы. Вид больного напряженный, беспокойный. Исследование легких патологии не выявляет.
Четвертый тип — гипервентиляционные эквиваленты — характеризуют периодически наблюдаемые вздохи, кашель, зевота, сопение. Указанные проявления являются достаточными для поддержания длительной гипокапнии и алкалоза в крови.
Эмоциональные нарушения при ГВС носят в основном тревожный или фобический характер. Наиболее часто наблюдается генерализованное тревожное расстройство. Оно, как правило, не связано с какой-либо конкретной стрессовой ситуацией — у пациента отмечаются в течение продолжительного времени (более 6 мес) различные как психические (ощущение постоянного внутреннего напряжения, неспособность расслабиться, беспокойство по мелочам), так и соматические проявления. Среди последних дыхательные расстройства (чаще «пустое дыхание» или гипервентиляционные эквиваленты — кашель, зевота) могут составлять ядро клинической картины — наряду, например, с алгическими и сердечно-сосудистыми проявлениями.
Значительной степени дыхательные нарушения достигают во время панической атаки, когда развивается так называемый гипервентиляционный криз. Чаще отмечаются расстройства второго и третьего типа — потеря автоматизма дыхания и затрудненное дыхание. У пациента возникает страх задохнуться и другие характерные для панической атаки симптомы. Для постановки диагноза панической атаки необходимо наблюдать четыре из следующих 13 симптомов: сердцебиение, потливость, озноб, одышка, удушье, боль и дискомфорт в левой половине грудной клетки, тошнота, головокружение, ощущение дереализации, страх сойти с ума, страх смерти, парестезии, волны жара и холода. Эффективным методом купирования гипервентиляционного криза и других симптомов, связанных с нарушением дыхания, является дыхание в бумажный или целлофановый мешок. При этом пациент дышит собственным выдыхаемым воздухом с повышенным содержанием углекислого газа, что приводит к уменьшению дыхательного алкалоза и перечисленных симптомов.
Нередко причиной появления ГВС является агорафобия. Это страх, возникающий в ситуациях, которые пациент расценивает как трудные для оказания ему помощи. Например, подобное состояние может возникнуть в метро, магазине и т. д. Такие пациенты, как правило, не выходят из дома без сопровождения и избегают указанных мест.
Особое место в клинической картине ГВС занимает повышение нервно-мышечной возбудимости, проявляющееся тетанией. К тетаническим симптомам относят:
- чувствительные расстройства в виде парестезий (онемения, покалывания, ползающие «мурашки», ощущения гудения, жжения и др.);
- судорожные мышечно-тонические феномены — спазмы, сведения, тонические судороги в руках, с феноменом «руки акушера» или карпопедальных спазмов.
Эти проявления нередко возникают в картине гипервентиляционного криза. Кроме того, для повышения нервно-мышечной возбудимости характерен симптом Хвостека, положительная манжеточная проба Труссо и ее вариант — проба Труссо-Бансдорфа. Существенное значение в диагностике тетании имеют характерные электромиографические (ЭМГ) признаки скрытой мышечной тетании. Повышение нервно-мышечной возбудимости вызвано наличием у больных с ГВС минерального дисбаланса кальция, магния, хлоридов, калия, обусловленного гипокапническим алкалозом. Отмечается четкая связь между повышением нервно-мышечной возбудимости и гипервентиляцией.
Наряду с классическими проявлениями ГВС, пароксизмальными и перманентными, имеются и другие расстройства, характерные для психовегетативного синдрома в целом:
- сердечно-сосудистые нарушения — боль в области сердца, сердцебиения, дискомфорт, сжатие в груди. Объективно отмечаются лабильность пульса и артериального давления, экстрасистолия, на ЭКГ — флюктуация сегмента ST; акроцианоз, дистальный гипергидроз, феномен Рейно;
- расстройства со стороны желудочно-кишечного тракта: усиление перестальтики кишечника, отрыжка воздухом, вздутие живота, тошнота, боли в животе;
- изменения сознания, проявляющиеся ощущением нереальности, липотимией, головокружением, неясностью зрения, в виде тумана или сетки перед глазами;
- алгические проявления, представленные цефалгиями или кардиалгиями.
Итак, для диагностики ГВС необходимо подтверждение следующих критериев:
- Наличие полиморфных жалоб: дыхательные, эмоциональные и мышечно-тонические нарушения, а также дополнительные симптомы.
- Отсутствие органических нервных и соматических заболеваний.
- Наличие психогенного анамнеза.
- Положительная гипервентиляционная проба.
- Исчезновение симптомов гипервентиляционного криза при дыхании в мешок или ингаляции смеси газов (5% СО2).
- Наличие симптомов тетании: симптом Хвостека, положительная проба Труссо, положительная проба ЭМГ на скрытую тетанию.
- Изменение pH крови в сторону алкалоза.
Лечение ГВС
Лечение ГВС носит комплексный характер и направлено на коррекцию психических нарушений, обучение правильному дыханию, устранение минерального дисбаланса.
Нелекарственные методы
- Больному объясняют сущность заболевания, убеждают, что оно излечимо (объясняют происхождение симптомов заболевания, особенно соматических, взаимосвязь их с психическим состоянием; убеждают, что нет органического заболевания).
- Рекомендуют бросить курить, меньше употреблять кофе и алкоголь.
- Назначают дыхательную гимнастику с регуляцией глубины и частоты дыхания. Для правильного ее проведения необходимо соблюсти несколько принципов. Во-первых, перейти на диафрагмальное брюшное дыхание, во время которого включается «тормозной» рефлекс Геринга–Брейера, обусловливающий снижение активности ретикулярной формации ствола мозга и в результате — мышечную и психическую релаксацию. Во-вторых, выдержать определенные соотношения между вдохом и выдохом: вдох в 2 раза короче выдоха. В-третьих, дыхание должно быть редким. И наконец, в-четвертых, дыхательная гимнастика должна проводиться на фоне психической релаксации и положительных эмоций. Вначале дыхательные упражнения продолжаются несколько минут, в последующем — довольно длительное время, формируя новый психофизиологический паттерн дыхания.
- При выраженных гипервентиляционных расстройствах рекомендуют дыхание в пакет.
- Показаны аутогенная тренировка и дыхательно-релаксационный тренинг.
- Высокоэффективным является психотерапевтическое лечение.
- Из инструментальных нелекарственных методов применяется биологическая обратная связь. Механизм обратной связи с объективизацией целого ряда параметров в реальном времени позволяет достигать более эффективной психической и мышечной релаксации, а также успешней, чем при аутогенной тренировке и дыхательно-релаксационном тренинге, регулировать паттерн дыхания. Метод биологической обратной связи в течение многих лет успешно применяется в Клинике головной боли и вегетативных расстройств им. акад. А. Вейна для лечения гипервентиляционных нарушений, панических атак, тревожных и тревожно-фобических нарушений, а также головной боли напряжения.
Лекарственные методы
Гипервентиляционный синдром относится к психовегетативным синдромам. Его основным этиологическим фактором являются тревожные, тревожно-депрессивные и фобические нарушения. Приоритет в его лечении имеет психотропная терапия. При терапии тревожных расстройств антидепрессанты превосходят по эффективности анксиолитические средства. Больным с тревожными расстройствами следует назначать антидепрессанты с выраженными седативными или анксиолитическими свойствами (амитриптилин, пароксетин, флувоксамин, миртазапин). Терапевтическая доза амитриптилина составляет 50–75 мг/сут, для уменьшения побочных эффектов: вялости, сонливости, сухости во рту и др. — следует очень медленно повышать дозу. Селективные ингибиторы обратного захвата серотонина имеют лучшую переносимость и менее выраженные нежелательные побочные действия. Терапевтическая доза флувоксамина — 50–100 мг/сут, пароксетина — 20–40 мг/сут. К их наиболее частым нежелательным побочным действиям относится тошнота. Для ее предотвращения или более успешного преодоления также рекомендуется назначать препарат в половинной дозировке в начале терапии и принимать его во время еды. Учитывая снотворное действие флувоксамина, препарат следует назначать в вечернее время; пароксетин имеет менее выраженные гипногенные свойства, поэтому его чаще рекомендуют принимать во время завтрака. Четырехциклический антидепрессант миртазапин обладает выраженным противотревожным и снотворным действием. Его назначают обычно перед сном, начиная с 7,5 или 15 мг, постепенно повышая дозу до 30–60 мг/сут. При назначении сбалансированных антидепрессантов (без выраженного седативного или активирующего действия): циталопрама (20–40 мг/сут), эсциталопрама (10–20 мг/сут), сертралина (50–100 мг/сут) и др., — возможно их сочетание в течение короткого периода 2–4 нед с анксиолитиками. Использование подобного «бензодиазепинового моста» в ряде случаев позволяет ускорить начало действия психотропной терапии (это является важным, если учитывать отсроченное на 2–3 нед действие антидепрессантов) и преодолеть усиление тревожных проявлений, временно возникающее у некоторых пациентов в начале терапии. При наличии у пациента гипервентиляционных кризов во время приступа наряду с дыханием в мешок следует принимать в качестве абортивной терапии анксиолитики: алпразолам, клоназепам, диазепам. Длительность психотропной терапии составляет 3–6 мес, при необходимости до 1 года.
Психотропные препараты наряду с положительным терапевтическим эффектом имеют и ряд отрицательных свойств: нежелательные побочные эффекты, аллергизация, развитие привыкания и зависимости, особенно к бензодиазепинам. В связи с этим целесообразно использование альтернативных средств, в частности средств, корригирующих минеральный дисбаланс, являющийся важнейшим симптомообразующим фактором при гипервентиляционных нарушениях.
В качестве средств, снижающих нервно-мышечную возбудимость, назначают препараты, регулирующие обмен кальция и магния. Наиболее часто применяют эргокальциферол (витамин Д2), Кальций–Д3, а также другие лекарственные средства, содержащие кальций, в течение 1–2 мес.
Общепринятым является воззрение на магний как ион с четкими нейроседативными и нейропротекторными свойствами. Дефицит магния в ряде случаев приводит к повышенной нервно-рефлекторной возбудимости, снижению внимания, памяти, судорожным приступам, нарушению сознания, сердечного ритма, расстройствам сна, тетании, парестезиям, атаксии. Стрессы — как физические, так и психические — увеличивают потребность магния в организме и служат причиной внутриклеточной магниевой недостаточности. Состояние стресса приводит к истощению запасов внутриклеточного магния и потере его с мочой, так как повышенное количество адреналина и норадреналина способствует выделению его из клеток. Магния сульфат в неврологической практике используется давно как гипотензивное и противосудорожное средство. Имеются исследования об эффективности магния в лечении последствий острого нарушения мозгового кровообращения [2] и черепно-мозговых травм [4], в качестве дополнительного средства при эпилепсии, лечении аутизма у детей [3, 7].
Препарат Магне В6 содержит лактат магния и пиридоксин, который дополнительно потенцирует абсорбцию магния в кишечнике и транспорт его внутрь клеток [6]. Реализация седативного, анальгетического и противосудорожного эффектов магнийсодержащих препаратов основана на свойстве магния тормозить процессы возбуждения в коре головного мозга [5]. Назначение препарата Магне В6 как в виде монотерапии по 2 таблетки 3 раза в сутки, так и в комплексной терапии в сочетании с психотропными средствами и нелекарственными методами лечения приводит к уменьшению клинических проявлений ГВС.
По вопросам литературы обращайтесь в редакцию.
Е. Г. Филатова, доктор медицинских наук, профессор
ММА им. И. М. Сеченова, Москва
Источник
Респираторный дистресс-синдром взрослых (РДСВ) – крайне тяжелое проявление дыхательной недостаточности, сопровождающееся развитием некардиогенного отека легких, нарушений внешнего дыхания и гипоксии. Несмотря на многообразие факторов, приводящих к РДВС, в его основе лежат повреждения легочных структур, вызывающие несостоятельность транспортировки кислорода в легкие. Другими названиями респираторного дистресс-синдрома являются «шоковое», «влажное», «травматическое» легкое.
Общие сведения
Респираторный дистресс-синдром взрослых (РДСВ) – крайне тяжелое проявление дыхательной недостаточности, сопровождающееся развитием некардиогенного отека легких, нарушений внешнего дыхания и гипоксии. Несмотря на многообразие факторов, приводящих к РДВС, в его основе лежат повреждения легочных структур, вызывающие несостоятельность транспортировки кислорода в легкие. Другими названиями респираторного дистресс-синдрома являются «шоковое», «влажное», «травматическое» легкое.
Резкое снижение оксигенации и вентиляции организма вызывает кислородную недостаточность сердца и головного мозга и развитие угрожающих для жизни состояний. При РДСВ летальность в случае несвоевременно или неадекватно оказанной помощи достигает 60-70%.

Респираторный дистресс-синдром
Причины и механизм развития РДСВ
Механизмом, запускающим развитие респираторного дистресс-синдрома, служит эмболизация мелких сосудов легких микросгустками крови, частичками поврежденных тканей, каплями жира на фоне образующихся в тканях токсичных биологически активных веществ — кининов, простагландинов и др. Микроэмболизация легочных сосудов развивается в результате прямого или опосредованного воздействия на капиллярно-альвеолярную мембрану легочных ацинусов различного рода повреждающих факторов.
Прямое повреждающее воздействие оказывает аспирация крови, рвотных масс и воды, вдыхание дыма и токсических веществ, контузия легких, перелом ребер, разрыв диафрагмы, передозировка наркотических средств. Опосредованное, непрямое повреждение капиллярно-альвеолярных мембран вызывает активация и агрегация форменных элементов крови при бактериальных и вирусных пневмониях, сепсисе, ожогах, сочетанных травмах и травматическом шоке, сопровождающихся массивной кровопотерей, панкреатите, аутоиммунных процессах, электротравме, эклампсии и т. д.
Повышение проницаемости мембраны для белка и жидкости вызывает отек интерстициальной и альвеолярной тканей, снижение растяжимости и газообменной функции легких. Эти процессы приводят к развитию гипоксемии, гиперкапнии и острой дыхательной недостаточности. Респираторный дистресс-синдром может развиваться на протяжении нескольких часов или суток от момента воздействия повреждающего фактора. В течении РДСВ выделяют три патоморфологические фазы:
- Острая фаза РДСВ (до 2-5 суток) – интерстициальный и альвеолярный отек легких, поражение капилляров легких и эпителия альвеол, развитие микроателектазов. В случае благоприятного течения респираторного дистресс-синдрома спустя несколько дней острота явлений стихает, транссудат рассасывается; в противном случае возможен переход в подострое либо хроническое течение.
- Подострая фаза РДСВ – развитие бронхоальвеолярного и интерстициального воспаления.
- Хроническая фаза РДСВ – соответствует развитию фиброзирующего альвеолита. Происходит утолщение и уплощение капиллярно-альвеолярных мембран, разрастание в них соединительной ткани, формирование микротромбозов и запустевание сосудистого русла. Исходом хронической фазы респираторного дистресс-синдрома служит развитие легочной гипертензии и хронической дыхательной недостаточности. Выраженный альвеолярный фиброз может возникнуть уже спустя 2-3 недели.
Симптомы респираторного дистресс-синдрома
Развитие респираторного дистресс-синдрома взрослых характеризуется последовательной сменой стадий, отражающих патологические изменения в легких и типичную картину остро нарастающей дыхательной недостаточности.
I (стадия повреждения) – первые 6 часов со времени воздействия стрессового фактора. Жалобы, как правило, отсутствуют, клинико-рентгенологические изменения не определяются.
II (стадия мнимого благополучия) – от 6 до 12 часов со времени воздействия стрессового фактора. Развиваются нарастающая одышка, цианоз, тахикардия, тахипноэ (учащение дыхания более 20 в мин.), беспокойство пациента, кашель с пенистой мокротой и прожилками крови. Одышка и цианоз не купируются кислородными ингаляциями, содержание кислорода в крови неуклонно падает. Аускультативно в легких – хрипы, крепитация; рентгенологические признаки соответствуют диффузному интерстициальному отеку.
III (стадия дыхательной недостаточности) – спустя 12-24 часа после воздействия стрессового фактора. Клокочущее дыхание с выделением пенистой розовой мокроты, нарастающая гипоксемия и гиперкапния, поверхностное дыхание, увеличение центрального венозного и снижение артериального давления. По всей поверхности легких выслушиваются влажные, множественные хрипы различного калибра. На рентгенограммах определяется слияние очаговых теней. В этой стадии происходит образование гиалиновых мембран, заполнение альвеол фибрином, экссудатом, распадающимися кровяными тельцами, поражение эндотелия капилляров с образованием кровоизлияний и микроателектазов.
IV (терминальная стадия) – метаболический ацидоз, гипоксемия и гиперкапния не устраняются предельно большими объемами интенсивной терапии и ИВЛ. Ложноположительная рентгенологическая динамика (появление очагов просветлений) вызвана разрастанием соединительной ткани, замещающей паренхиму легких. В этом терминальном периоде респираторного дистресс-синдрома развивается полиорганная недостаточность, характеризующаяся:
- артериальной гипотонией, выраженной тахикардией, фибрилляцией предсердий, желудочковой тахикардией;
- гипербилирубинемией, гиперферментемией, гипоальбуминемией, гипохолестеринемией;
- ДВС-синдромом, лейкопенией, тромбоцитопенией ;
- повышением мочевины и креатинина, олигурией;
- желудочно-кишечными и легочными кровотечениями;
- угнетением сознания, комой.
Осложнения
Диагностика респираторного дистресс-синдрома
Респираторный дистресс-синдром является критическим состоянием и требует экстренной оценки состояния пациента. Ранними объективными проявлениями РДСВ служат нарастающие одышка, тахикардия и цианоз. Аускультативная картина легких изменяется соответственно стадиям респираторного дистресс-синдрома: от жесткого «амфорического» дыхания к клокочущим влажным хрипам и симптому «немого» («молчащего») легкого в терминальной стадии.
Характерным показателем газового состава крови при РДСВ является РаО2 ниже 50 мм рт. ст. (гипоксемия), несмотря на проводимую оксигенотерапию (при FiО2 более >60%.), нарастание гиперкапнии. У пациентов с РДСВ выраженная дыхательная недостаточность и гипоксемия сохраняются даже при ингаляциях высококонцентрированной кислородной смеси.
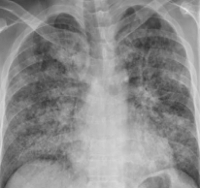
Биохимические показатели венозной крови характеризуются гипоальбуминемией, повышением свертывающих факторов, нарастанием трансаминаз и билирубина. При рентгенографии легких на периферии выявляются диффузные множественные тени (симптом “снежной бури”), снижение прозрачности легочной ткани, плевральный выпот обычно отсутствует.
Показатели функции внешнего дыхания свидетельствуют об уменьшении всех дыхательных объемов и статического растяжения легочной ткани менее 5 мл/мм вод. ст. Измерение давления в легочной артерии катетером Суона–Ганца показывает его «заклинивание» на уровне менее 15 мм рт.ст. Респираторный дистресс-синдром следует отличать от кардиогенного отека легких, пневмонии, ТЭЛА.
Лечение респираторного дистресс-синдрома
Лечение респираторного дистресс-синдрома осуществляется в условиях отделения интенсивной терапии и реанимации. Мероприятия по купированию РДСВ включают:
- устранение стрессового повреждающего фактора;
- коррекцию гипоксемии и острой дыхательной недостаточности;
- лечение полиорганных нарушений.
На первом этапе лечения респираторного дистресс-синдрома устраняются прямые повреждающие факторы легких, назначается массивная антибактериальная терапия при бактериальных пневмониях, сепсисе, осуществляется соответствующее лечение ожогов и травм. Для устранения гипоксии проводится подбор адекватного режима кислородотерапии с динамическим контролем газов крови (с поддержанием РО2 не менее 60 мм рт.ст.). Подача кислорода может осуществляться чрез маску или носовой катетер, при неэффективной оксигенации показана ИВЛ (при ЧД 30 в минуту).
Для профилактики развития ДВС-синдрома назначаются ацетилсалициловая кислота, дипиридамол и реополиглюкин, гепарин. Несмотря на интерстициальный и альвеолярный отек, проводится инфузионная терапия для улучшения питания органов, нормализации диуреза и поддержания уровня АД. Эффективность лечения респираторного дистресс-синдрома зависит от его своевременности: оно успешно лишь на ранних стадиях данного состояния до наступления необратимых поражений легочной ткани.
Прогноз и профилактика респираторного дистресс-синдрома
Летальность в III стадии респираторного дистресс-синдрома составляет около 80%, в терминальной стадии, соответствующей полиорганной недостаточности, обычно все пациенты погибают. При благоприятном исходе после купирования РДСВ функция легких может практически полностью восстановиться, однако чаще требуется длительная поддерживающая терапия.
Специфические профилактические мероприятия респираторного дистресс-синдрома отсутствуют. Следует остерегаться воздействия стрессовых повреждающих факторов, ведущих к развитию РДСВ.
Источник
