Роль глюкокортикоидов в адаптационном синдроме
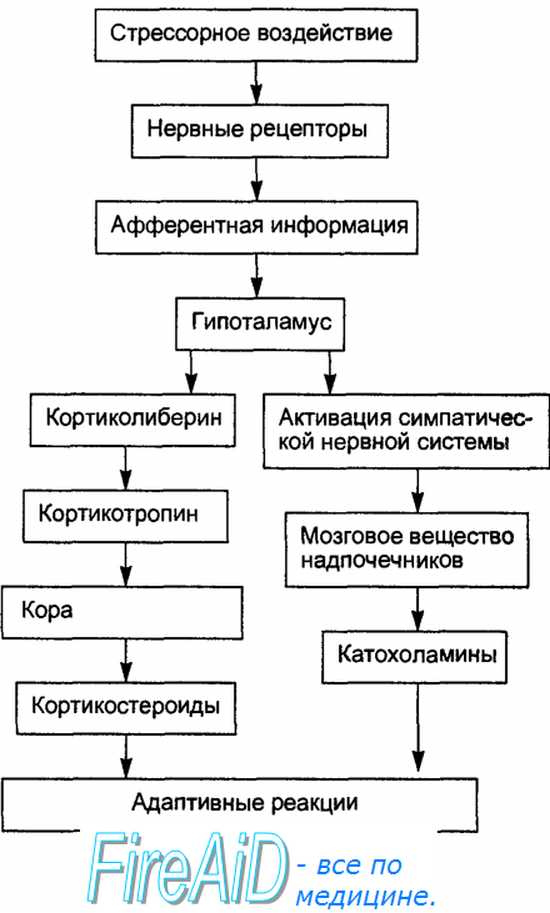
Оглавление темы “Гормоны почек. Гормоны сердца. Гормоны сосудов. Гормоны при стрессе. Выделение гормонов при повреждении тканей.”: Стресс. Гормоны при стрессе. Общий адаптационный синдром. Гормональное обеспечение общего адаптационного синдрома, или стресса.Примером неспецифического участия эндокринной системы в приспособительных реакциях организма являются изменения ее деятельности при стрессе. Состояние стресса возникает как следствие действия на организм любых сильных, в том числе экстремальных и повреждающих, раздражителей. При действии на организм экстремальных факторов неспецифические реакции стресса прежде всего направлены на стимуляцию энергетического обеспечения приспособительных процессов. Ведущую роль в этих неспецифических реакциях играют катехоламины и глюкокортикоиды, в значительных количествах мобилизуемые в кровь (рис. 6.30). Активируя катабо-лические процессы, эти гормоны ведут к гипергликемии — одной из начальных реакций субстратного энергообеспечения. Как следствие гипергликемии на некоторое время повышается в крови уровень инсулина. Метаболические перестройки при таком гипергормональном профиле связаны, прежде всего, с активацией в печени фосфорилазы и гликогенолизом, а поступающая в кровь глюкоза под влиянием инсулина интенсивно утилизируется тканями, прежде всего скелетными мышцами, что увеличивает их работоспособность и повышает теплообразование в организме. Жиромобили-зующий эффект глюкокор-тикоидов и катехоламинов способствует повышению в крови второго важнейшего энергетического субстрата — свободных жирных кислот. Однако подобный «форсированный» режим функционирования эндокринной системы из-за ограниченности функциональных резервов не может длиться долго, вскоре содержание инсулина в крови уменьшается, что носит название «функциональный транзиторный диабет». Это необходимое условие для усиления жиромобилизующего эффекта глюкокортикоидов и активации глюконеогенеза. Важнейшим источником глюкозы как энергетического материала в этот период становится глюко-неогенез, но на образование глюкозы расходуется дефицитный пластический материал — аминокислоты. Необходимым условием длительно повышенного энергоснабжения является переключение энергетического обмена с углеводного типа на липидный, тем более что углеводные резервы в виде гликогена достаточно быстро оказываются практически исчерпанными. Постепенно снижается продукция глюкокортикоидов, устанавливается новое гормональное соотношение: нерезко повышенный уровень глюкокортикоидов при более значительном снижении уровня инсулина. Этот новый уровень функционирования эндокринной системы способствует восстановлению равновесия между катаболическими и анаболическими процессами, расходы белка на энергетические нужды снижаются. Жиромобилизующий эффект гормональной перестройки и образование транспортной формы эндогенного жира — липопротеинов очень низкой плотности — приводят к тому, что растет использование клетками липидов как источников энергии. Жирные кислоты интенсивно окисляются в скелетных мышцах, миокарде и печени. Образующиеся при этом кетоновые тела усиленно окисляются в мышечной ткани, почках, а также сердце и мозге. Особенно резко ограничивается потребление углеводов мышечной и жировой тканью, что экономит глюкозу для углеводзависимых тканей — головного мозга, кроветворной ткани и эритроцитов, в некоторой степени — миокарда. Таким образом, происходящие при стрессе гормональные и метаболические перестройки обеспечивают длительное неспецифическое повышение энергообеспечения приспособительных процессов.
Стресс как неспецифическая реакция приспособления и компенсации нарушенных функций может при резкой выраженности сопровождаться и активацией гипоталамо-гипофизарно-тиреоидной системы, приводя к росту в крови уровня тиреоидных гормонов. Физиологический стресс, например эмоциональное напряжение, напротив, характеризуется снижением гормональной активности щитовидной железы. Гиперфункция щитовидной железы в ответ на повреждение тканей является неспецифической реакцией компенсации, поскольку тиреоидные гормоны, благодаря стимуляции синтеза белков, способствуют клеточным регенеративным процессам и репарации поврежденных структур. Активация гипоталамо-гипофизарно-тиреоидной системы может носить и черты специфической компенсации, например в условиях холодового стресса, как компенсация термического угнетения метаболизма. Стресс при экстремальных состояниях сопровождается активацией и других гормональных систем — гипоталамо-гипофизарно-андрогенной и гипоталамо-нейрогипофизарной. Повышение активности системы гонадолиберины—гонадотропины—андрогены (одним из проявлений является повышение либидо) и избыточно секретируемые при этом андрогены за счет анаболического эффекта способствуют репаратив-ным процессам. При хирургическом и эмоциональном стрессе повышается секреция вазопрессина. Компенсаторное значение активации секреции вазопрессина заключается в облегчении консолидации процессов памяти, формирования аналгезии, потенцировании эффектов кортиколиберина на секрецию кор-тикотропина, восстановлении нарушенной при кровопотере гемодинамики. Избыточная секреция вазопрессина при травмах является примером опережающей перестройки эндокринных механизмов компенсации, реализующей избыточный гормональный сигнал для предотвращения возможности потери организмом воды при кровотечении. Реакция гипоталамо-нейрогипофизарной системы может быть и специфической компенсацией возникших в организме нарушений водно-солевого и осмотического гомеостазиса (осмотический стресс). – Также рекомендуем “Выделение гормонов при повреждении тканей. Регенерация. Репарации. Гормональная регуляция местных компенсаторных реакций.” |
Источник
Медицинский эксперт статьи
х
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
В научной литературе адаптационный синдром характеризуется как комплекс изменений, которые несвойственны для человека, но проявляются при воздействии на организм различного рода сильных раздражителей или факторов, которые причиняют ему вред.
[1], [2], [3]
Код по МКБ-10
F43 Реакция на тяжелый стресс и нарушения адаптации
Эффекты глюкокортикоидов при общем адаптационном синдроме
Глюкокортикоиды – гормоны, что выделяются в процессе активной работы коры надпочечников. Их роль крайне важна в функционирования организма во время адаптационного синдрома. Они исполняют защитную функцию, которая проявляется в понижении степени проницаемости сосудов, что предотвращает уменьшение уровня АД при негативных раздражителях. Снижая проницаемость мембран клеток и лизосом, глюкокортикоиды препятствуют их повреждению во время травм и при отравлениях. Также благодаря ним повышается уровень энергетического ресурса организма, поскольку эти гормоны принимают активное участие в регуляции углеводго обмена.
Снижая степень проницаемости клеток и сосудов, глюкокортикоиды устраняют воспалительные процессы. Еще одна их особенность в том, что они повышают тонус нервной системы, снабжая нервные клетки глюкозой. Активируя в печени выработку альбуминов, что отвечают за создание нужного уровня давления крови в сосудах , в стрессовых ситуациях глюкокортикоиды предотвращают снижения объема циркулирующей крови и падению артериального давления.
Но не всегда глюкокортикоиды полезны, они имеют и повреждающее действие. Они приводят к разрушению лимфоидной ткани, что провоцирует развитие лимфопении. Это сказывается на выработке антител. Поэтому случается, что физически здоровые люди начинают чаще болеть.
Чтобы не столкнуться с таким неприятным состоянием как адаптационный синдром необходимо проводить профилактику стресса, а именно заниматься спортом, закаливать организм, посещать аутотренинги, откорректировать рацион питания, уделить внимание любимому занятию. Данные методы помогут корригировать ответную реакцию организма на психические раздражители, травмы, инфекции. Процесс лечения зависит от стадии синдрома. На первом этапе применяются гидроэлектрические растворы. На втором – назначают соли калия и гидрокортизон. На стадии истощения потребуется восстановление процесса кровообращения, поэтому используют сердечнососудистые аналептики.
[4], [5]
Стресс и адаптационный синдром
Адаптационный синдром является реакцией организма на стресс. Специалистами были установлены факторы, которые предрасполагают к развитию данной патологии:
- индивидуальные особенности человека: тревожность, низкая степень стресоустойчивости, нигилизм, безынициативность, социальная отчужденность,
- механизмы защиты и противостояния стресогенным факторам,
- социальная поддержка либо ее отсутствие,
- предварительный прогноз индивидом события, которое может оказать стрессовое воздействие.
Причиной появления адаптационного синдрома может стать травма, перепад температуры, физические нагрузки, инфекция и прочее. Среди главных признаков адаптационного синдрома выделяют: кровотечения в органах пищеварения, усиленная работа и увеличение размеров коркового слоя надпочечников, с повышенным выделением гормональных веществ, инволюция вилочковой железы и селезенки, снижения выработка клеток крови. Диагностировать адаптационное расстройство можно и по таким критериям:
- появление реакции на стресс в течение 3-х месяцев, с момента его проявления;
- оно не является реакцией на необычный стрессогенный фактор, и выходит за рамки нормального поведения;
- очевидны нарушения в профессиональной и социальной сферах.
Избежать появления адаптационного синдрома можно естественным путем. Даже специалисты назначают медикаментозное лечение как последнюю меру. Необходимо выработать механизм психологической защиты, основная функция которого заключается в выработке сознательных психологических барьеров от негативных эмоций и факторов, что травмируют психику.
Общий адаптационный синдром Селье
Известный физиолог, патолог и эндокринолог Ганс Селье выдвинул теорию, что у людей проявляются неспецифические физиологические реакции организма на стресс. Совокупности этих реакций он дал название – «общий адаптационный синдром». Ученый определил, что данное проявление представляет собою усиленное приспособление организма к изменениям в условиях среды обитания, за счет включения специальных механизмов защиты.
Селье отмечал, что ни один организм не может постоянно пребывать в тревожном состоянии. Если стресс оказывает сильное воздействие, то пациента ожидает смертельный исход еще на начальной стадии. На втором этапе израсходуются адаптационные резервы. Если же стрессор не прекращает своего действия, то это приводит к истощению. Селье утверждал, что при запущенности общего адаптационного синдрома, может наступить смерть.
Стадии адаптационного синдрома
В адаптационном синдроме было выделено три фазы:
- 1 – стадия тревоги. Она может длиться от шести часов и до двух суток. В это время повышается степень выработки и поступление в кровоток глюкокортикоидов и адреналина. Организм пациента начинает подстраиваться к сложившейся ситуации. Стадия тревоги имеет две фазы: шока и противошока. Во время первой повышается степень угрозы функциональным системам организма, вследствие чего появляется гипоксия, снижается АД, повышается температура, понижается уровень глюкозы в крови. В фазе противошока наблюдается активная работа надпочечников и выброс кортикостероидов.
- 2 – стадия резистентности. Возрастает устойчивость пациента к разного рода воздействиям. Ближе к ее завершению, общее состояние человека заметно улучшается, работы систем приходит в норму и наступает выздоровление. Если сила раздражителя значительно превышает возможности организма, тогда о положительном результате нельзя говорить.
- 3 – стадия истощения. Здесь есть большая вероятность летального исхода, поскольку ослабевает функциональная активность коры надпочечников. Происходит сбой в работе других систем.
Источник
1. Определение общего адаптационного синдрома Общий адаптационный синдром – совокупность неспецифических защитных приспособительных реакций, возникающих на фоне действия стрессорных раздражителей, характеризуется фазными изменениями гормонального баланса, соответствующими метаболическими и функциональными сдвигами, направленными на адаптацию организма к действию раздражителя.
Стрессорные раздражители вызывают напряжение функциональных систем, направленных на поддержание гомеостаза.
Стрессорные раздражители подразделяются на:
– эмоциогенные факторы внешней среды (положительные и отрицательные);
– физические раздражители (чрезмерная физическая нагрузка или ее отсутствие – иммобилизационный стресс);
– биологические раздражители (вирусы, бактерии).
2. Характер действия стресса По характеру действия:
– чрезвычайно сильные раздражители для данного организма;
– несильные, но необычные для организма средний и малой силы воздействия.
Основоположником учения об общем адаптационном синдроме является канадский ученый Ганс Селье (1907-1982 гг.). Впервые основы концепции стресса были заложены в 1936 г. В статье “Синдром ответа и повреждения”. Несмотря на характер стрессорного воздействия организм всегда отвечает классической триадой: атрофией тимуса и лимфоидной ткани, гипертрофией, гиперплазий коры надпочечников (пучковой зоны), множественными кровоизлияниями и изъязвлениями в слизистой желудочно-кишечного тракта. В развитии реакций адаптации на повреждения важная роль отводится соматотропному гормону и глюкокортикоидам.
3. Стадии общего адаптационного синдрома В соответствии с динамикой уровня глюкокортикоидов в ткани Г. Сенье выделяют 3 стадии общего адаптационного синдрома:
1 стадия – стадия тревоги возникает в момент действия стресса;
2 стадия – стадия резистентности;
3 стадия – стадия истощения.
Реакция тревоги означает немедленную иммобилизацию защитных сил организма.
Она состоит из фазы шока и противошока. Фаза шока возникает при резком усилении секреции глюкокортикоидов, но в тканях уровень их падает из-за усиленного метаболизма. В эту фазу возникает относительная недостаточность глюкокортикоидов. В фазе шока наблюдается недостаточность кровообращения в периферических органах и тканях, мышечная и артериальная гипотензия, гипотермия, гипогликемия, сгущение крови, эозинопения. Если человек адаптируется, не погибает, то возникает гипертрофия, гиперплазия пучковой зоны коры надпочечников, уровень глюкокортикоидов в крови и тканях повышается, начинаются изменения в обратном направлении (стадия противошока), активируются анаболические процессы, ведущие к развитию следующей стадии – стадии резистентности. Высокий уровень глюкокортикоидов обеспечивает высокую резистентность организма к действию патогенного фактора. Это неспецифическая резистентность.
Человек устойчив к действию различных патогенных факторов. Если стрессорный раздражитель действует однократно, повышается резистентность, он прекращает действовать, то может произойти нормализация гормонального баланса. При длительном действии повреждающего агента (реинфекции, повторные эмоциональные и физические нагрузки), адаптация нарушается и наступает 3 стадия – стадия истощения, когда наступает необратимая атрофия пучковой зоны коры надпочечников, снижается концентрация глюкокортикоидов, снижается артериальное давление, идет распад белков, снижается устойчивость организма к действию различных патогенных факторов. В эту стадию преобладает минералокортикоидный фон, что способствует плазматизации лимфоидной ткани.
Биологическое значение адаптационного синдрома заключается не только в том, что во второй его стадии повышается резистентность организма по отношению к фактору, вызвавшему состояние стресса, но и в том, что при не очень сильном и длительном стрессе может создаваться или повышаться неспецифическая резистентность организма к различным другим факторам.
4. Реакция эндокринной системы Систематическое воздействие на организм слабых и умеренных раздражителей (например, холодный душ, физические упражнения) поддерживает готовность эндокринной системы к адаптивным реакциям. Механизмы развития гормональных сдвигов при действии стрессорных раздражителей: возникает поток афферентной импульсации по соответствующим чувствительным путям в таламус, в лимбическую систему, в корковые структуры (чувствительные и двигательные зоны). Эта специфическая импульсация отражает характер действия раздражителя, приводит к специфической реакции организма (поведенческие реакции, рефлекторные). Возникает еще и неспецифическая реакция в ретикулярную формацию ствола мозга, что приводит к увеличению активирующих влияний на различные структуры мозга, а также на область гипоталамуса. Активация переднего гипоталамуса повышает активность супраоптического ядра, что приводит к секреции вазопрессина. Усиленное влияние на средний гипоталамус приводит к секреции кортиколиберина. Это гормон пептидной природы, который по системе воротного кровоснабжения достигает базальных клеток гипофиза и стимулирует выработку адренокортикотропного гормона, который стимулирует продукцию глюкокортикоидов.
Антидиуретический гормон также стимулирует секрецию АКТГ и глюкокортикоидов. Влияние на задний гипоталамус: возникает активация симпатоадреналовой системы. Из мозгового вещества надпочечников выбрасывается норадреналин, адреналин. Норадреналин вызывает спазм сосудов многих внутренних органов, спазм приносящих сосудов почек, и возникает ишемия почек. Ренин вызывает усиленную продукцию ангиотензина II и минералкортикоидов.
Усиленная продукция норадреналина приводит к активации паращитовидных желез, вырабатывающих паратгормон, что приводит к мобилизации кальция из костной системы. Возбудимость нейронов гипоталамо-гипофизарной системы возрастает, что приводит к выбросу АКТГ, глюкокортикоидов, катехоламинов.
Избыточная продукция норадреналина стимулируется выброс глюкагона и подавляет выработку инсулина.
Источник
