Синдром беста что это такое
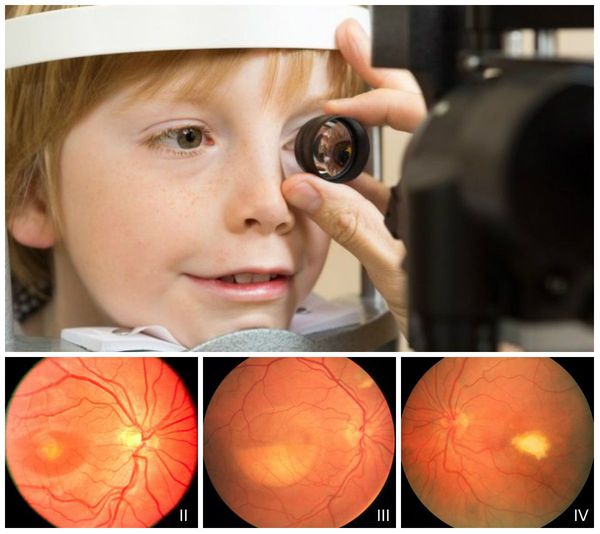
Болезнь Беста – одна из форм двухсторонней центральной (макулярной) пигментной абиотрофии сетчатки, приводящая к дистрофии фоторецепторов желтого пятна и значительному ухудшению зрения. Характеризуется первоначально бессимптомным течением, со временем падает острота зрения, возникает центральная скотома. Диагностика производится на основании осмотра глазного дна, данных электроокулографии и флюоресцентной ангиографии сосудов сетчатки, генетических исследований. Специфического лечения болезни Беста не существует, используется поддерживающее лечение для замедления прогрессирования проявлений патологии.
Общие сведения
Болезнь Беста (центральная пигментная абиотрофия, вителлиформная дистрофия Беста) – генетическое заболевание, характеризующееся развитием кистозных дистрофических изменений в области желтого пятна. Впервые описано в 1905 году Ф. Бестом, который изучил идентичные нарушения зрения у восьми родственников и высказал предположение о наследственной природе патологии. Болезнь Беста с одинаковой частотой поражает как мужчин, так и женщин, встречаемость составляет примерно 3-4:100000. В отличие многих других форм абиотрофии сетчатки болезнь Беста редко приводит к полной слепоте, кроме того, характеризуется длительным многостадийным течением. На первоначальных этапах патологии нарушения зрения не развиваются, и нет практически никаких симптомов, изменения на сетчатке нередко бывают случайной находкой при медицинском осмотре у врача-офтальмолога. Своевременно назначенная поддерживающая терапия может значительно замедлить развитие болезни Беста.
Болезнь Беста
Причины болезни Беста
Причиной дистрофии сетчатки, которая имеет место при болезни Беста, является мутация гена BEST1, локализованного на 11-й хромосоме. Он кодирует белок бестрофин, относящийся к классу анионных каналов пигментного эпителия сетчатой оболочки глаза. Патогенез нарушений при болезни Беста досконально не изучен – выяснено, что при этой патологии происходит медленное разрушение пигментного эпителия в области желтого пятна, и изменяются свойства мембраны Бруха. В результате этого происходит прорастание капилляров в субретинальное пространство, в сетчатке накапливаются гранулы вещества, по своим биохимическим свойствам схожего с липофусцином. Макроскопически при болезни Беста в области желтого пятна медленно нарастают пигментные нарушения, затем возникает киста, которая перекрывает поступление света к большей части фоторецепторов макулярной области. Затем происходит разрыв кисты, ее содержимое резорбируется, на ее месте формируется рубец, который и является причиной стойких нарушений зрения.
Механизм наследования мутаций гена BEST1 – аутосомно-доминантный с достаточно высокой пенетрантностью. Помимо болезни Беста, нарушения структуры этого гена могут быть причиной некоторых других форм пигментной дегенерации сетчатки, бестрофинопатии, вителлиформной дистрофии взрослых. Последняя по своему течению очень похожа на болезнь Беста, но в отличие от нее развивается не в детском, а взрослом возрасте. Это позволяет предположить, что вителлиформная дистрофия взрослых является разновидностью синдрома Беста – современная генетика пока не обнаружила иных мутаций, которые приводили бы именно к этому состоянию.
Симптомы болезни Беста
Первые изменения на глазном дне при болезни Беста возникают в возрасте 2-5 лет, однако субъективных симптомов при этом не наблюдается. Поэтому заболевание диагностируется либо по итогам случайного медицинского обследования, либо в более позднем возрасте, после развития первых нарушений зрения. В целом болезнь Беста характеризуется определенной стадийностью.
Нулевая стадия болезни Беста диагностируется очень редко, так как при ней нет даже незначительных изменений в области желтого пятна. Наблюдается только снижение фовеального рефлекса и изменения электроокулографии. При изучении последней выявляется снижение коэффициента Ардена. Иногда такие проявления регистрируются у взрослых без дальнейшего развития клинической картины болезни Беста – это считается признаком носительства мутации гена BEST1.
В течение первой стадии субъективные симптомы все также не выражены, лишь в некоторых случаях наблюдается незначительное снижение остроты зрения. На глазном дне выявляются несколько желтоватых точек в макулярной области сетчатки. Во время второй стадии точки разрастаются до размеров, сопоставимых с диаметром диска зрительного нерва, и внешне схожи с яичным желтком. Нарушения остроты зрения на этой стадии болезни Беста не соответствуют офтальмологической картине и незначительны – она сохраняется на уровне 0,6-0,9. На третьей стадии болезни Беста происходит разрыв вителлиформных кист, что приводит к резкому снижению остроты зрения. Также распространенными жалобами на этой стадии являются затуманивание зрения, трудности с чтением мелкого текста. Четвертая стадия характеризуется резорбцией продуктов разрыва кист и формированием на их месте рубца. Острота зрения у разных пациентов на этом этапе составляет от 0,02 до 0,7, кроме того, возникает относительная центральная скотома и псевдогипопион. Границы поля зрения, как правило, не изменяются, сохраняется нормальное восприятие цветов.
Длительность каждой стадии у разных больных может колебаться в широких пределах. Кроме того, в некоторых случаях болезнь Беста может развиваться более быстро, поэтому некоторые стадии не диагностируются. Изменения на глазном дне обоих глаз чаще всего имеют асимметричный характер. Как правило, полной слепоты не наступает, одним из осложнений болезни Беста может быть формирование субретинальной неоваскулярной мембраны, значительно снижающей остроту зрения. Кроме того, с возрастом на месте рубцов после вителлиформных кист возможно развитие хориодального склероза.
Диагностика болезни Беста
Диагностика болезни Беста производится при помощи методов современной офтальмологии – осмотра глазного дна, электроокулографии, флюоресцентной ангиографии сосудов сетчатки. При осмотре в зависимости от стадии заболевания выявляются либо желтые точки, либо сформировавшиеся вителлиформные кисты, сконцентрированные в центре. После их разрыва (третья стадия болезни Беста) картина глазного дна напоминает «яичницу-болтушку». Кроме того, на любом этапе заболевания могут возникать ретинальные кровоизлияния, также заметные при осмотре. На последней стадии болезни Беста формируется псевдогипопион, заметны пигментные отложения в области желтого пятна.
Одним из самых первых проявлений заболевания является аномальная картина электроокулографии, которая регистрируется еще до появления первых изменений на глазном дне. Патогномоничный признак болезни Беста – снижение коэффициента Ардена или отношения светового пика к световому спаду, который на конечных этапах развития патологии не превышает 1,5. При флюоресцентной ангиографии на первых стадиях болезни (до образования вителлиформных кист) наблюдаются участки локальной гиперфлюоресценции, соответствующие местам атрофии пигментного эпителия. После образования кист (вторая стадия болезни Беста) в местах их локализации обнаруживают полное отсутствие флюоресценции, а при их разрыве (третья стадия) – гиперфлюоресценцию в верхних частях кист и ее отсутствие в нижних.
Врачом-генетиком может быть произведена и генетическая диагностика болезни Беста, которая сводится к секвенированию последовательности гена BEST1 с целью поиска мутаций. Это исследование относится к достаточно сложным, так как в этой области 11-й хромосомы расположено огромное количество генов, мутации многих из них также способны приводить к наследственным офтальмологическим заболеваниям. Дифференциальную диагностику болезни Беста проводят с синдромом Коатса и отслойкой пигментного эпителия. В отличие от них центральная пигментная абиотрофия всегда имеет двухсторонний характер и характеризуется аномальной электроокулографией.
Лечение и прогноз болезни Беста
Специфического лечения болезни Беста не существует, в связи с чем используют поддерживающую терапию, способную значительно замедлить прогрессирование патологии. К ней относят назначение витаминов А и Е, сосудорасширяющих и улучшающих трофику сетчатки средств – мельдоний, метилэтилпиридинол, этилметилгидроксипиридина сукцинат. Это тормозит развитие и последующий разрыв вителлиформных кист, позволяя сохранять удовлетворительную остроту зрения длительное время. В тех случаях, когда болезнь Беста осложнилась образованием субретинальной неоваскулярной мембраны, показана лазерная коррекция.
Прогноз болезни Беста, как правило, условно благоприятный. Полная потеря зрения наступает в очень редких случаях, обычно все ограничивается снижением остроты зрения и относительной центральной скотомой. Периферическое и сумеречное зрение не страдает, больные в дальнейшем только затрудняются при работе с небольшим шрифтом и мелкими деталями. При вителлиформной дистрофии взрослых нарушения зрения выражены еще слабее, в ряде случаев больные совсем не имеют жалоб, а наличие болезни определяется только офтальмологическими и генетическими исследованиями.
Источник
Болезнь Беста — это генетическое заболевание глаз, которое вызывает изменения в центральной области сетчатки, так называемой макуле. Первоначально оно протекает бессимптомно, но постепенно приводит к ухудшению остроты зрения и появлению слепого участка в центре поля зрения.
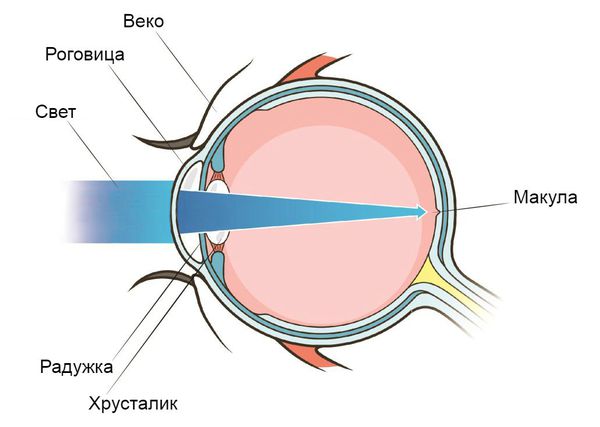
Возникновение и развитие болезни связано с дефектами в наследственном аппарате — мутациями гена VMD2 [3]. Область, в которой локализуется ген VMD2, известна врачам как область скопления генов, отвечающих за развитие большой группы гетерогенных генетических заболеваний с поражением глаз в комплексе с умственной отсталостью, ожирением, тугоухостью и другими патологиями органов и систем [11].
Болезнь Беста наследуется по аутосомно-доминантному пути, т. е. вероятность возникновения заболевания не зависит от пола и тяжести течения болезни у родителей.
У данного заболевания высокая пенетрантность, т. е. болезнь развивается у большинства людей с патологическим геном. Несмотря на это, выраженность клинических проявлений у родственников варьирует от минимальных изменений и сохранения 100 % зрения до выраженного снижения остроты зрения (вплоть до 0,02) и инвалидизации. Проследить семейную отягощённость удаётся не всегда, даже при комплексном обследовании [2].
Заболевание считается редким. Его распространённость составляет около 1 случая на 10000 населения [1]. Впервые упоминание о нём в литературе появилось в 1905 году: офтальмолог Ф. Бест описал его как двустороннюю макулодистрофию, которую он наблюдал у восьми членов одной семьи.
Факторов, способствующих манифестации заболевания при наличии наследственной предрасположенности, не выявлено.
На начальных стадиях заболевание никак не проявляется, поэтому обычно оно диагностируется случайно при медицинском осмотре. Симптомы появляются только на более поздних стадиях патологии.
Манифестирует болезнь в возрасте 5-15 лет. Ребёнок жалуется на прогрессирующее, обязательно двустороннее снижение чёткости зрения: он начинает испытывать затруднение при чтении мелкого шрифта вблизи. Также его беспокоят “вспышки”, “мерцание огоньков” и ухудшение цветовосприятия (в основном наблюдается цветослабость на жёлто-зелёный, зелёный, сине-зелёный цвета).
Изменения в большинстве случаев несимметричные, но возникают на обоих глазах. Острота зрения в зависимости от стадии болезни значительно колеблется: от 0,01 до 1,0.
Важно отличать болезнь Беста от вителлиформной макулодистрофии взрослых. Это заболевание также является генетическим, но возникает и прогрессирует оно в зрелом возрасте (около 40-50 лет). Для него характерно двустороннее, как правило, симметричное субретинальное поражение в центральной области сетчатки. Изменения так же, как при болезни Беста, имеют локальную, очерченную, круглую форму, желтоватый оттенок, но их размер всегда значительно меньше и они не прогрессируют [10].
Патофизиологический механизм болезни Беста на данный момент неизвестен. Предполагается, что при данной патологии происходит аномальное накопление вещества, подобного липофусцину — жёлто-коричневому пигменту гликопротеиновой природы, который встречается во всех тканях и органах человека. Это вещество скапливается между пигментным эпителием сетчатки и слоем светочувствительных клеток — фоторецепторов. В результате нарушается мембрана Бруха (самый внутренний слой сосудистой оболочки глаза) и разрушаются нервные элементы сетчатки.
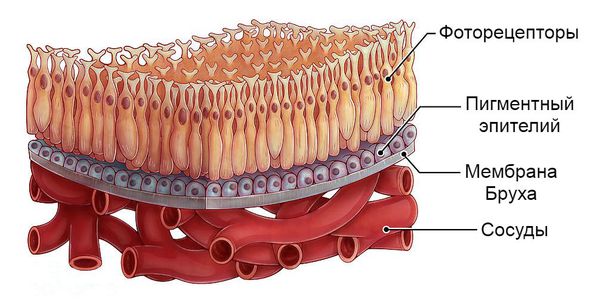
Большинство наружных сегментов фоторецепторов разрушается полностью, при этом во внутренних сегментах светочувствительных клеток скапливаются продукты кислых мукополисахаридов, вызывая изменения в сетчатке. Слой пигментного эпителия отделяется от слоя фоторецепторов, из-за чего формируется немного проминирующее (выбухающее) жёлтоватое образование, т.е. киста, которая локализуется в центральной или околоцентральной области сетчатки [3].
Заболевание относится к наследственным ретинальным дистрофиям. В Международной классификации болезней (МКБ-10) ему присвоен код H35.5.
Болезнь Беста всегда протекает с прохождением четырёх определённых стадий, которые завершаются образованием рубца в центральной области сетчатки [1].
- Первая стадия — превителлиформная. Она предшествует формированию кисты. В макуле наблюдаются изменения пигментации в виде множества маленьких желтоватых очажков. Во время электроокулографии фиксируются аномальные изменения.
- Вторая стадия — вителлиформная. Формируется классическая вителлиформная киста, которая при осмотре очень похожа на “яичный желток” довольно крупных размеров (до 1 диаметра диска зрительного нерва). Изменения асимметричны и практически всегда поражают оба глаза. Офтальмоскопические изменения не соответствуют высокой остроте зрения: даже у пожилых пациентов этот показатель находится в пределах от 0,4 до 0,9.
- Третья стадия — разрыв кисты и её резорбция, т. е. рассасывание. Острота зрения снижается, пациентам становится трудно читать мелкий текст.
- Четвёртая стадия — формирование фиброглиального рубца на месте кисты. Также на этой стадии возможно развитие субретинальной неоваскуляризации — образование новых сосудов под сетчаткой [3]. Острота зрение падает ещё сильнее, в поле зрения появляются слепые зоны.
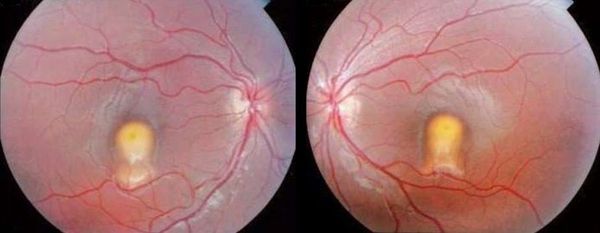
На поздних стадиях заболевания начинают развиваться осложнения. Самые частые — это образование сквозных разрывов в макулярной области, потеря центральной остроты зрения и формирование “пятна перед глазами”. Возникновение отслойки сетчатки встречается реже.

Одним из частых осложнений так же является субретинальная неоваскуляризация — образование новых сосудов в зоне глазного дна [11]. Она является одной из причин инвалидизации при болезни Беста, так как приводит к стойкому снижению центральной остроты зрения. При этом полная слепота не развивается.
Для постановки диагноза “болезнь Беста” необходим ряд обследований. В первую очередь нужно зарегистрировать специфическую офтальмоскопическую картину глазного дна, характерную для каждой стадии заболевания. Затем, чтобы оценить состояние сетчатки, следует выполнить электроокулографию (ЭОГ) и электроретинографию (ЭРГ). В последние годы, с развитием генетики, стало обязательным молекулярное генетическое исследование пациента. Вместе с этим производят офтальмологическое и генетическое обследование других членов семьи.
Офтальмоскопия позволяет обнаружить первые признаки болезни Беста на первом и втором десятилетии жизни. На первых стадиях в макуле появляются желтоватые очажки, затем формируются виттелиформные кисты, при разрывах которых глазное дно напоминает картину “яичницы-глазуньи”. На последних стадиях в макуле формируется атрофические глиальные рубцы, а при осложнениях — неоваскулярная мембрана и сквозные макулярные отверстия.

Электроокулография является очень важным методом диагностики при болезни Беста. С её помощью можно выявить такой специфический признак заболевания, как снижение коэффициента Ардена — соотношения биопотенциала глаз в темноте и при свете. Данный показатель будет снижен даже на нулевой стадии болезни при нормальной офтальмоскопической картине. В случае вителлиформной макулодистрофии взрослых электроокулография изменений не выявит.

Флюоресцентная ангиография позволяет диагностировать болезнь Беста даже на доклиническом этапе. Изменения сетчатки зависят от стадии заболевания. На начальном этапе болезни видны мелкие окончатые дефекты и участки с локальной гиперфлюоресценцией (свечением). При наличии сформированной кисты флюоресценция полностью отсутствует. На третьей стадии болезни гиперфлюоресценция наблюдается только в верхней части кисты, а в нижней её части отсутствует [8].
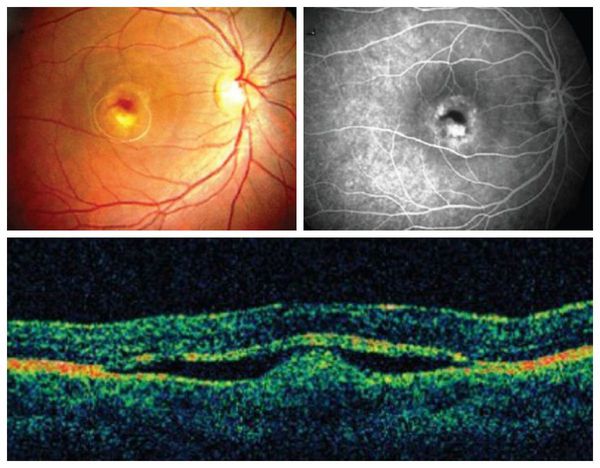
При электроретинографии (общей и ритмичной) наблюдается снижение амплитуды “а” волн, увеличение латентных периодов “а” и “b” волн, а также угнетение ответа от центральных отделов сетчатки [9].
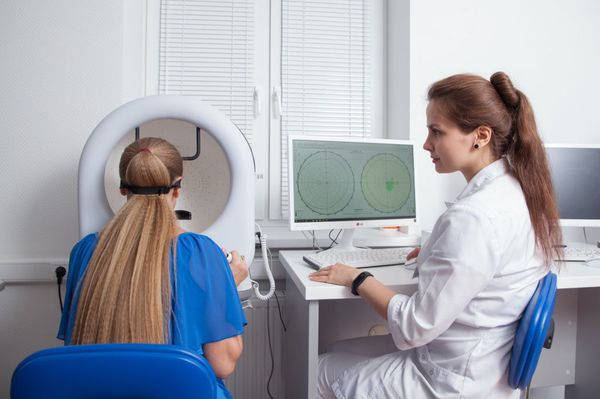
Статическая компьютерная периметрия выявляет снижение чувствительности макулярной области, а при разорвавшейся вителлиформной кисте — центральную абсолютную скотому (слепое пятно). При этом границы поля зрения по периферии остаются в норме.
Дифференциальная диагностика
Болезнь Беста необходимо отличить от других заболеваний:
- болезни Коатса и других макулярных дистрофий пигментного эпителия сетчатки (Х-образной макулярной дистрофии);
- острого хориоретинита (в первую очередь токсоплазмозной этиологии);
- болезни Штаргардта;
- вителлиформной дистрофии взрослых;
- отслойки пигментного эпителия сетчатки [11].
Болезнь Коатса — врождённая ненаследственная патология, при котором наблюдаются аномалии сосудов сетчатки глаза. Она может стать причиной частичной или полной слепоты. На первых стадиях болезнь Коатса так же, как и болезнь Беста, течёт без симптомов и в большинстве случаев диагностируется у детей 2-8 лет при случайных профилактических осмотрах, проводимых в детских садах или школах. В отличие от болезни Беста, при болезни Коатса, как правило, в патологический процесс вовлекается только один глаз. Лишь у 5-8 % больных наблюдаются двусторонние изменения. Мальчики заболевают им в 3 раза чаще, чем девочки [9].
У большинства пациентов с заболеванием Коатса во время первого офтальмологического обследования в центральной области сетчатки выявляют возвышающийся округлый очаг твёрдого желтоватого экссудата, очень похожий на вителлиформные изменения, встречающиеся при болезни Беста. Данные экссудаты в центральной области сетчатки очень часто сочетаются с кровоизлияниями за сетчаткой и образованием новых сосудов, что тоже характерно для болезни Беста.
Диагностика болезни Коатса основывается на результатах осмотра глазного дна (офтальмоскопии), а также центральной области и периферии глазного дна с применением или налобного офтальмоскопа с линзами 20-30 дптр, или офтальмобиомикроскопии с трёхзеркальной линзой Гольдмана. У большинства пациентов с болезнью Коатса во время данного обследования обязательно выявляются аномалии сосудов: микро- и макроаневризмы, телеангиэктазии (сосудистые звёздочки), артериовенозные шунты. Чаще всего эти аномалии располагаются в височной половине сетчатки.
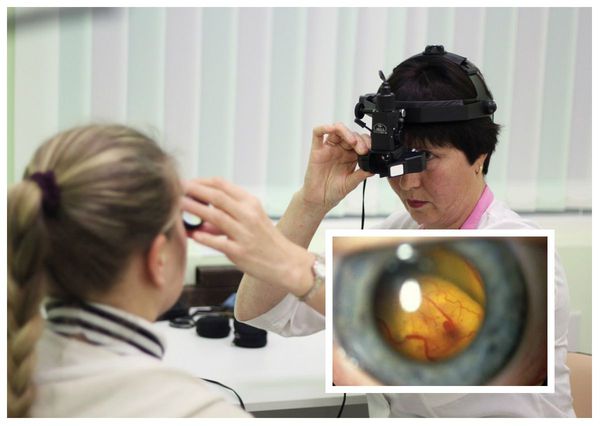
Изменения при электроокулографии в начальной и развитой стадиях заболевания, как и при болезни Беста, не выявляются. Но острота зрения у больных с ретинитом Коатса низкая: при наличии изменений в центральной области сетчатки она не превышает 0,4, а при болезни Беста длительно сохраняются в норме [7].
Острый токсоплазмозный хориоретинит — это паразитарное заболевание глаз, для которого характерно в основном скрытое или хроническое течение. Как правило, оно поражает только один глаз, в отличие от болезни Беста. При неадекватном и несвоевременном лечении может привести к стабильному снижению остроты зрения.
Трудности при диагностике обычно возникают при обследовании больных с приобретённым токсоплазмозом и экссудативно-геморрагическими изменениями в центральной области сетчатки, которые похожи на вителлиформные очажки с субретинальными геморрагиями, как при болезни Беста. Хориоретинальные поражения при токсоплазмозе сочетаются с выпотом в стекловидное тело различной степени тяжести, а порой и изменениями переднего отрезка глаза.
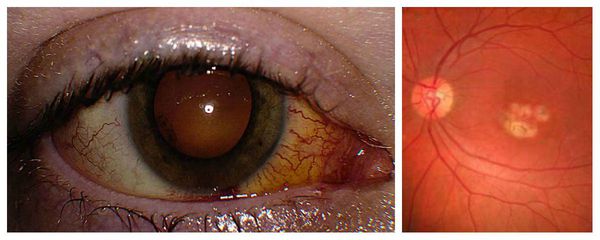
Пациенты, как правило, предъявляют жалобы на внезапное, резкое и значительное снижение центральной остроты зрения, которая в ряде случаев изменяется до 0,01-0,2. При статической периметрии регистрируется повышенный порог яркостной чувствительности, относительная или абсолютная центральная скотома. Электроокулография, как правило, не изменена.
Для подтверждения и верификации токсоплазмоза необходимо выполнить иммунологические исследования, определить антитела к токсоплазме или выделить её методом ПЦР (полимеразной цепной реакции). В 95 % случаев токсосплазмозный хориоретинит хорошо поддаётся лечению, острота зрения может восстановиться до исходных значений [12].
Болезнь Штаргардта иначе называют ювенильной макулярной дегенерацией. Впервые это заболевание описал немецкий врач-офтальмолог К. Штаргардт как врождённое поражение макулы, которое передавалось по наследству в одной семье.
Как правило, болезнь Штаргардта начинается в молодом (ювенильном) возрасте и сопровождается поражением центральной области сетчатки, как и болезнь Беста. Её отличает быстрое прогрессирование, вплоть до инвалидизации. Медленное ухудшение зрения встречается крайне редко (при доминантном типе наследования) [9].
Данное заболевание всегда двустороннее и симметричное. Его характерными признаками являются различные процессы: атрофия хориоидеи (сосудистой оболочки глаза), “бычий глаз”, очаг дистрофии цвета “битой (кованой) бронзы” и др. При далеко зашедшем процессе фовеолярный рефлекс (центральная ямка макулы) отсутствует. В макулярной области на уровне пигментного эпителия сетчатки наблюдаются скопления коричневатого, тёмного пигмента, который окружён участками гипер- и депигментации. Эти скопления отличаются от вителлиформных жёлтых очагов при болезни Беста.
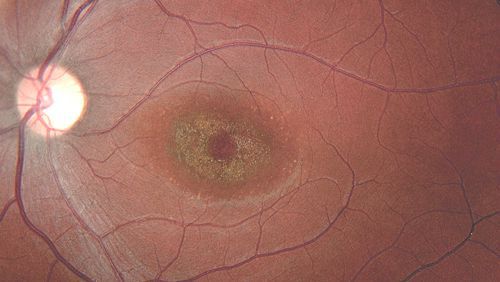
Вителлиформная макулодистрофия взрослых, в отличие от болезни Беста, развивается у людей 40-50 лет. Для неё характерно двустороннее симметричное поражение макулы с локальными изменениями. Очаги патологии, как правило, имеют округлую форму и жёлтый оттенок. Их отличает отсутствие прогрессирования и небольшие размеры: диаметр поражений достигает 0,3-0,5 размера диска зрительного нерва. При этом нарушения зрительных функций минимальны.
Вещества, подобные липофусцину, скапливаются диффузно в различных местах: в пигментном эпителии, внутренней части фоторецепторов, мюллеровских клетках и даже в стекловидном теле.
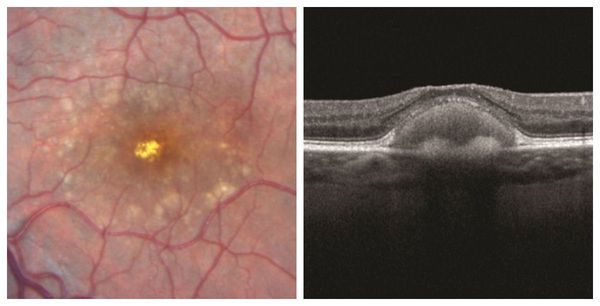
Отслойка пигментного эпителия сетчатки возникает при нарушении нормального соединения пигментного эпителия сетчатки с мембраной Бруха. К причинным факторам относятся сосудистые, воспалительные и дистрофические процессы.
Длительное время болезнь может существовать без какой-либо динамики, спонтанно исчезать, а вследствие инвазии сосудов из хориоидеи трансформироваться в геморрагическую отслойку. Сложности в диагностике могут возникнуть при атипичной клинической картине заболевания и экссудативных изменениях в центральной области сетчатки.
Обычно болезнь поражает только один глаз. Общая электроретинография не меняется, локальная — может быть снижена. Электроокулография, как правило, в норме. При флюоресцентной ангиографии на последней стадии отслойки регистрируется гиперфлюоресценция.
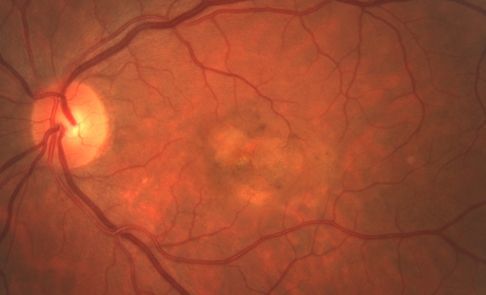
Лечения болезни Беста на сегодняшний момент не существует. Можно лишь затормозить формирование кист, предотвратить их разрывы и наступление осложнений, которые сильно влияют на остроту зрения пациента. С этой целью применяется антиоксидантная и вазоактивная терапия, а также витамины С, Е и А. Вазоактивные препараты улучшают кровоснабжение сетчатки, а витамины являются мощными антиоксидантами [5].
Вероятно, что в будущем при лечении болезни Беста будет применяться генная инженерия или терапия, направленная на нормализацию тока жидкости через пигментный эпителий сетчатки, торможение накопления липофусцина и воздействия на другие этапы патогенеза [13].
Прогноз для зрения относительно благоприятный. Так как заболевание протекает медленно, острота зрения снижается постепенно, при этом страдает только центральное зрение. Благодаря сохранению периферического зрения человек хорошо адаптируется, часто сохраняя работоспособность и возможность чтения.
При обнаружении заболевания врач должен проинформировать больного о вариабельности течения заболевания, рисках его возникновения у будущих детей и функциональных прогнозах. Желательно проконсультироваться с врачом-генетиком.
Все члены семьи пациента обязательно должны пройти обследование у офтальмолога. Сам пациент должен регулярно наблюдаться у своего лечащего врача [14].Чтобы дети и подростки не отставали в развитии, необходимо вовремя применять технические средства реабилитации слабовидящих [1].
Источник
