Синдром ломкой х хромосомы что это

Синдром Мартина-Белл – это наследственная болезнь, которая характеризуется стойким интеллектуальным снижением, расстройствами аутистического спектра и специфическими фенотипическими особенностями. Ключевой симптом – недостаточность познавательных функций. Отмечается гиперактивность, дефицит коммуникативных способностей, замкнутость. Лицо удлиненное, ушные раковины большие, лоб выступающий, кончик носа загнутый. Диагностика основывается на клинико-анамнестических данных и результатах биогенетического анализа. Лечение симптоматическое, включает использование медикаментов и психолого-педагогическую коррекцию.
Общие сведения
Синдром Мартина-Белл получил свое название по фамилиям исследователей, впервые описавших патологию. В 1943 году физиологи из Великобритании Д. Мартин и Д. Белл изучали 11 случаев олигофрении у мужчин из одной семьи, в которой женщины имели нормальное интеллектуальное развитие. Генетическая основа заболевания была выявлена в 1969 году американским генетиком Г. Лабсом. Синонимичное название – синдром ломкой X-хромосомы. Распространенность среди мальчиков составляет 1:4 000, среди девочек – 1:6 000. Согласно данным зарубежных врачей-генетиков, частота синдрома Мартина-Белл у пациентов мужского пола с умственной отсталостью достигает 1,9-5,9%. Отечественные исследования указывают на более высокие значения, в соответствии с ними этот синдром имеют 8-10% больных олигофренией.
Синдром Мартина-Белл
Причины
Синдром Мартина-Белл является результатом дефекта гена FMR1, расположенного в X-хромосоме. Наследование происходит по доминантному сцепленному с полом типу с неполной пенетрантностью. У мужчин присутствует одна X-хромосома, поэтому мутантный аллель всегда провоцирует болезнь. У женщин есть две половые хромосомы типа X: одна активная, другая – резервная, инактивированная. Таким образом, при наличии мутации в одном из двух генов FMR1 заболевание проявляется или нет в зависимости от активности измененной хромосомы. Мужчины с ломкой хромосомой X не могут передать ее сыновьям, но передают всем дочерям, которые либо болеют, либо остаются здоровыми носителями мутации. Женщины с дефектной хромосомой передают ее детям обоих полов с вероятностью 50%. Наследование синдрома учащается от поколения к поколению, этот феномен называется парадоксом Шермана.
Патогенез
При секвенировании FMR1-гена было выявлено, что основой симптоматики и цитогенетически определяемой ломкости хромосомы X является многократное увеличение количества единичных тринуклеотидов ЦГГ. Это приводит к подавлению транскрипции и последующему недостаточному производству белка FMR1, ответственного за развитие центральной нервной системы, а именно – за формирование аксонов и синапсов, появление и усложнение нейронных связей, успешность процессов обучения и запоминания.
Участок хромосом, подверженный структурным изменениям при наследственном синдроме Мартина-Белл, может находиться в четырех состояниях, характеризующихся различным удлинением повторяющихся последовательностей тринуклеотидов. При отсутствии болезни и носительства определяется нормальное количество повторов – от 6 до 39. В промежуточном состоянии диагностируется 40-60 повторов, в состоянии премутации – 55-200. В обоих случаях заболевание отсутствует. Поскольку экспансия тринуклеотидов возможна лишь в период гаметогенеза, премутация способна превратиться в полную мутацию. Это происходит при передаче измененного материнского гена, аллель «утяжеляется» во время овогенеза. При полной мутации выявляется больше 200 повторов ЦГГ, чаще всего – от 230 до 4 000.
Симптомы
Дети рождаются с увеличенной массой тела, в среднем – 3,5-4 кг. Первыми обращают на себя внимание фенотипические особенности младенцев. Характерен макроорхизм – увеличение яичек без эндокринного заболевания. Окружность головы больше нормы или соответствует ее верхним границам. Лоб высокий и широкий, лицо вытянутое с уплощенной средней частью. Нос имеет слегка клювовидный загиб, ушные раковины крупные, располагаются низко. Суставы отличаются хорошей подвижностью, кости кистей и стоп широкие. Кожа зачастую гиперэластичная, волосы и радужные оболочки глаз светлого оттенка. Фенотипические признаки могут быть выражены по-разному, от одного-двух едва определяемых до полного комплекса.
Ключевое клиническое проявление заболевания – умственная отсталость. Стойкое интеллектуальное снижение проявляется слабым развитием сложных форм мышления и памяти. Пациентам недоступно понимание абстрактно-логических высказываний и явлений, использование категорий, установление аналогий. Сравнение, анализ и обобщение могут осуществляться на простом уровне, например, в конкретных бытовых ситуациях. Словарный запас обеднен. У многих мальчиков IQ равен 40-50 баллам, реже достигает 70-79. Относительно сохранна номинативная речь и зрительное восприятие. У девочек когнитивное снижение менее выраженное, соответствует легкой степени олигофрении или пограничному уровню интеллектуального развития.
Другой типичный симптом заболевания – своеобразие речи. Она ускоренная, сбивчивая, изобилует повторами, эхолалиями и персеверациями. Аутистические расстройства представлены трудностями коммуникации и поведенческими нарушениями. Дети часто проявляют агрессивность и замкнутость при попытке установления контакта. В тяжелых случаях развивается мутизм – полное отсутствие речи как средства общения. В поведении преобладает двигательная расторможенность, гиперактивность, стереотипии, самопровреждения. Пациенты избегают смотреть в глаза, не допускают прикосновений, но по сравнению с больными аутизмом интерес к общению присутствует. Стереотипные движения включают хлопки руками, прыжки, вращения вокруг своей оси, встряхивания руками, бег по кругу, гримасничанье и однообразное хныканье. Имеются трудности планирования и контроля поведения, переключения внимания и пространственной координации.
Неврологические симптомы неспецифичны. Определяется легкое снижение мышечного тонуса, двигательная дискоординация. Недостаточное развитие мелкой моторики затрудняет освоение письма, некоторых игровых и бытовых навыков (сборки конструктора, рисования, шитья и др.). У части больных имеются глазодвигательные нарушения, усиление сухожильных рефлексов, экстрапирамидные паракинезы, например, зажмуривание глаз, нахмуривание бровей, гримасничанье. При тяжелых формах синдрома возникают эпилептические припадки. У 25% пациенток с премутационным состоянием развивается первичная недостаточность яичников.
Диагностика
При выраженных фенотипических изменениях заболевание может быть обнаружено с первых месяцев жизни ребенка – неонатологи и врачи-педиатры обращают внимание на увеличенные размеры яичек и характерные особенности лица. В иных случаях подозрение на умственную отсталость возникает в возрасте от полугода до 2-3 лет. В этот период прослеживается отставание умственного развития, поведенческие и речевые нарушения. Дифференциальная диагностика нацелена на исключение РАС, в частности раннего детского аутизма, а также умственной отсталости другого происхождения (не связанной с ломкостью хромосомы Х). Обследование проводится психиатрами, неврологами и врачами-генетиками, включает:
- Клинический опрос, осмотр. В беседе с ребенком на первый план выходит снижение интеллекта, гиперактивность и расторможенность поведения, нарушение коммуникативных навыков. Уровень психического развития не соответствует возрасту, методики исследования интеллекта выявляют олигофрению (IQ – 40-79 баллов). Внешне наблюдаются характерные фенотипические признаки, при неврологическом осмотре выявляется мышечный гипотонус, усиленные сухожильные рефлексы, паракинезы.
- Генеалогический анализ. В отличие от других форм олигофрении при синдроме Мартина-Белл прослеживается наследственная передача болезни. Как правило, у пациента имеются родственники с данным заболеванием, чаще – мужчины (дед, дядя, брат). Иногда признаки легкого интеллектуального снижения обнаруживаются у матери, но диагноз у нее часто не установлен (не подтвержден).
- Генетическое исследование. В лабораторных условиях исследуется строение ДНК: определяется количество ЦГГ-повторов и статус метилирования. Применяется ПЦР и цитогенетический метод. Диагноз подтверждается, если количество триплетных повторов составляет более 200. При результате 60-199 возможны легкие фенотипические проявления болезни, риск развития патологии в следующем поколении (если показатель диагностирован у женщины).
Лечение синдрома Мартина-Белл
Методы специфической терапии синдрома в настоящее время отсутствуют. Проводится симптоматическое медикаментозное лечение и психолого-педагогическая коррекция. Усилия врачей и специальных психологов направлены на минимизацию эмоционально-поведенческих отклонений, овладение навыками ходьбы, речи и общения, чтения и письма. Медикаментозная терапия включает прием психостимуляторов, антидепрессантов, ноотропов, противоэпилептических средств и гормональных препаратов (при первичной недостаточности яичников). Обучение пациентов проводится по специальным коррекционно-развивающим программам. Для улучшения социальных навыков используются методы когнитивно-поведенческой терапии, групповые тренинги.
Прогноз и профилактика
Синдром Мартина-Белла не имеет осложнений и не сокращает продолжительность жизни больных, поэтому при своевременной и адекватной медико-психолого-педагогической помощи прогноз достаточно благоприятный: пациенты осваивают навыки общения и самообслуживания, обучаются в специальных школах, иногда овладевают рабочими профессиями. Профилактика основана на медико-генетическом консультировании пар из групп риска и пренатальной диагностике синдрома. Эти меры необходимы женщинам с синдромом преждевременного истощения яичников, семьям, в которых диагностированы премутационные состояния FMR1 или выявлены случаи интеллектуальной недостаточности у мальчиков и мужчин.
Источник
Здравствуйте. Сегодня я расскажу вам о синдроме ломкой Х-хромосомы и его влиянии на женскую репродуктивную функцию и здоровье потомства, о связи генов и бесплодия, о методах диагностики при раннем истощении резерва яичников. Всеми этими проблемами мы занимаемся в Центре иммунологии и репродукции.
Синдром ломкой X-хромосомы – наследственное заболевание, при котором нарушена работа гена FMR1. Суть генетического нарушения в увеличении количества повторов сочетания из трех «букв» генетического кода CGG. У здоровых людей таких повторов в X-хромосоме не более 50–60. При синдроме ломкой X-хромосомы – более 200.
Состояние, когда повторов от 60 до 200, называется премутацией. У ее носителя практически нет симптомов, но повышен риск возникновения полноценной мутации у потомства. Другие названия патологии – синдром фрагильной хромосомы X и синдром Мартина-Белл.
Мутация в гене FMR1 – одна из самых распространенных вместе с синдромом Дауна причин наследственного интеллектуального нарушения. Но этот генетический дефект привлекает и пристальное внимание врачей-репродуктологов, потому что он приводит к преждевременному истощению овариального резерва и может передаваться ребенку.
Распространенность синдрома ломкой X-хромосомы встречается у одного из 4000 мужчин и одной из 8000 женщин. Такое различие связано с тем, что у женщин две X-хромосомы. Если в одной возникает дефект, вторая может его компенсировать. У мужчин только одна X-хромосома. Поэтому, если им достается мутация FMR1, она проявляется в полную силу.
Премутация встречается очень часто: у каждой из 250 женщин в одной из X-хромосом имеется более 50 повторов CGG.
Почему возникают симптомы?
При экстремальном увеличении количества копий последовательности CGG происходит метилирование промотора – участка ДНК, который активирует экспрессию т.е.преобразование генетического кода в структуру белка гена FMR1. В итоге ген не работает. В организме он отвечает за формирование связей в нервной системе и некоторые другие важные процессы. В итоге возникают нарушения, которые и проявляются характерными симптомами.
Симптомы синдрома Мартина-Белл
Несмотря на то, что премутация у женщин зачастую не проявляется какими-либо симптомами, она нарушает репродуктивную функцию и может привести к проблемам со здоровьем у потомства.
- Во- первых, первичная недостаточность яичников.
У женщин с дефектным геном FMR1 рано происходит истощение овариального резерва, и менопауза наступает до 40 лет. Поэтому при преждевременной менопаузе врач может порекомендовать пройти генетический анализ. По статистике, в 5% случаев раннее истощение овариального резерва становится следствием синдрома ломкой X-хромосомы.
Недостаточность яичников возникает примерно у 25% носительниц премутации.
- Во-вторых, передача дефектного гена потомству.
Если у женщины премутация, ее детям может достаться полноценная мутация, когда число повторов CGG увеличено более 200. При этом у девочки симптомы возникнут с вероятностью 30–50%, а у мальчика почти гарантированно. Мужчина со 100% вероятностью передаст ломкую X-хромосому всем дочерям, но ни одному из сыновей , потому что дочь в любом случае получит одну X-хромосому от отца, а сын – всего одну только от матери.
- Существуют и другие симптомы. В первую очередь синдром ломкой X-хромосомы грозит потомству нарушением интеллекта.
Развивается умственная отсталость легкой или средней степени тяжести. У некоторых детей возникают симптомы аутизма: они много раз повторяют одни и те же слова, фразы, действия, не входят в зрительный контакт во время общения, избегают социума.
- Синдром фрагильной хромосомы X может привести к тремору/атаксии, ассоциированному с ломкой X-хромосомой .
Чаще всего патология поражает мужчин и встречается примерно у трети носителей премутации. Симптомы этого состояния: тремор , мозжечковая атаксия, то есть нарушение чувства равновесия, паркинсонизм, деменция .
Обычно первые признаки появляются после 50 лет, до этого возраста человек чувствует себя абсолютно здоровым.
- Другие возможные проявления синдрома Мартина-Белл.
Характерные черты лица: выступающий лоб и подбородок, большие уши. Высокое сводчатое нёбо. Чрезмерная подвижность суставов. Пролапс митрального клапана и другие проблемы с сердцем.
Сразу после рождения установить диагноз невозможно. Симптомы ломкой X-хромосомы могут появиться только после того, как ребенку исполнится год.
- Диагностика синдрома ломкой Х-хромосомы
Раньше это состояние выявляли с помощью цитогенетических исследований. У человека получали образец клеток, вводили в них фолиевую кислоту, и после этого становилось видно, что в X-хромосоме есть как бы разрыв. Один участок «отшнуровывается». На самом деле хромосома цела, просто такой эффект создается из-за мутации. В настоящее время от цитогенетического анализа отказались, так как он недостаточно точен.
Кстати, раньше синдром Мартина-Белл считался хромосомным заболеванием, как и синдром Дауна. Эта группа патологий связана с нарушением структуры и количества хромосом. В настоящее время известно, что это генная болезнь, то есть нарушение происходит на уровне одного определенного гена.
Современный метод диагностики ломкой хромосомы X – полимеразная цепная реакция , когда с помощью фермента получают много копий ДНК, и конечные продукты выявляют методом капиллярного электрофореза. Это позволяет точно определить мутантный ген и его размер до 200 повторов CGG.
Кому показан анализ на ломкую х-хромосому?
Женщине стоит пройти этот анализ в следующих случаях:
- При ранней до 40 лет менопаузе.
- При нарушении репродуктивной функции, в сочетании с повышенным уровнем фолликулостимулирующего гормона ,пониженном антимюллеровом гормоне , урежении ,то есть более 35 дней в цикле и укорочении – менее 3 дней менструации.
- Если у родственников диагностирован синдром ломкой X-хромосомы.
Во многих странах сейчас исследование на мутацию гена FMR1 у плода включено в обязательную программу скрининга во время беременности. Нарушение намного проще выявить у будущей мамы, чем у ребенка, особенно если у женщины имеется премутация, а ребенку досталась полноценная мутация.
ПЦР хуже выявляет дефекты в гене FMR1, если число копий CGG более 200, можно получить ложноотрицательный результат.
Что делать, если анализ обнаружил это нарушение?
Положительный результат анализа на ломкую Х-хромосому
Если у будущей мамы еще до беременности диагностирована премутация или мутация, это дает шанс не допустить передачи заболевания потомству. В ходе ЭКО врачи могут отобрать эмбрионы с нормальной X-хромосомой.
Если из-за синдрома ломкой X-хромосомы у женщины происходит преждевременное истощение овариального резерва, также может помочь ЭКО. Это состояние обязательно учитывается в ходе процедуры, потому что такие женщины хуже реагируют на гормональную стимуляцию яичников.
Такой анализ можно сделать в Лаборатории ЦИР. Мы проводим все доступные лабораторные исследования, которые помогают разобраться в нарушении репродуктивной функции, оценить риски для потомства, вероятность развития тех или иных осложнений во время беременности.
Если у Вас есть вопросы по теме видео, пишите их в комментариях или приходите на консультацию. Часто доступна онлайн-поддержка, о которой Вы можете узнать по ссылке на нашем сайте.
Источник
Генетические особенности синдрома ломкой Х-хромосомы
Среди группы наследственных болезней есть два заболевания, относящихся к самым частым причинам интеллектуальной недостаточности. Самая известная и наиболее распространённая патология – синдром Дауна, связанный с наличием лишней 21-ой хромосомы в геноме человека. В этой статье мы расскажем о втором по распространенности наследственном заболевании, которое приводит к умственной отсталости, а также может сопровождаться другими клиническими проявлениями.
Синдром ломкой X-хромосомы или синдром Мартина-Белл является результатом нарушения в гене FMR1 (fragile X mental retardation-1), который расположен на Х-хромосоме и играет важную роль в появлении и развитии нервных связей, обучении и запоминании. Частота этого синдрома среди мальчиков составляет 1:4000.
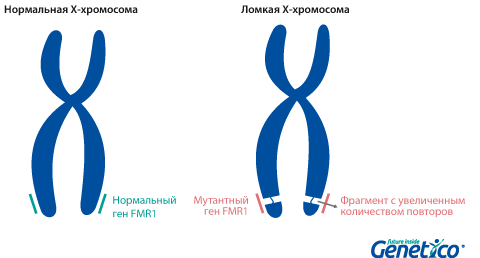
Так называемая «ломкость» X-хромосомы проявляется в том, что хромосома выглядит нетипично при специальном окрашивании, как будто один кусок отделился, хотя физически она остается цельной. Генетическая основа этого явления заключается в увеличении числа тринуклеотидных повторов CGG в гене FMR1, расположенном на X-хромосоме.
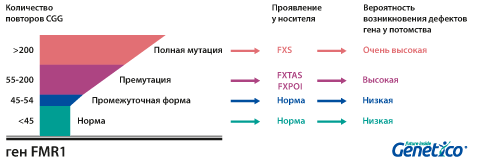
У здоровых людей число повторов в этом гене колеблется от 5 до 54. Если повторов больше 200, то наработка белка с гена FMR1 нарушается, что приводит к развитию синдрома Мартина-Белл и клиническому проявлению заболевания. Премутационное состояние — это количество повторов CGG от 55 до 200. В таком состоянии заболевание у людей в типичной форме не проявляется, но чем больше повторов в этом гене у носителя, тем больше вероятность того, что у ее или его детей количество повторов будет больше 200 и заболевание разовьется. В случае носительства премутации при формировании половых клеток количество повторов может увеличиваться, поэтому если у родителя количество повторов от 55 до 200, то высока вероятность рождения ребенка с мутантным геном FMR1 и синдромом Мартина-Белл. При этом носительство премутационного состояния будущим папой и мамой неравнозначно по вероятности возникновения мутантного аллеля у их детей: если носитель – мама, то вероятность значительного увеличения числа повторов гораздо выше. Количество повторов от 45 до 54 является промежуточной формой, которая не имеет никакого влияния на здоровье человека, но может приводить к проблемам у будущих поколений, как и в случае премутационного состояния гена.
Важно учитывать, что наследование и развитие заболевания зависит от пола, так как ген FMR1 находится на Х-хромосоме. У мужчин только одна Х-хромосома, которую они получают от матери. Поэтому, в случае, если эта одна хромосома оказалась «ломкой», у них проявляется заболевание. У женщин две Х-хромосомы, однако активно работает только одна из них. Поэтому наличие одной Х-хромосомы с мутантным геном FMR1 может не проявляться клинически, в случае инактивации именно «ломкой» хромосомы, или приводить к развитию заболевания в 30-50% случаев. Мужчина с ломкой Х-хромосомой может передать её всем дочерям, но ни одному из сыновей. Женщина с мутантной хромосомой имеет шансы передать её как сыновьям, так и дочерям с равной вероятностью.
Премутационное состояние гена влияет как на судьбу потомков носителя такого гена, так и непосредственно на его здоровье:
Развитие первичной недостаточности яичников (FXPOI) (снижение овариального резерва и наступление менопаузы до 40 лет). Мутация FMR1 является причиной преждевременного истощения яичников у 5% женщин с этим диагнозом. Среди носительниц премутации примерно у четверти развивается это состояние. Оно влияет не только на общие репродуктивные возможности, но и на подбор протокола стимуляции при ВРТ, так как часто оказывается причиной бедного ответа яичников на стимуляцию. Интересно, что по данным, полученным в центре Genetico, хотя бедный ответ яичников на стимуляцию влияет на число получаемых в цикле эмбрионов, он не приводит к увеличению доли анеуплоидных эмбрионов.
Тремор/атаксия, ассоциированные с ломкой Х-хромосомой (FXTAS). Это состояние чаще развивается у мужчин: при носительстве премутации мужчиной проявляется в 33% случаев, а при носительстве премутации женщиной – лишь в 5-10%. Синдром FXTAS начинает проявляться в пожилом возрасте. Наблюдается тремор, шаткая походка, может страдать речь.
Метод диагностики, используемый в лаборатории Genetico, основан на использовании полимеразной цепной реакции с особым набором праймеров, позволяющих не только детектировать нормальное, премутационное и мутационное состояния, но и точно определить количество повторов в случаях, когда их меньше 200. Такая диагностика позволяет выявить синдром ломкой X-хромосомы на молекулярном уровне, а также оценить вероятность рождения ребенка с этим синдромом и возможность развития у пациента расстройств, связанных с увеличенным количеством повторов в гене FMR1. Такая диагностика также позволяет детектировать наличие AGG повторов среди повторов CGG. Полагают, что участки AGG, прерывающие длинную последовательность из CGG повторов, придают ДНК устойчивость и снижают риск увеличения количества повторов в следующем поколении.
Генетический тест, определяющий количество повторов в гене FMR1, рекомендуется пройти в первую очередь женщинам с синдромом преждевременного истощения яичников или с выявленной неслучайной инактивацией Х-хромосомы (косвенный признак), семьям, в которых есть сыновья с интеллектуальной недостаточностью. Также анализ состояния гена FMR1 необходим:
1) женщинам с репродуктивными проблемами или нарушениями фертильности, связанными с повышенным уровнем фолликулостимулирующего гормона (ФСГ)
2) пациентам с интеллектуальной недостаточностью и их родственникам
3) тем, у кого в семье были случаи синдрома ломкой Х-хромосомы или умственной отсталости без точного диагноза
4) женщинам, у родственников которых наблюдались нарушения, связанные с премутационным состоянием FMR1
5) пациентам с поздно проявившимся тремором и мозжечковой атаксией (нарушения согласованности работы мышц из-за поражения систем мозга, управляющих движением мышц).
В случае обнаружения бессимптомного носительства мутации в гене FMR1 у женщины может быть рекомендовано использование донорских ооцитов или проведение преимплантационной генетической диагностики (ПГД) с целью исключить возможность проявления синдрома у ребенка. Также важно правильно оценивать риск рождения больного ребенка в случае премутационного состояния гена FMR1 у будущих родителей. В таком случае по результатам теста рекомендуется консультация врача-генетика.
Автор: Очир Мигяев
Стажер лаборатории Genetico
Источник
