Синдром мартин белл и аутизм
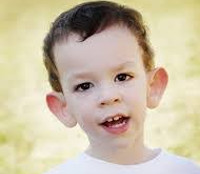
Синдром Мартина-Белл – это наследственная болезнь, которая характеризуется стойким интеллектуальным снижением, расстройствами аутистического спектра и специфическими фенотипическими особенностями. Ключевой симптом – недостаточность познавательных функций. Отмечается гиперактивность, дефицит коммуникативных способностей, замкнутость. Лицо удлиненное, ушные раковины большие, лоб выступающий, кончик носа загнутый. Диагностика основывается на клинико-анамнестических данных и результатах биогенетического анализа. Лечение симптоматическое, включает использование медикаментов и психолого-педагогическую коррекцию.
Общие сведения
Синдром Мартина-Белл получил свое название по фамилиям исследователей, впервые описавших патологию. В 1943 году физиологи из Великобритании Д. Мартин и Д. Белл изучали 11 случаев олигофрении у мужчин из одной семьи, в которой женщины имели нормальное интеллектуальное развитие. Генетическая основа заболевания была выявлена в 1969 году американским генетиком Г. Лабсом. Синонимичное название – синдром ломкой X-хромосомы. Распространенность среди мальчиков составляет 1:4 000, среди девочек – 1:6 000. Согласно данным зарубежных врачей-генетиков, частота синдрома Мартина-Белл у пациентов мужского пола с умственной отсталостью достигает 1,9-5,9%. Отечественные исследования указывают на более высокие значения, в соответствии с ними этот синдром имеют 8-10% больных олигофренией.

Синдром Мартина-Белл
Причины
Синдром Мартина-Белл является результатом дефекта гена FMR1, расположенного в X-хромосоме. Наследование происходит по доминантному сцепленному с полом типу с неполной пенетрантностью. У мужчин присутствует одна X-хромосома, поэтому мутантный аллель всегда провоцирует болезнь. У женщин есть две половые хромосомы типа X: одна активная, другая – резервная, инактивированная. Таким образом, при наличии мутации в одном из двух генов FMR1 заболевание проявляется или нет в зависимости от активности измененной хромосомы. Мужчины с ломкой хромосомой X не могут передать ее сыновьям, но передают всем дочерям, которые либо болеют, либо остаются здоровыми носителями мутации. Женщины с дефектной хромосомой передают ее детям обоих полов с вероятностью 50%. Наследование синдрома учащается от поколения к поколению, этот феномен называется парадоксом Шермана.
Патогенез
При секвенировании FMR1-гена было выявлено, что основой симптоматики и цитогенетически определяемой ломкости хромосомы X является многократное увеличение количества единичных тринуклеотидов ЦГГ. Это приводит к подавлению транскрипции и последующему недостаточному производству белка FMR1, ответственного за развитие центральной нервной системы, а именно – за формирование аксонов и синапсов, появление и усложнение нейронных связей, успешность процессов обучения и запоминания.
Участок хромосом, подверженный структурным изменениям при наследственном синдроме Мартина-Белл, может находиться в четырех состояниях, характеризующихся различным удлинением повторяющихся последовательностей тринуклеотидов. При отсутствии болезни и носительства определяется нормальное количество повторов – от 6 до 39. В промежуточном состоянии диагностируется 40-60 повторов, в состоянии премутации – 55-200. В обоих случаях заболевание отсутствует. Поскольку экспансия тринуклеотидов возможна лишь в период гаметогенеза, премутация способна превратиться в полную мутацию. Это происходит при передаче измененного материнского гена, аллель «утяжеляется» во время овогенеза. При полной мутации выявляется больше 200 повторов ЦГГ, чаще всего – от 230 до 4 000.
Симптомы
Дети рождаются с увеличенной массой тела, в среднем – 3,5-4 кг. Первыми обращают на себя внимание фенотипические особенности младенцев. Характерен макроорхизм – увеличение яичек без эндокринного заболевания. Окружность головы больше нормы или соответствует ее верхним границам. Лоб высокий и широкий, лицо вытянутое с уплощенной средней частью. Нос имеет слегка клювовидный загиб, ушные раковины крупные, располагаются низко. Суставы отличаются хорошей подвижностью, кости кистей и стоп широкие. Кожа зачастую гиперэластичная, волосы и радужные оболочки глаз светлого оттенка. Фенотипические признаки могут быть выражены по-разному, от одного-двух едва определяемых до полного комплекса.
Ключевое клиническое проявление заболевания – умственная отсталость. Стойкое интеллектуальное снижение проявляется слабым развитием сложных форм мышления и памяти. Пациентам недоступно понимание абстрактно-логических высказываний и явлений, использование категорий, установление аналогий. Сравнение, анализ и обобщение могут осуществляться на простом уровне, например, в конкретных бытовых ситуациях. Словарный запас обеднен. У многих мальчиков IQ равен 40-50 баллам, реже достигает 70-79. Относительно сохранна номинативная речь и зрительное восприятие. У девочек когнитивное снижение менее выраженное, соответствует легкой степени олигофрении или пограничному уровню интеллектуального развития.
Другой типичный симптом заболевания – своеобразие речи. Она ускоренная, сбивчивая, изобилует повторами, эхолалиями и персеверациями. Аутистические расстройства представлены трудностями коммуникации и поведенческими нарушениями. Дети часто проявляют агрессивность и замкнутость при попытке установления контакта. В тяжелых случаях развивается мутизм – полное отсутствие речи как средства общения. В поведении преобладает двигательная расторможенность, гиперактивность, стереотипии, самопровреждения. Пациенты избегают смотреть в глаза, не допускают прикосновений, но по сравнению с больными аутизмом интерес к общению присутствует. Стереотипные движения включают хлопки руками, прыжки, вращения вокруг своей оси, встряхивания руками, бег по кругу, гримасничанье и однообразное хныканье. Имеются трудности планирования и контроля поведения, переключения внимания и пространственной координации.
Неврологические симптомы неспецифичны. Определяется легкое снижение мышечного тонуса, двигательная дискоординация. Недостаточное развитие мелкой моторики затрудняет освоение письма, некоторых игровых и бытовых навыков (сборки конструктора, рисования, шитья и др.). У части больных имеются глазодвигательные нарушения, усиление сухожильных рефлексов, экстрапирамидные паракинезы, например, зажмуривание глаз, нахмуривание бровей, гримасничанье. При тяжелых формах синдрома возникают эпилептические припадки. У 25% пациенток с премутационным состоянием развивается первичная недостаточность яичников.
Диагностика
При выраженных фенотипических изменениях заболевание может быть обнаружено с первых месяцев жизни ребенка – неонатологи и врачи-педиатры обращают внимание на увеличенные размеры яичек и характерные особенности лица. В иных случаях подозрение на умственную отсталость возникает в возрасте от полугода до 2-3 лет. В этот период прослеживается отставание умственного развития, поведенческие и речевые нарушения. Дифференциальная диагностика нацелена на исключение РАС, в частности раннего детского аутизма, а также умственной отсталости другого происхождения (не связанной с ломкостью хромосомы Х). Обследование проводится психиатрами, неврологами и врачами-генетиками, включает:
- Клинический опрос, осмотр. В беседе с ребенком на первый план выходит снижение интеллекта, гиперактивность и расторможенность поведения, нарушение коммуникативных навыков. Уровень психического развития не соответствует возрасту, методики исследования интеллекта выявляют олигофрению (IQ – 40-79 баллов). Внешне наблюдаются характерные фенотипические признаки, при неврологическом осмотре выявляется мышечный гипотонус, усиленные сухожильные рефлексы, паракинезы.
- Генеалогический анализ. В отличие от других форм олигофрении при синдроме Мартина-Белл прослеживается наследственная передача болезни. Как правило, у пациента имеются родственники с данным заболеванием, чаще – мужчины (дед, дядя, брат). Иногда признаки легкого интеллектуального снижения обнаруживаются у матери, но диагноз у нее часто не установлен (не подтвержден).
- Биогенетическое исследование. В лабораторных условиях исследуется строение ДНК: определяется количество ЦГГ-повторов и статус метилирования. Применяется ПЦР и цитогенетический метод. Диагноз подтверждается, если количество триплетных повторов составляет более 200. При результате 60-199 возможны легкие фенотипические проявления болезни, риск развития патологии в следующем поколении (если показатель диагностирован у женщины).
Лечение синдрома Мартина-Белл
Методы специфической терапии синдрома в настоящее время отсутствуют. Проводится симптоматическое медикаментозное лечение и психолого-педагогическая коррекция. Усилия врачей и специальных психологов направлены на минимизацию эмоционально-поведенческих отклонений, овладение навыками ходьбы, речи и общения, чтения и письма. Медикаментозная терапия включает прием психостимуляторов, антидепрессантов, ноотропов, противоэпилептических средств и гормональных препаратов (при первичной недостаточности яичников). Обучение пациентов проводится по специальным коррекционно-развивающим программам. Для улучшения социальных навыков используются методы когнитивно-поведенческой терапии, групповые тренинги.
Прогноз и профилактика
Синдром Мартина-Белла не имеет осложнений и не сокращает продолжительность жизни больных, поэтому при своевременной и адекватной медико-психолого-педагогической помощи прогноз достаточно благоприятный: пациенты осваивают навыки общения и самообслуживания, обучаются в специальных школах, иногда овладевают рабочими профессиями. Профилактика основана на медико-генетическом консультировании пар из групп риска и пренатальной диагностике синдрома. Эти меры необходимы женщинам с синдромом преждевременного истощения яичников, семьям, в которых диагностированы премутационные состояния FMR1 или выявлены случаи интеллектуальной недостаточности у мальчиков и мужчин.
Источник
Синдром Мартина-Белл (синдром ломкой Х-хромосомы) — генетический синдром, обусловленный мутацией гена FMR1, находящемся в Х-хромосоме. Синдром возникает, когда работа гена нарушена либо экспансией тринуклеотидных повторов (в 99% случаев), либо другой мутацией типа LOF (loss of function, утрата функции гена) — это может быть делеция или однонуклеотидная замена.
У мальчиков отмечаются интеллектуальные нарушения разной степени тяжести, в большинстве случаев выраженные (IQ колеблется от 30 до 55). Это особая форма расстройства умственного развития, сцепленная с полом. Характерен СДВГ, аутизм встречается в 25-60% случаев. Речь скомкана, часты эхолалии. Внешний вид имеет характерные признаки. Основными характерными чертами является макроцефалия, высокий широкий лоб, большая нижняя челюсть, оттопыренные крупные ушные раковины с мягкими хрящами, легкие признаки соединительнотканной дисплазии: суставная гипермобильность, малые аномалии развития сердца (пролапсы, дополнительные хорды). У мужчин после полового созревания — увеличенный размер яичек, высокий рост. У девочек с полной мутацией наблюдаются обычно менее выраженные нарушения, интеллектуальная недостаточность развивается у 50%. По внешним признакам диагноз далеко не всегда удается поставить. Основной метод диагностики — молекулярно-генетическое исследование (анализ ДНК).
Распространенность
Частота синдрома изучена недостаточно, с совершенствованием методов диагностики проводилась ее переоценка в сторону уменьшения. На сегодняшний день опубликованы данные о частоте 16-25 больных мальчиков на 100 000 населения. Частота носительства премутации у женщин достигает 1,7%, но данные по разным популяциям и народам значительно различаются.
Этиология
Причина болезни состоит в увеличении числа нуклеотидных повторов в промоторе гена FMR1. При этом аллели размером 5-44 повтора стабильны, т. е. число повторов в таких аллелях не увеличивается при передаче от родителей к детям. Аллели размером 45-54 в 14% случаев могут увеличиваться, но не до состояния полной мутации, а до состояния премутации. Дальнейшее увеличение числа повторов не более чем до 200 само по себе не вызывает болезнь, но предрасполагает к болезни у потомства (так называемая премутация). Когда повторов становится больше 200, развивается болезнь. У женщин–носительниц премутации 55-200 повторов возможны преждевременная менопауза (20%), аффективные расстройства и аномалии головного мозга на МРТ. У мужчин-носителей премутации 55-200 бывают усиливающиеся с возрастом тревожные расстройства, нарушение организующих влияний лобной коры, тремор.
Экспансия (увеличение числа) повторов происходит обычно при передаче нестабильного аллеля от матери. Незначительное увеличение может происходить при передаче от отца (иногда в таких случаях происходит и уменьшение числа повторов).
Диагностика
Современные методы молекулярной диагностики позволяют выявить как полные мутации, так и премутации. Точность определения числа повторов современными лабораторными методами составляет ±2-3. В случае полной мутации обычно выявляется соматический мозаицизм: присутствие в ДНК одного человека нескольких вариантов мутации с разным числом повторов (разница может составлять несколько сотен).
Возможно проведение пренатальной и преимплантационной диагностики.
Поскольку генетика синдрома Мартина-Белл достаточно сложна, всем носителям нестабильного варианта гена и их родственникам рекомендована консультация генетика для уточнения риска рождения ребенка с синдромом Мартина-Белл.
Статью подготовил: Екатерина Померанцева, к.б.н., врач-генетик, зав.лабораторией Genetico
Литература:
FMR1-Related Disorders. Robert A Saul, MD, FACMG and Jack C Tarleton, PhD, FACMG. https://www.ncbi.nlm.nih.gov/books/NBK1384/
“fragile X syndrome”. Genetics Home Reference. https://ghr.nlm.nih.gov/condition/fragile-x-syndrome
National Fragile X Foundation https://www.fragilex.org
FRAXA Research Foundation https://www.fraxa.org
Генетические особенности синдрома ломкой Х-хромосомы https://genetico.ru/stati/geneticheskie-osobennosti-sindroma-lomkoy-h-hromosomyi.html
Источник
Автор Предложить Статью На чтение 6 мин. Опубликовано 15.05.2015 11:44
Обновлено 04.03.2018 20:52
Синдром Мартина-Белл — заболевание генетического происхождения. Основными звеньями патологического процесса при синдроме Х-ФРА на молекуляном уровне является экспансия нестабильного тринуклеоидного повтора CGG (в первом экзоне гена FMRI (fragile X mental retardation I) или метилирование CpG-островка этого гена и подавление экспрессии FMRP-белкового продукта гена FMRI. В последних работах попытки коррелировать поведенческий фенотип, экспрессию FMR1 протеина и траекторию психического развития мальчиков с синдромом Х-ФРА не продемонстрировали взаимосвязь между поведением и FMR1 (Bailey D.B. ct al., 2001). Таким образом, патофизиологическая роль мутации FMR1 и ее отношение с фенотипом аутизма остается неопределенной (Rogers S.J. et al., 2001).
Фото: Синдром Мартина-Белл
Ко второму направлению изучения атипичного аутизма, относится исследование синдрома Мартина-Белл в рамках аутистических расстройств при генетически обусловленной хромосомной патологии. Данная патология привлекает к себе внимание в связи с тем, что по данным разных авторов аутизм при Х-ФРА встречается достаточно часто — от 15-25% до 50 — 90% случаев, является аутистическиподобным по мнению В.М. Башиной (1999), наиболее выражен и приближается к классическому аутизму.
Синдром Мартина-Белл — распространенность
Распространенность синдрома Мартина — Белл среди новорожденных мальчиков составляет от 1 на 1000 до 1 на 2000.
В 1976 году J.Cantu с соавт. впервые описал клинические особенности у больных с ломкой Х-хромосомой. С этого периода постепенно увеличивается число работ, посвященных изучению поведенческого фенотипа этого заболевания, подробно описан интеллектуальный дефект, гипердинамический синдром, частично изложена шизофреноподобная симптоматика с указанием на присутствие аутизма у ряда больных при данном заболевании.
Синдром Мартина-Белл — признаки
Больным свойственен специфический психофизический фенотип и особый поведенческий фенотип.
К менее специфичным отнесены: большая голова, большие низко расположенные уши, светлые волосы и глаза. Вместе взятые они составляют «портретную» диагностику синдрома Мартина-Белл. Макроорхизм для детей не характерен и диагностического значения не имеет.
По данным И.А.Скворцова, Е.А. Селивановой, В.М.Башиной и др. (1999), первые месяцы жизни дети развиваются нормально. К полугоду проявляются симптомы аутизма с остановкой в умственном развитии: ограничивается общение, отторгается тактильный контакт с матерью, останавливается формирование глазной реакции, слежения, что сочетается с робостью, избеганием взгляда. Возникают стереотипные спонтанные регрессивные движения протопатического и более глубинного уровня с расширением набора на последующих возрастных этапах. После становления ходьбы выступает двигательная расторможенность с дефицитом внимания. К 1,5-2 годам замедляется формирование речи, возникают персеверации. Игровая деятельность также носит стереотипный характер, протекает в одиночестве, с отказом от социальных контактов с родными и сверстниками.
К особенностям аутистического поведения у этих больных авторы отнесли осциллирующий характер отрешенности на протяжении коротких отрезков времени со сменяющейся тенденцией к более полноценному общению, смягчению отрешенности. Периодически у ребенка выявляются черты примитивного, свойственного более раннему возрасту поведения, усиливаются стереотипии в моторной и речевой сферах, вплоть до полного угнетения активности. Смешения более ранних и более поздних функций не происходит, а наблюдается целостное реагирование, как бы соответствующее то более раннему, то более зрелому возрасту. Флюктуация активности остается постоянным качеством энергетического потенциала у этих лиц, выраженность ее с возрастом смягчается. Нарастают когнитивные проблемы, торпидность в мышлении. С годами умственный дефект имеет тенденцию к утяжелению, углублению пустой аутизации с психическим опустошением, нарастающей астенией.
Синдром Мартина-Белл — диагностика
У больных детей с синдромом Мартина-Белл отмечаются характерные изменения ЭЭГ в виде отсутствия затылочного альфа-ритма при доминировании в лобно-центрально-теменных областях коры высокоамплитудной (до 160 мкВ) ритмической 0- активности частотой 5-7 Гц, занимающей от 30 до 90% записи. Этот ритм практически не подавляется при открывании глаз, в большинстве случаев отмечается его депрессия на моторные пробы. 9-активность доминирующей частоты не претерпевает существенных изменений с возрастом, остальные ритмические диапазоны изменяются. В возрастном интервале 8-11 лет возникает увеличение индекса a-активности в центральных зонах коры. Последнее связано с появлением в этих зонах сенсомоторного ритма а-диапазона.
Корреляций между картиной ЭЭГ и наличием или отсутствием симптомов аутизма при Х-ФРА выявлено не было.
Изменения, регистрируемые при Х-ФРА при проведении МРТ головного мозга, по данным И.А. Скворцова с соавт. (2003), оказались следующими: расширение ликворных пространств (главным образом — боковых желудочков мозга, преимущественно в области задних рогов, но также третьего и четвертого желудочков, субарахноидальных пространств и окружности ствола мозга и мозжечка), выраженное изменение плотности перивентрикулярного белого вещества как в больших полушариях, так и в мозжечке, атрофия коры мозга, преимущественно в передних отделах лобных и височных долей.
При исследовании синдрома экспансии тринуклеотидных цитогенными основаниями ДНК динамической мутации изменяется не качество, а количество нуклеотидных повторов. При превышении некоторого нормального числа Мартина-Белл был открыт феномен повторов (триплета, образованного цитозин-гуанин-гуанин (СГГ). При тринуклеотидных повторов в гене возникает мутация, приводящая к заболеванию. У нормальных индивидуумов число CGG-повторов в X-хромосоме колеблется от 2 до 54. Увеличение длины повтора до 200-230, не сопровождающееся клиническими проявлениями, называется премутацией. Дальнейшая экспансия повтора, свыше 230 копий, является полной мутацией и обычно сопровождается клиническими проявлениями синдрома Мартина-Белл. Переход от состояния премутации к полной мутации происходит только при передаче гена от матери. Экспансия CGG-повторов зависит от пола потомков: она увеличена при передаче от матери к сыну в большей мерс, чем при передаче от матери к дочери.
Экспансия триплетов является постзиготическим событием и происходит на ранних стадиях эмбриогенеза. Поэтому так необходима своевременная пренатальная диагностика данного заболевания путем исследования околоплодных вод или ворсинок хориона начиная с 12,5 недели развития, что дает возможность определить как аномальное расположение триплета CGG в гене FMR1, так и гиперметиляцию его островка CpG. К указанным диагностическим возможностям в настоящее время добавляется возможность дозачаточной или доимплатационной диагностики, при которой техника основывается на генетическом исследовании эмбрионов оплодотворенных in vitro, выборе и перенесении в матку тех из них, которые не подвержены ни мутации, ни премутации для принятия решения о прерывании беременности в случае подтверждения диагноза.
Необычность наследования синдрома Мартина-Белл заключается в том, что не все, а лишь 80% мужчин, носители мутантного гена, имеют клинические и цитогенетические признаки заболевания. Оставшиеся 20% как клинически, так и цитогенетически нормальны. Однако после передачи мутации своим дочерям, они могут иметь пораженных внуков. Такие мужчины названы трансмиттерами передатчиками неэкспрессированного мутантного гена. Наряду с этим, в литературе были описаны 2 типа женщин — гетерозиготных носительниц гена фрагильной Х-хромосомы. Первый тип — дочери нормальных мужчин-трансмиттеров, не имеющие синдрома Мартина-Белл и ломкой Х-хромосомы при цитогенетическом обследовании. Второй тип — внучки нормальных мужчин-траисмитгеров, а также родные сестры пораженных мужчин, обнаруживающие клинические признаки заболевания до 35% случаев.
Применение метода сокращенного трехгруппового анализа мальчиков с Х-ФРА, мальчиков с аутизмом и мальчиков как с Х-ФРА, так и с аутизмом показало, что дети с сочетанием Х-ФРА и аутизма оказались значительно более замедлены в развитии, чем дети только с аутизмом или только с X-ФРА.
Синдром Мартина-Белл — лечение
На сегодняшний день, лечения синдрома Мартина-Белла нет.
Источник
