Синдром некомпактного миокарда левого желудочка

Некомпактный миокард левого желудочка (синонимы: губчатый миокард, эмбриональный миокард, персистирующие синусоиды) — генетически детерминированная кардиомиопатия, которая характеризуется патологической трабекулярностью миокарда левого желудочка в результате нарушения нормального эмбриогенеза сердца с формированием двух слоев миокарда: толстого некомпактного (эндокардиального) и тонкого нормального (компактного, эпикардиального).
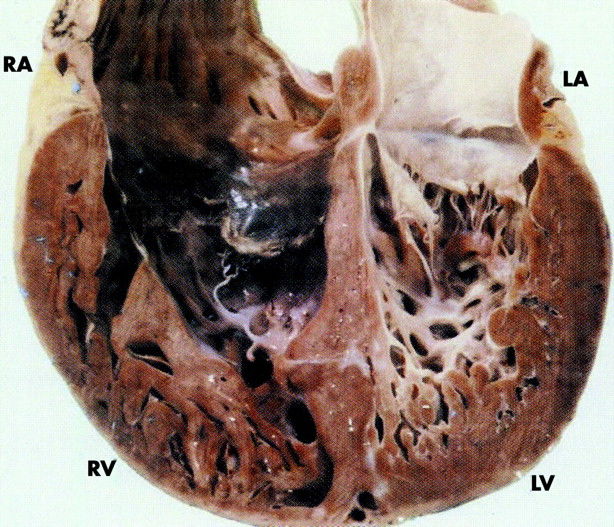
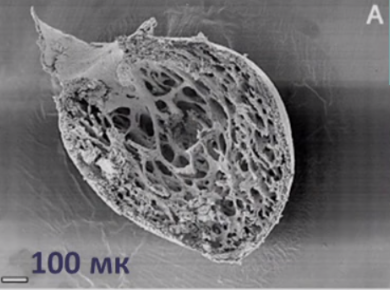
Рис. 1. Макропрепарат сердца.
Визуализируется выраженная трабекулярность миокарда левого желудочка, отграниченная с нормальным слоем.
Код по МКБ-11
BC44 Noncompaction cardiomyopathy
Историческая справка
Первые упоминания губчатого миокарда описаны американским хирургом Самуэлем Беллетом в 1932 году: в миокарде левого желудочка новорожденного с цианотическим врожденным пороком сердца отмечались глубокие лакуны и трабекулы, выявленные при аутопсии. Далее, лишь с развитием и внедрением эхокардиографии (далее ЭхоКГ), в 1984 году немецкие ученые Рольф Энгбердинг и Франц Бендер описали наличие синусоид миокарда у пациента, характерные лишь для эмбрионального этапа развития сердца. В 1990 году детский кардиолог и американский профессор кафедры педиатрии вместе с соавторами предложил термин «изолированная некомпактность миокарда левого желудочка». Учитывая все большее внедрение в практику ЭхоКГ, описывалось множество случаев данной нозологии, и в 1995 году Всемирная организация здравоохранения включила данное заболевание в группу неклассифицируемых кардиомиопатий. Затем, в 2006 году, Американская ассоциация сердца отнесла данную патологию к первичным генетическим кардиомиопатиям. С 2008 года заболевание включено в группу неклассифицируемых кардиомиопатий согласно классификации Европейского общества кардиологов.
Эпидемиология
Распространенность заболевания среди взрослого населения составляет 0,014%. Встречается: у 0,01-0,27% всех взрослых пациентов, направленных на ЭхоКГ; у 3% больных из 960 с признаками ХСН; у 100 пациентов из 36933, перенесших ЭхоКГ (в период с 1994-2006 гг). По данным разных ученых, заболевание чаще встречается у мужчин (56–82 %). В детской практике из всех случаев кардиомиопатий некомпактный миокард встречается в 9,2%, занимая третье место после гипертрофической КМП и дилатационной КМП.
Эмбриональное развитие миокарда
Для наиболее точного понимания механизма образования некомпактного слоя миокарда обратимся к эмбриологии. Миокард развивается из миоэпикардиальной пластинки спланхнотома мезодермы, представляя собой сеть волокон, разделенных широкими полостями. С 5-й недели эмбрионального развития происходит уплотнение сети волокон, сужение межтрабекулярных лакун, формируется коронарный кровоток, происходит процесс уменьшения межтрабекулярных пространств до размеров капилляров. Миокард «компануется» от основания к верхушке, от эпикарда к эндокарду (рис. 1, 2, 3, 4). При нарушении данного процесса, чаще всего в результате генетической мутации в генах, кодирующих белок таффазин, альфадистробеверин, гетерозиготные мутации в генах, кодирующих MYH7, ACTC, TNNT2, в сердце остаются зоны некомпактного миокарда с глубокими межтрабекулярными пространствами.
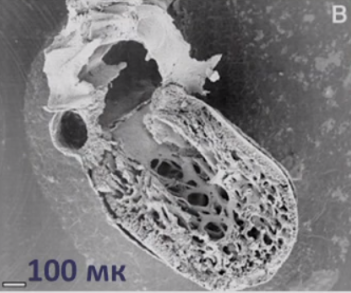
Рис. 2. Эмбриогенез сердца, 6 неделя развития.
Heart Fail Clin. Author manuscript; available in PMC 2009 July 2
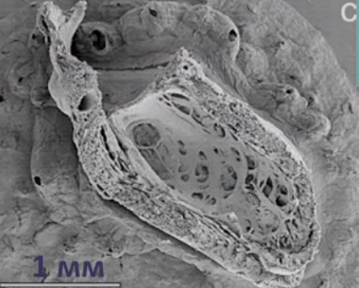
Рис. 3. Эмбриогенез сердца, 12 неделя развития.
Heart Fail Clin. Author manuscript; available in PMC 2009 July 2
Рис. 4. Эмбриогенез сердца, 16 неделя развития.
Heart Fail Clin. Author manuscript; available in PMC 2009 July 2
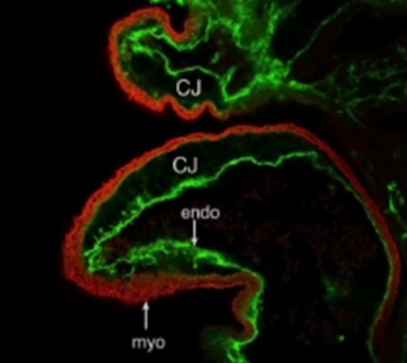
Рис. 5. Эмбриогенез сердца, трубчатое сердце.
Красный маркер тяжелых цепец миозина. Зеленый маркер эндотелия. Author manuscript; available in PMC
2009 July 2
Классификация
Большинство ученых выделяют следующие формы некомпактного миокарда:
– изолированный;
– в сочетании с врожденными пороками сердца;
– в сочетании с нейромышечными заболеваниями (метаболическая миопатия, синдром Barth, синдром Roifman, синдром Ohtahara, синдром Noonan, мышечная дистрофия Emery–Dreifuss, мышечная дистрофия Becker, синдром Melnick–Needles).
По форме возникновения:
– спорадическая;
– семейная (30%).
По анатомическим формам выделяют:
– левожелудочковая;
– правожелудочковая;
– бивентрикулярная.
По морфологическим типам:
– лакунарный;
– губчатый;
– смешанный.
По степени некомпактности миокарда (по отношению толщины слоя некомпактного миокарда к толщине всей стенки сердца на уровне верхушки левого желудочка):
– мягкая (0,33–0,26)
– умеренная (0,25–0,20)
– тяжелая (менее 0,2)
Патогенез и клиника
Патогенез складывается из сердечной недостаточности, синдрома нарушений ритма, тромбоэмболического синдрома.
Сердечная недостаточность выходит на ведущее место в клинике данного заболевания. Из-за нарушенной архитектоники строения миокарда происходит нарушение его сократительной способности. При тяжелой степени некомпактности клиническая картина данного синдрома наиболее выражена с преобладанием недостаточности по обоим кругам кровообращения и с выраженным снижением общей сократительной способности миокарда. Как правило, у некоторых пациентов клиника заболевания может манифестировать в результате запуска воспалительного процесса в миокарде, а в ряде случаев, при благоприятном течении, некомпактный миокард можно выявить впервые у лиц пожилого возраста. В клинической картине заболевания на первое место может выходить болевой синдром, который выражается приступами стенокардии. Это объясняется большей потребностью в кислороде некомпактного слоя миокарда, который не кровоснабжается основными ветвями коронарных артерий, а кровоснабжение его происходит непосредственно из полости левого желудочка.
Синдром нарушений ритма проявляется чаще всего желудочковыми нарушениями ритма — более чем в половине случаев (экстрасистолия, нередко и высоких градаций). В четверти случаев наблюдается фибрилляция предсердий. Также, вследствие эндомиокардиального фиброза с захватом проводящей системы сердца наблюдаются нарушения проводимости по типу АВ, СА-блокад.
Конечно же, нарушение глобальной систолической функции, наличие нарушений ритма сердца, а в частности фибрилляции предсердий, наличие глубоких лакун предрасполагает к образованию тромбов в полости левого желудочка, а отсюда и тромбоэмболических осложнений (кардиоэмболические инсульты, ТИА, мезентериальный тромбоз).
Диагностика
Клиника при данном заболевании неспецифична, она может маскировать и дебют ИБС, и прочие кардиомиопатии. В данном случае нам помогает ЭхоКГ и МРТ с контрастированием гадолинием, помимо стандартной ЭКГ и суточного мониторирования ЭКГ.
Выделяют следующие эхокардиографические критерии некомпактного миокарда:
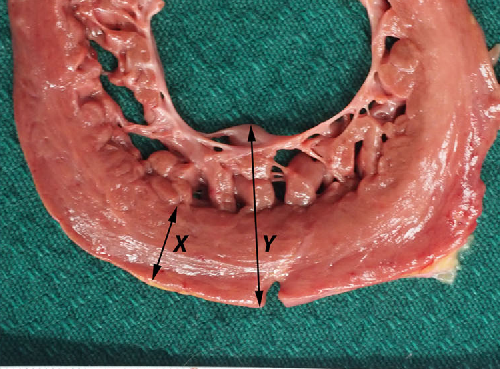
- Критерий Chin, 1990. Отношение компактной (X) части миокарда к общей толще миокарда (Y) ≤ 0,5.(рис.6) Измерение проводится в конце диастолы из парастернальной проекции по короткой оси и верхушечной проекции;
- Критерий Jenni, 2001. Измеряется в конце систолы из парастернальной позиции по короткой оси левого желудочка. Отмечается отношение некомпактной части миокарда к компактной более 2; визуализируются многочисленные выступающие трабекулы с глубокими межтрабекулярными пространствами, между которыми при цветовом доплере выявляется кровоток;
- Критерий Stollberger, 2007. Наличие более 3 трабекул в левом желудочке в направлении от верхушки к папиллярным мышцам, визуализирующиеся одновременно в одной эхокардиографической позиции; выявление кровотока в межтрабекулярных пространствах при цветном доплере;
Так же проводится оценка всех стандартных параметров при ЭхоКГ (размеры полостей, наличие изменений сократительной способности, клапанная недостаточность, оценка фракции выброса).
МРТ проводится с контрастным усилением редкоземельного металла гадолиния, оценивается: ФВ ЛЖ, индексированная масса миокарда (компактного, некомпактного); число некомпактных сегментов; критерий некомпактности (чувствительность 86%, специфичность 99%: соотношение компактного и некомпактного слоя миокарда в диастолу более 1:2); индекс ремоделирования левого желудочка.
И, конечно же, не стоит забывать о генетическом картировании и биопсии миокарда.
Рис. 6. Макроскопический срез задней стенки левого желудочка.
Принципы и тактика лечения.
Пациентам с бессимптомным течением специфической терапии не требуется, им нужно лишь динамическое наблюдение у врача кардиолога. При наличии клиники лечение должно складываться из следующих составляющих: стандартная терапия ХСН; назначение антикоагулянтной терапии при необходимости (снижение ФВ, ТЭ в анамнезе, тромбоз полостей сердца); назначение, при необходимости, антиаритмической терапии; назначение иммуносупрессивной терапии при доказанности аутоиммунного повреждения миокарда. Так же, в отдельных случаях, могут рассматриваться варианты установки ЭКС (при наличии блокад высоких градаций с эпизодами синкопе); установки кардиовертера-дефибриллятора (при плохом терапевтическом ответе на антиаритмики); трансплантации сердца.
Источники
- Диагноз при сердечно-сосудистых заболеваниях (формулировка, классификация) / С.Г. Горохова. – 4-е изд., перераб. и доп. – М.: ГЭОТАР-Медиа, 2018.-стр. 192-193
- Басаргина Е. Н., Гасанов А. Г. Некомпактный миокард левого желудочка у детей-редкая кардиомиопатия? //Российский вестник перинатологии и педиатрии. – 2010. – Т. 55. – №. 4.
- Голухова Е. З., Шомахов Р. А. Некомпактный миокард левого желудочка //Креативная кардиология. – 2013. – №. 1. – С. 35-45.
- ICD-11 (Mortality and Morbidity Statistics). https://icd.who.int/browse11/l-m/en
Нашли опечатку? Выделите фрагмент и нажмите Ctrl+Enter.
Источник
Некомпактный миокард левого желудочка (НМЛЖ) относят к редким формам кардиомиопатии, имеющим генетическую обусловленность. Характерной особенностью патологии является наличие губчатого строения одного из двух стенок миокарда.
Гипертрабекулярный слой ЛЖ обращен к его полости, у которого снижена сократительная способность. Нарушения закладываются во время эмбрионального развития.
Клинические признаки заключаются в проявлении сердечной недостаточности, тромбоэмболического синдрома и нарушениях сократительной ритмики. Специфического лечения на данный момент нет, пациентам с терминальной стадией показана трансплантация сердца.

Некомпактный миокард
Эпидемиология и классификация
Болезнь регистрируется как в детском, так и во взрослом возрасте. Наследственное происхождение аномалии подтверждается у 18–20% совершеннолетних и у 40–50% детей соответственно.
Распространённость в последнем случае выше – около 1,3% от общей популяции маленьких пациентов, у взрослых встречаемость заболевания ниже – 0,014 %. Однако важно понимать, что приведенная статистика должна считаться относительной, поэтому истинные цифры могут быть более значимыми.
Важно. Некомпактный миокард левого желудочка у лиц мужского пола диагностируется чаще – 55-80% от числа всех зарегистрированных случаев.
Патология формируется в период эмбрионального развития, во время образования пластов миокарда у плода. Главным признаком аномалии является развитие глубоких трабекул в ЛЖ и межжелудочковой перегородке, что негативно отображается на систолической способности сердечной камеры. У некоторых больных болезненный процесс может затрагивать и ткани правой стороны сердца.
Аномалия может иметь как спорадический, так и семейный характер. Последняя выявляется значительно чаще, поэтому болезнь классифицируют как ту, которая имеет наследственную предрасположенность.
В то же время ряд специалистов отмечают, что патологию можно считать и назальной формой, поскольку это может быть вторичным следствием других кардиологических болезней. В настоящее время данный вопрос остается дискуссионным.
Этиология
Есть несколько гипотез, объясняющих причины формирования заболевания.
Обобщая полученные научные данные, можно выделить две основные формы:
- Эмбриональная – заболевание обуславливается генными процессами (наследственность или мутагенез), что приводит к формированию неправильного (губчатого) строения миокарда левого желудочка и его межсердечной перегородки. Это объясняется мутированием цистрона G4.5, кодирующего образование таффазина. Патологии сцеплена с полом, т. е. наследуется с Х хромосомами. Кроме этого, описаны мутации других генов, например, α-дистробревина и транскрипционного фактора NKX 2.5.
- Гипотеза функциональной дезадаптации, как вероятные изменения при развитии кардиомиопатии. Данная теория не обуславливается генными изменениями во время внутриутробного развития плода. Мнение подкрепляется зарегистрированными факторами, когда синдром НМЛЖ у взрослых больных не регистрировался на более ранних обследованиях при ультразвуковом обследовании сердца.
Заметка. Заболевание может наследоваться с половыми Х-хромосомами по рецессивному типу. Это означает, что женщины (даже не являющиеся больными) могут иметь в геноме и передавать по наследству НМЛЖ. Например, вероятность того, что мальчики, рожденные ими, будут иметь мутационный ген составляет примерно 50%. Все дочки такой матери не будут больными, однако, каждая вторая девочка станет носительницей опасного гена.
Чреспищеводная эхокардиограмма, цветное допплеровское картирование: межтрабекулярные пространства, сообщающиеся с полостью ЛЖ
Симптоматика и диагностика
Клиническая картина разнообразна, зависит от степени поражения и уровня патогенеза. Довольно часто первые признаки уже заметны в детском возрасте.
На болезнь указывает:
- возникновение и усугубление признаков сердечной недостаточности;
- патологические изменения иннервации;
- ненормальные изменения, связанные с сократительной деятельностью и ритмикой;
- систолическая дисфункция левого желудочка;
- гипертрофическая и рестриктивная кардиомиопатия;
- появление некоторых симптомов синдрома Барта;
- тромбообразование в трабекулярной зоне и возникновение осложнений;
- мышечная дистрофией Беккера (случается редко);
- неожиданная клиническая смерть, как итог заболевания.
Поскольку указанные признаки свойственны другим кардиологическим заболеваниям, диагностика часто бывает достаточно затруднена. Основные методы обследования обозначены в таблице и на закрепленном в статье видео.
Таблица. Способы диагностики некомпактного миокарда левого желудочка:
| Метод | Характеристика |
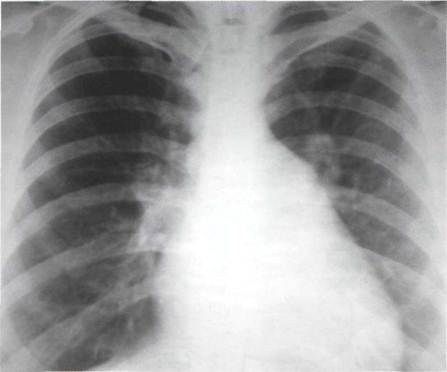
Рентген | Помогает визуализировать на фото наличие аномальных изменений в сердце. |
ЭхоКГ | Другое название – УЗИ сердца. Является основным методом обследования состояния миокарда, показания обследования становятся основой для постановки диагноза. |
МРТ и КТ | Томографии несмотря на хороший уровень визуализации сердечных структур при губчатом миокарде на данный момент применяются не часто. |
Вентрикулография левого желудочка | Контрастное рентгенологическое обследование полостей сердца, показывает аномальные изменения морфологических структур. |
Диагностическую ценность в данном случае имеют исследования, позволяющие визуально оценить состояние сердца. Главный признак, на которой обращают внимание клиницисты при верификации заболевания это наличие глубоких трабекул в миокарде ЛЖ или межсердечной перегородке.
Как правило, аномалии локализуются на верней половине органа, а также на боковой и нижней стенках левого желудочка.
Основным и наиболее информативным диагностическим методом является ультразвуковое обследование сердца (ЭхоКГ), которое показывает:
- изменение величины стенок желудочка;
- выступы ЛЖ в сердечные полости;
- наличие трабекул;
- соотношение некомпактного слоя к истинному миокардиальному;
- межтрабекулярные синусы, а также характер кровотока в измененных полостях можно хорошо увидеть на цветной доплерографии;
- наличие других патологий.
Повышенная трабекулярность миокарда левого желудочка
МРТ позволяет получать снимки высокого качества с более четкими контурами. На них видны субэндокардиальные дефекты перфузии.
Диагностическую ценность несет ситуация, когда некомпактный слой миокарда превышает компактный в 2,3 или более раз. При наличии трабекул изменяется кровоток, что представляет повышенную вероятность образования тромбов и осложнений, связанных с ними. Завихрения и изменения кровотока хорошо можно визуализировать при доплерографии.
МТР, как и КТ – это современные и достаточно высокоинформативные диагностики, однако, пока их нужно относить к перспективным методикам обнаружения некомпактного миокарда левого желудочка. На данный момент в медицинской литературе встречается достаточно мало описания критериев томографической диагностики рассматриваемого симптома.
Сегодня МРТ и КТ остаются методами выбора, как средства лучшей визуализации, когда иные диагностические процедуры не позволяют точно выяснить патологические изменения в сердце.
Вентрикулографию или коронарографию показано делать всем пациентам с подозрительными клиническими проявлениями, чей возраст выше 30 лет. Это помогает дифференцировать болезни и исключить аномалии венечных артерий.
Лечение
Специфическая терапия синдрома НМЛЖ на данный момент отсутствует и в ближайшее время медицина не сможет найти адекватное этиотропное лечение.
В основном назначается симптоматическая терапия для устранения или облегчения клиники:
- хронической сердечной недостаточности;
- нарушений сердечной ритмики;
- профилактические мероприятия против образования тромбов и всевозможных осложнений, которые с ними связаны.
В определенных случаях эффективным может быть оперативное вмешательство. Тем не менее добиться успешного результата можно только при помощи трансплантации сердца.
В некоторых источниках можно найти информацию об успешной пересадке левого желудочка. При злокачественных синдромах показана имплантация кардиовертера-дефибриллятора.

Губчатый миокард левого и правого желудочков на снимке МРТ
Прогноз
В общем прогноз является неблагоприятным. По статистике смертность в течение семилетнего периода составляет от 22 до 50%.
Основные причины летальных исходов состоят в патологии ритмики сердца или усугубленной недостаточности. Среди детей уровень смертности ниже и составляет около 18%.
Тут многое будет зависеть от уровня аномальных сегментов, того насколько функционально активен миокард (его сократительная способность), времени появления негативной клиники и скорости ее прогрессирования.
Заключение
Прошло более двадцати лет с момента описания синдрома некомпактного миокарда левого желудочка, однако, на сегодня нет четких регламентаций насчет диагностики, терминологии и классификации патологии. Не являются корректными методы исследования и верификации болезни, поэтому часто ее неверно трактуют и лечат.
В то же время высокие риски летальных исходов при НМЛЖ диктуют необходимость раннего обнаружения и высокой дифференциации диагноза. Верный подход к лечению позволит подбирать адекватную консервативную или радикальную терапию, что улучшит общие прогнозы и продолжительность жизни.
Тайное Слово: Артерия
Рекомендуем статьи по теме


Источник