Синдром приобретенного иммунодефицита это мутация
СПИД (AIDS) — инфекционное заболевание, которое вызывается вирусом иммунодефицита человека (ВИЧ). Диагноз ВИЧ-инфекции устанавливается при обнаружении антител к вирусу, вирусных антигенов, вирусной РНК или ДНК или при выделении культуры вируса.
Несмотря на огромные финансовые средства, потраченные в последние годы на борьбу с этим заболеванием, проводимые мероприятия пока не принесли ожидаемых результатов. Некоторый успех достигнут — в масштабе планеты эпидемическая ситуация стабилизируется, количество новых случаев ВИЧ-инфекции снизилось. Хотя эта болезнь перешла из смертельных заболеваний в разряд медленно текущих, управляемых инфекций, смертность во всем мире от СПИДа и связанных с ним болезней всё ещё остаётся высокой.
История открытия вируса и происхождение заболевания
Сидром приобретённого иммунодефицита впервые был зарегистрирован и описан в 1981 году в США. В 1984 – 1985 году была установлена этиологическая роль вируса иммунодефицита человека. Вирус был выделен двумя группами ученных независимо друг от друга: Люком Монтанье (Франция, Montagnier L. et al.) и Робертом Галло (США, Gallo R. C. et al.).
Выявлено несколько основных типов ВИЧ: ВИЧ-1 широко распространён во всём мире, ВИЧ-2 обнаруживается преимущественно в Западной Африке. Основной причиной пандемии СПИДа в мире стал ВИЧ-1; этот вирус и был впервые выделен исследовательскими группами. ВИЧ-2 — менее вирулентный вирус, и, хотя он встречается в мире повсюду, широкое распространение его отмечено только в Африке. Вирусы имеют принципиальную общность структуры вириона и генома, однако значительно (до 25% генома) различаются последовательностями РНК и белков.
Вирус ВИЧ сходен с некоторыми вирусами обезьян, поэтому многие учёные предполагают, что он возник в результате изменчивости этих вирусов и был занесён в популяцию человека извне относительно недавно. ВИЧ-2 более близок к вирусам иммунодефицита обезьян и может заражать многие виды приматов, не вызывая при этом симптомов иммунодефицита. ВИЧ-1 заражает только человека и шимпанзе.
Вопрос о том, когда и каким образом произошло попадание инфекции в популяцию человека, остается невыясненным. Вирус ВИЧ существовал в Центральной Африке (Заир) до 1960 года, что было установлено с помощью ретроспективных исследований коллекций сывороток крови. Он был занесён на Гаити до середины 70-х годов и в США до 1978 года. Иначе говоря, его истоки лежат в Африке, где в некоторых странах вирусоносители составляют до половины населения, хотя заболевание СПИД проявляется далеко не у всех. К 90-м годам XX-го века СПИД был зарегистрирован во всех странах мира.
Различные штаммы вируса ВИЧ, выделенные в разных районах Африки, Карибского бассейна и США, были секвенированы.
Пути заражения
Источником инфекции являются инфицированные люди во всех клинических стадиях, включая инкубационный период. ВИЧ содержится в большой концентрации не только в крови, но и в первую очередь в сперме, а также в менструальных выделениях и вагинальном (цервикальном) секрете. Кроме того, ВИЧ обнаруживается в грудном молоке, слюне, слезной и цереброспинальной жидкости, в биоптатах различных тканей, поте, моче, бронхиальной жидкости, кале. Наибольшую эпидемиологическую опасность представляют кровь, сперма и вагинальный секрет, грудное молокоимеющие достаточную для заражения долю инфекта.
Заражение человека ВИЧ происходит при попадании вируссодержащего материала непосредственно в кровь или на слизистые оболочки.
На данный момент выделяют следующие пути инфицирования ВИЧ:
- незащищенный половой контакт
- заражение плода и новорожденных при беременности и родах (от ВИЧ-инфицированных матерей)
- от матери ребёнку при вскармливании грудным молоком
- инъекционная наркомания
- инфицирование при медицинских манипуляциях
- при переливании крови и ее компонентов
Вирус иммунодефицита человека (ВИЧ)
Вирус иммунодефицита человека (ВИЧ; HIV) принадлежит к семейству ретровирусов — сложных РНК- геномных вирусов, образующих с помощью обратной транскриптазы ДНК-копию генома, которая, интегрируя с геномом хозяина, вызывает интегральную инфекцию.
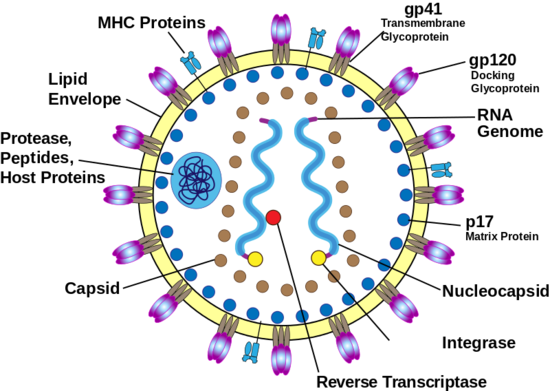
Вирус поражает клетки иммунной системы. В результате работа иммунной системы угнетается и развивается синдром приобретённого иммунного дефицита (СПИД), организм больного теряет возможность защищаться от инфекций и опухолей.
Вирус инфицирует Т-лимфоциты класса хелперов. Вирусная частица присоединяется к Т-рецептору на наружной поверхности мембраны Т-хелпера, липидная оболочка вируса сливается с клеточной мембраной, и содержимое вирусной частицы оказывается в цитозоле. Инфицированные вирусом Т-хелперы постепенно гибнут из-за разрушения вирусом, апоптоза или уничтожения Т-киллерами.
В норме в 1 мл крови содержится около 1000 Т-лимфоцитов. У лиц, инфицированных ВИЧ, их содержание снижается в процессе развития инфекции. Когда количество Т-лимфоцитов уменьшается в 4-5 раз (через 7-10 лет после инфицирования), появляются явные и тяжелые симптомы недостаточности иммунной системы.
Организм уже не в состоянии противостоять возбудителям оппортунистических инфекций, которые неопасны или малоопасны для здоровых людей с нормально функционирующей иммунной системой. Главные из них — вирусные, грибковые и бактериальные инфекции (часто — туберкулез), а также злокачественные опухоли (часто — саркома Капоши, форма рака кожи). В отсутствие антиретровирусной терапии смерть пациента наступает не в результате размножения вируса, а по причине развития заболеваний, вторичных по отношению к ВИЧ-инфекции.
Строение и размножение ВИЧ
ВИЧ содержит РНК, которая служит матрицей для синтеза ДНК (ретровирус); фермент, необходимый для такого синтеза — обратная транскриптаза, — также содержится в вирусной частице. Образующаяся ДНК поступает в ядро, интегрируется с ДНК лимфоцита (при участии белков вируса) и служит матрицей для транскрипции — синтезируется вирусная РНК. В результате трансляции этой РНК образуются вирусные белки — обратная транскриптаза, белки оболочки вируса, а также регуляторные белки, стимулирующие по механизму положительной обратной связи транскрипцию и трансляцию вирусной РНК. Комплекс вирусной РНК и вирусных белков присоединяется к внутренней поверхности мембраны лимфоцита и покидает клетку вместе с частью мембраны лимфоцита, образующей липидную оболочку вируса. Размножение вируса в клетке истощает ее ресурсы, и она в конечном счете погибает.
Генетическая изменчивость ВИЧ
Ретровирусы способносы выполнять уникальную, ни у одного живого объекта более не встречающуюся реакцию — обратную транскрипцию. Обратная транскрипция, в отличие от многих других реакций матричного синтеза (например, ДНК–ДНК) — процесс, слабоподкрепленный специальными корректирующими механизмами. Репликация ВИЧ характеризуется чрезвычайно высокой частотой спонтанных мутаций.
Это означает, что всякая случайно возникшая в ходе обратной транскрипции мутация имеет большие шансы закрепиться в потомстве, что имеет важные последствия для жизни самих ретровирусов и их хозяев. В частности, одним из наиболее характерных свойств ВИЧ является его непревзойденная изменчивость (вариабельность).
Вскоре после первичного заражения, в организме инфицированного присутствует уже несколько различных вариантов ВИЧ. Большое количество вариантов ВИЧ составляет основу для его быстрой эволюции (например, в случае применения антиретровирусных препаратов), однако даже в отсутствие факторов эволюционного отбора вирус продолжает существовать в виде так называемого «роя» из близкородственных в генетическом отношении, но неодинаковых вирусов.
Генетическое разнообразие ВИЧ подкрепляется быстротой его репликативного цикла, в результате которого в организме зараженного человека ежедневно образуются миллиарды новых вирусных частиц.
Стадии ВИЧ-инфекции
При отсутствии антиретровирусной терапии можно выделить следующие стадии течения ВИЧ-инфекции:
Инфицирование —>2-3 недели—> острый ретровирусный синдром —> 2-3 недели—>исчезновение клинических симптомов + сероконверсия —>2-4 недели—>бессимптомная хроническая ВИЧ-инфекция —>в среднем 8 лет—> симптоматическая ВИЧ-инфекция/СПИД —>в среднем 1.3 года—> смерть
При проведении антиретровирусной терапии продолжительность жизни пациента может быть продлена до 70—80 лет.
Лечение ВИЧ-инфекции
При проведении антиретровирусной терапии продолжительность жизни пациента значительно увеличивается. Антиретровирусные препараты мешают ВИЧ размножаться в клетках иммунной системы человека, блокируя внедрение вирионов в клетки и нарушая на разных этапах процесс сборки новых вирионов. Своевременно начатое лечение антиретровирусными препаратами в сотни раз снижает риск развития СПИДа и последующей смерти.
Анализы на ВИЧ
В нашем центре Вы можете сдать анализ на ВИЧ-инфекцию, комплексный анализ — на сифилис, ВИЧ, гепатиты В и С, а также анализы на другие инфекции.
Источник
СИНДРОМ ПРИОБРЕТЁННОГО ИММУННОГО ДЕФИЦИТА (СПИД; англ. Acquired immune deficiency syndrome, AIDS; син. синдром приобретенной иммунной недостаточности, или СПИН) — вирусное заболевание, характеризующееся поражением системы иммунитета и развитием приобретенной, вторичной, иммунной недостаточности.
Известно, что деятельность клеток, обеспечивающих гуморальный и клеточный иммунитет, регулируется субпопуляциями Т-лимфоцитов— Т-хелперами (Т-помощниками) и Т-супрессорами. Динамическое равновесие при их взаимодействии и создает хорошо отрегулированную систему иммунного ответа на чужеродные антигены. При синдроме приобретенного иммунного дефицита поражается субпопуляция Т-хелперов, за счет чего возрастает активность Т-супрессоров и развивается иммунологическая недостаточность.
Первые случаи заболевания были выявлены в конце 70-х гг. 20 в. в Центральной Африке, в районе Ка-рибского моря и в США. Исследования по идентификации болезни начались в июне 1981 г., когда служба здравоохранения США (Центр по контролю за болезнями, Атланта, Джорджия) стала регистрировать это заболевание. Вскоре после этого случаи СПИД были зарегистрированы в европейских и других странах, а с 1983 г. данные о болезни начала публиковать ВОЗ в еженедельном эпидемиол. бюллетене.
После введения регистрации отмечается повышение показателя заболеваемости СПИД в ряде стран. К концу 1986 г. в 110 странах мира зарегистрировано 36 483 случая, в том числе 30 480 в Америке, 3732 в Европе, 1819 в Африке, 366 в Австралии и Океании, 86 в Азии. Летальность среди заболевших снизилась за последние 2—3 года с 60% до 40%. Отдельные случаи СПИД зарегистрированы в СССР. Несомненно, что рост заболеваемости в значительной мере связан с введением регистрации, однако имеются веские основания считать, что наблюдается истинный рост числа случаев СПИД и распространение его в страны с меньшим уровнем заболеваемости, а также страны, где заболевание ранее не выявлялось.
По данным Центра по контролю за болезнями (США), за 1983 г. на 100 заболевших СПИД гомосексуалисты и бисексуалисты составляли 75%, наркоманы — 13%, иммигранты из Гаити — 6%, лица, страдающие гемофилией,— ок. 1%; в остальных 5% случаев не выявлено определенных факторов риска. Мужчины составили 92,8%, женщины — 7,2% заболевших. Сходные данные получены при анализе заболеваемости в Канаде и странах Западной Европы. В США отмечается нек-рое сходство факторов повышенного риска в группах заболевших СПИД и заболевших гепатитом В, на основании к-рого можно сделать вывод о передаче возбудителей через кровь и ее препараты, а также через сперму. Необычно высокий процент гомосексуалистов среди заболевших может также свидетельствовать об иммунодепрессирующем действии спермы на мужчин. На это, в частности, указывают данные о снижении соотношения Т-хелперов и Т-супрессоров, наблюдающемся у клинически здоровых гомосексуалистов.
Поскольку среди групп повышенного риска довольно значительное место занимают выходцы из Гаити, было проведено обследование на заболеваемость СПИД населения стран Карибского моря; при этом большое число случаев выявлено на Гаити и лишь единичные случаи заболевания — на других островах Карибского моря. Естественным продолжением этих исследований были поиски СПИД в Африке, откуда предки нынешних гаитянцев в 17—19 вв. были вывезены в качестве рабов. Очаги заболевания обнаружены в Заире и других странах Центральной Африки. В отличие от США и стран Европы, где болеют преимущественно мужчины, в Африке мужчины и женщины болеют примерно одинаково часто, нередки случаи заболевания детей.
Вирусная природа СПИД установлена в 1983 г. Монтанье и Барре-Синусси (L. Montagnier, F. Barre-Sinoussi) с соавторами; вирус был выделен от больного и назван LAV (lymphadenopathy virus). В 1984 г. сходный вирус выделен Галло (R. С. Gallo) с соавторами и назван HTLV-III (human T-lymphotropic virus III) по аналогии с вирусами Т-кле-точного лейкоза (HTLV-I, HTLV-II), выделенными ранее. В этом же году вирус был выделен Леви (J. A. Levy) с соавторами и назван ARV (AIDS associated retrovirus). По рекомендации ВОЗ вирус СПИД получил обозначение ВИЧ — вирус иммунодефицита человека, по-английски — HIV (human immunodeficiency virus). Известны две серологические разновидности вируса — ВИЧ 1 и ВИЧ 2, при этом последний иммунологически близок к вирусу иммунодефицита обезьян.
ВИЧ изучен довольно подробно. Он относится к ретровирусам, и ближайшими к нему по свойствам вирусами, имеющими перекрестное серологическое родство, являются вирус инфекционной анемии лошадей, вирус оспы овец и вирус коз. Несмотря на различия биологических и частично серологических свойств штаммов, выделенных разными исследователями, все они представляют довольно однородную группу. Наряду с высокопатогенными штаммами существуют малопатогенные, к-рые обнаружены в СССР и скандинавских странах.
Цикл репродукции вирусов СПИД, по-видимому, аналогичен циклам репродукции других ретровирусов (см.). Вирионы фиксируются на поверхности чувствительных к ним клеток, проникают в клетку путем слияния мембран вируса и клетки и пиноцитоза, затем следует обратная транскрипция вирионной РНК в двунитчатую ДНК и интеграция ее в геном клетки. На матрице провируса синтезируются вирионная и субвирусные РНК, последние ассоциируются с рибосомами и кодируют синтез вирусспецифических белков. Сборка вирионов завершается на клеточных мембранах, а выход вирионов происходит путем почкования.
Вирус репродуцируется в Т-лимфоцитах, а также в макрофагах и нейроглии. Поскольку вирус оказывает цитопатическое действие на продуцирующие его Т-лимфоциты, для поддержания культуры к пассируемому материалу добавляют свежие лимфоциты либо культуру перевиваемых Т-лимфоцитов. Получены также перевиваемые культуры Т-лимфоцитов, продуцирующие вирус, но устойчивые к его цитопати-ческому действию, и сходные культуры В-лимфоцитов. Стандартные культуры продуцируют вирус в течение 3—5 дней в достаточно высоких титрах. Из животных к вирусу восприимчивы шимпанзе; у них заболевание протекает как активная персистирующая инфекция без развития лимфаденопатии и опухолей.
У людей вирус накапливается и обнаруживается в лимфоцитах и в плазме крови, а также в сперме, в слезной жидкости и слюне. Возбудитель не передается воздушно-капельным путем, т. к. концентрация вируса в слюне недостаточна. По-видимому, его проникновение в организм возможно при повреждении слизистой оболочки или кожи. Как предполагают, именно таким образом — через поврежденные слизистую оболочку и кожу, а также при половых сношениях осуществляется в основном передача возбудителя в естественных очагах заболевания Центральной Африки. В экономически развитых странах, где широко применяется гемотрансфузия, возможно введение вируса с препаратами крови. У больных гемофилией заражение может произойти через концентраты факторов крови VIII и IX.
Результаты серологических исследований, проведенных в разных странах, включая Центральную Африку, свидетельствуют о существовании легких, стертых форм заболевания и бессимптомной инфекции; однако доказана возможность заражения от лиц с бессимптомной инфекцией, в частности половым путем. Регистрируемые случаи заболевания, по-видимому, составляют лишь часть от общего числа инфицированных. При этом следует учитывать длительный инкубационный период заболевания (9—20 мес.).
В связи с существованием выраженных очагов СПИД в Центральной Африке были проведены поиски сходных вирусов у низших и человекообразных обезьян. По данным ВОЗ, у африканских зеленых мартышек и макак-резусов были обнаружены три экзогенных ретровируса: два лимфотропных вируса, названных STLV-I и STLV-III (simian T-lymphotropic viruses), и вирус, сходный с вирусом Мейсона — Пфайзера, относящийся к онкогенным типа D. Все эти вирусы были также выделены от обезьян, страдающих иммунодефицитными болезнями. Из них вирус STLV-III имеет серологическое родство с HTLV-III, хотя и отличен от последнего. Он обнаружен у здоровых зеленых мартышек, привезенных в США из Африки. В связи с этими находками исследовали на содержание ретровирусов живые вакцины против полиомиелита, к-рые готовятся с использованием почек обезьян; результаты были отрицательны. На основании сходства групп риска СПИД и гепатита В лица, привитые сериями вакцин гепатита В, приготовленных из сывороток носителей HBsAg, были проверены на присутствие антител к вирусу СПИД; результаты были также отрицательными.
Суммируя эти данные, можно предположить, что в отдаленном прошлом вирус СПИД человека произошел от сходного вируса обезьян аналогично тому, как вирус натуральной оспы — от вируса оспы обезьян. В настоящее время вирусы СПИД человека и обезьян значительно ди-вергировали. Однако вопрос происхождения вируса СПИД во многом остается не выясненным.
Распространению заболевания в первую очередь в США, а также странах Западной Европы способствовал не только приток в них выходцев из Африки, где, по-видимому, исторически образовались естественные очаги, но, что важнее, такие типичные для западного мира процессы, как половая распущенность, гомосексуализм, наркомания.
Клинические проявления заболевания разнообразны. У больных могут развиваться длительно протекающие (от 4 мес. до 4 и более лет) лимфаденопатии и лимфомы, разнообразные опухолевые поражения органов и тканей, среди к-рых доминирует саркома Капоши. Отмечаются и другие признаки болезни: продолжительная лихорадка, не поддающаяся терапии антибиотиками, длительная диарея, значительная потеря веса и истощение.
СПИД сопровождается развитием инфекций вирусной, бактериальной, грибковой или протозойной природы. Из вирусных инфекций наиболее часто наблюдаются заболевания, вызванные вирусами простого герпеса, Эпстайна — Барра, гепатита В. Отмечены поражения, обусловленные микобактериями, а также криптоспоридиями, дрожжевыми и другими грибками. Часто наблюдается пневмоцистная пневмония, вызываемая протозойным организмом Pneumocystis carinii. Перечисленные возбудители обладают относительной или даже условной патогенностью для человека. Инфекции, вызываемые этими возбудителями, развиваются на фоне иммунодефицитного состояния, поэтому их называют оппортунистическими инфекциями.
Пневмония, вызванная Pneumocystis carinii, раньше наблюдалась преимущественно у недоношенных и ослабленных детей. Вспышки пневмоцистной пневмонии возникали в родильных домах и детских яслях. При СПИД пневмоцистная пневмония протекает тяжело, плохо поддается лечению и сопровождается высокой летальностью.
Саркома Капоши раньше встречалась редко, отмечалась преимущественно у лиц старше 60 лет и протекала длительно, с ремиссиями. При СПИД саркома Капоши наблюдается у лиц моложе 60 лет, протекает быстро, характеризуется склонностью к распространению и мета-стазированию, часто сопровождается изъязвлениями с развитием гнойной инфекции и характеризуется высокой летальностью. Вместе с тем наблюдается более легкое течение болезни, завершающееся выздоровлением, или даже бессимптомная инфекция, выявляемая при серологических исследованиях (см. Иммунодиагностика).
СПИД регистрируется при наличии реально диагностируемого заболевания, к-рое возникает на фоне снижения клеточного иммунитета (напр., оппортунистические инфекции или саркома Капоши у лиц моложе 60 лет), не обусловленного данным заболеванием. В связи с открытием вируса СПИД при диагностике этого синдрома необходимо серологическое подтверждение инфекции. При отсутствии оппортунистических инфекций серологические исследования показаны в случае гистоплазмоза, изоспороза с хронической диареей, бронхиального или легочного кандидоз а, лимфомы, гистологически подтвержденной саркомы Капоши, гистологически подтвержденной хронической лимфоидной интерстициальной пневмонии, лимфоретикулеза.
Диагностика СПИД основывается на изучении клинической картины заболевания, эпидемиологическом обследовании и иммунологических и серологических тестах. При клиническом обследовании следует иметь в виду как полиморфность клинических проявлений болезни, так и наиболее часто встречающиеся оппортунистические инфекции (пневмоцистная пневмония) и опухолевые процессы (саркома Капоши).
При эпидемиологическом обследовании обращают внимание на принадлежность заболевшего к группам повышенного риска (гомосексуализм, наркомания, беспорядочная половая жизнь), а также на наличие гемофилии и гемотрансфузий в анамнезе.
Из иммунологических тестов, позволяющих обнаружить иммунодефицит, наиболее достоверным при диагностике СПИД является изменение соотношения Т-хелперов и Т-супрессоров (в норме 1,76—2,1), к-рое у больных СПИД составляет менее 1 за счет уменьшения числа Т-хелперов. Для этих исследований применяют моноклональные антитела. Меньшую диагностическую ценность имеют такие признаки, как сниженная чувствительность лимфоцитов к действию митогенов — фитогемагглютинина и конканавали-на А (тесты на бластотрансформацию), наличие стойкой лимфопении (менее 1000 лимфоцитов в 1 мкл крови), не поддающейся лечению стимуляторами лимфоцитопоэза.
Поскольку инкубационный период заболевания продолжительный, антитела к вирусу появляются уже в течение этого периода, а интеграция генома вируса в геном Т-лимфоцитов приводит к продукции вируса клетками при наличии в сыворотке крови антител. По этой же причине у больных могут образовываться комплексы антиген — антитело. Поэтому тест-системы первого поколения (им-му ноф люо ресценция, иммунофермент-пый анализ) направлены на обнаружение в сыворотке крови антител к вирусу СПИД. Наиболее удобен метод иммуноферментного анализа и соответствующие тест-системы в виде плашек с ячейками, в к-рых адсорбирован инактивированный вирус. Разрабатываются также тест-системы, основанные на получении вирусных антигенов с помощью методов генетической инженерии (экспрессируемые рекомбинантные ДНК, содержащие гены вируса).
Необходимо, однако, иметь в виду, что иммуноферментный анализ может давать ложные положительные результаты. Поэтому необходимы повторные исследования положительных образцов с применением более точных методов исследования, напр, электрофоретического разделения белков вируса (иммуноблота).
Для обнаружения вируса СПИД в лимфоцитах применяются методы ДНК — ДНК- и ДНК — РНК-гиб-ридизации с использованием клонов плазмид, несущих отдельные гены или весь геном вируса. В связи с тем, что плазмиды, содержащие полный геном, инфекционны, использование их требует соблюдения мер и редоеторожности.
Лечение больных с клинически выраженными формами СПИД проводят в стационаре. Специфических методов лечения заболевания пока не существует, хотя были испытаны без особого успеха аномальные нуклеотиды; эффективным оказался азидотимидин — ингибитор обратной транскрипции. Из средств патогенетической терапии используют интерферон , иитерлейкин-2, Т-активии и другие стимуляторы (см. Иммунотерапия). При вторичных инфекционных и паразитарных заболеваниях п рименяют соответствующие средства (антипротозойные, антибак-тери а льны е, и ротивогрибковые и ре-параты), к-рые, однако, в этих с луча ях ма лоэффективны.
Прогноз чаще неблагоприятный. Во многих случаях заболевание за-к а н ч и в а етс я л ет а л ьн ым и с х о до м.
Профилактика основана на активной сан.-просвет, работе среди населения, борьбе с половой распущенностью и половыми извращениями. Указом Президиума Верховного Совета СССР от 25 августа 1987 г. «О мерах профилактики заражу н”п вирусом СПИД» определен линя ‘о:, мед. освидетельствования * i:,;** выявления зараженных ви-рл*<»ч СПИД. 29 августа 1987 г.
М3 СССР изданы «Правила медицинского освидетельствования на выявление заражения вирусом СПИД». Согласно этим правилам освидетельствованию подлежат: доноры крови и других биол. жидкостей и тканей; советские i |>аж.ыш возвращающиеся из зарубежны v командировок продолжительностью св. 1 мес.; лица, к-рым и { и hjo шлись множественные перед ш ши i крови и ее препаратов; лиц,! р и шщие наркоманией, занимай щш ся проституцией, гомосексуалисты; советские граждане и иностранцы, имевшие контакты с больными СПИД или вирусоноснте-лями, выявленные врачом-эпидемпо-логомпри сборе эпидемиол. анамнеза, и нек-рые другие группы лиц.
Обследование на выявление заражения вирусом СПИД может пройти каждый изъявивший такое желание. Целесообразно также обследование больных оппортунистическими инфекциями, лимфаденопатиями, саркомой Капоши и другими проявлениями, характерными для СПИД.
Больные и лица, у к-рых результаты серологических исследований на СПИД положительны, подлежат диспансерному наблюдению в кабинетах инфекционных заболеваний поликлиник и обследованию методом иммуноферментного анализа 2 раза в год. Лиц, контактировавших с больным, обследуют с помощью этого метода; лиц, у к-рых результат исследования положительный, обследуют повторно через 6 мес., при отрицательном результате наблюдение прекращают.
Медработники, имеющие дело с препаратами крови, а также жидкостями и выделениями, должны принимать меры личной профилактики (работа в перчатках, текущая дезинфекция). Важнейшее значение имеют правильная стерилизация мед. инструментов, широкое внедрение в клин, практику игл. шприцов и систем для переливания одноразового пользования.
Библиогр.: Балаян М. С. Приобретенный имму но дефицитный синдром, Клин, мед., т. 62, Л!» 9, с. 8, 1984, библиогр.; В о р о б ь е в А. П. и др. Приобретенный иммунодефицит г принцип «один донор — один ()(*.»i’is*‘ii». Тер. арх., т. 57, Л* 7, с. 3, 1985, Пни, iii .• j» ; Ф а р б e р Н. А. Синдром приобрел ьн,чо иммунодефицита, Вопр. вирусол., т ’и, До 1, с. 9, 1985, библиогр.; В а г г Г‘->- i n о ussi F. а. о. Isolation ol а mpliotropic retrovirus from a patient <Л n-k юг acquired immune deficiency syndic ’ * < UDS), Science, v. 220, p. 868/ 19S t.allo R, C. a. o. Frequent detect]-»^ isolation of cytopathic retrovirus ; ilTLV-III) from patients with AIDS «>* f ,»f risk for AIDS, ibid., v. 224, p. 500. 1‘1.4 i. Levy J. A. a. o. Isolation of lympt.. „ b/pathic retroviruses from San France << patients with AIDS, ibid., v. 225, p. n<<!; Montagnier L. AIDS priority, V.tuio (Lond.), v. 310, p. 446, 1984; M n «* – i и ц M. A. a. o. Nucleic acid struelui-’ »t*«1 expression at the human AIDS Kim 1 -deriopathy retrovirus, ibid., v. 313, p. , « ‘us5, bibliogr.
В. М. Жданов.
Источник
