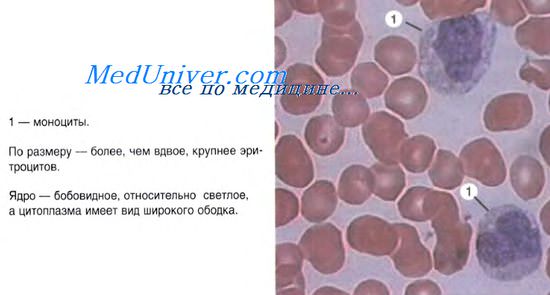
Синдромы нарушения эритропоэза и лейкопоэза у животных

Оглавление темы “Функции клеток крови. Эритроциты. Нейтрофилы. Базофилы.”:
1. Функции клеток крови. Функции эритроцитов. Свойства эритроцитов. Цикл Эмбдена—Мейергофа. Строение эритроцитов.
2. Гемоглобин. Типы ( виды ) гемоглобина. Синтез гемоглобина. Функция гемоглобина. Строение гемоглобина.
3. Старение эритроцитов. Разрушение эритроцитов. Длительность жизни эритроцита. Эхиноцит. Эхиноциты.
4. Железо. Железо в норме. Роль ионов железа в эритропоэзе. Трансферрин. Потребность организма в железе. Дефицит железа. ОЖСС.
5. Эритропоэз. Эритробластические островки. Анемия. Эритроцитоз.
6. Регуляция эритропоэза. Эритропоэтин. Половые гормоны и эритропоэз.
7. Лейкоциты. Лейкоцитоз. Лейкопения. Гранулоциты. Лейкоцитарная формула.
8. Функции нейтрофильных гранулоцитов ( лейкоцитов ). Дефенсины. Кателицидины. Белки острой фазы. Хемотаксические факторы.
9. Бактерицидный эффект нейтрофилов. Гранулопоэз. Нейтрофильный гранулопоэз. Гранулоцитоз. Нейтропения.
10. Функции базофилов. Функции базофильных гранулоцитов. Нормальное количество. Гистамин. Гепарин.
Эритропоэз. Эритробластические островки. Анемия. Эритроцитоз.
Эритропоэз — процесс образования эритроцитов в костном мозге. Первой клеткой эритроидного ряда, образующейся из колониеобразующей клетки эритроцитарной (КОК-Э) — клетки-предшественницы эритроидного ряда, является проэритробласт, из которого в ходе 4—5 последующих удвоений и созревания образуется 16—32 зрелых эритроцита.

Схема процесса: 1 проэритробласт (удвоение) => два базофильных эритробласта I порядка => 4 базофильных эритробласта II порядка =>
8 полихроматофильных эритробластов I порядка => 16 полихроматофильных эритробластов II порядка => 32 полихроматофильных нормобласта =>
32 оксифильных нормобласта => денуклеация нормобластов => 32 ретикулоцита => 32 эритроцита.
Эритропоэз до формирования ретикулоцита занимает 5 дней.
Эритропоэз у человека и животных (от проэритробласта до ретикулоцита) протекает в эритробластических островках костного мозга, которых в норме содержится до 137 на 1 мг ткани костного мозга. Макрофаги эритроцитарных островков играют основную роль в физиологии эритроидных клеток, влияя на их пролиферацию и созревание.
Макрофаги фагоцитируют вытолкнутые из нормобластов ядра, обеспечивают эритробласты ферритином и пластическими веществами, секретируют эритропоэтин и гликозаминогликаны, последние повышают концентрацию ростковых факторов в островках. Эти благоприятные условия для развития эрит-робластов макрофаги создают благодаря наличию рецепторов к эритроидным клеткам-предшественницам.
Из костного мозга ретикулоциты выходят в кровь и в течение суток созревают в эритроциты. По количеству ретикулоцитов в крови судят об эритроцитарной продукции костного мозга и интенсивности эритропоэза. У человека их количество составляет 5— 10%о. За сутки в 1 мкл крови поступает 60—80 тыс. эритроцитов.
В 1 мкл крови у мужчин содержится 5,21 (4,52—5,9) млн, а у женщин — 4,6 (4,1—5,1) млн эритроцитов.
Уменьшение количества эритроцитов в единице объема крови называется анемией, увеличение — эритроцитозом.
Последний может носить физиологический, приспособленный для организма человека характер (например, при подъеме человека в горы, на высоту более 3000 м над уровнем моря).
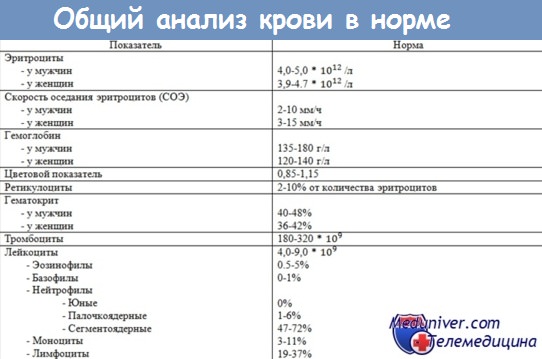
Общий анализ крови в норме
– Также рекомендуем “Регуляция эритропоэза. Эритропоэтин. Половые гормоны и эритропоэз.”
Источник
Диагностика миелодиспластических синдромов – нарушения эритропоэза
Установление диагноза миелодиспластических синдромов (МДС) основывается на выявлении диспластических изменений одного или нескольких ростков гемопоэза. Морфологические изменения клеток эритро-, гранулоцито- и мегакариоцитопоэза в костном мозге и крови очень разнообразны, соотношение нормальных и диспластических элементов у разных больных существенно варьирует. Принято считать клеточную линию измененной, если число диспластических элементов в ней составляет более 10 %.
Для подтверждения клональности процесса и прогнозирования течения заболевания диагностика миелодиспластических синдромов (МДС) должна непременно включать цитогенетическое исследование клеток костного мозга, особенно при незначительном числе гемопоэтических клеток с признаками дисплазии или отсутствии цитопении.
Нарушения эритропоэза при миелодиспластических синдромах. Анемия — наиболее частая патология кроветворения, наблюдаемая у большинства пациентов. Как показали собственные исследования (82 больных первичными миелодиспластическими синдромами (МДС)), анемия была диагностирована у 95,2 % пациентов: наиболее часто — в составе панцитопении (47,6 %), только в сочетании с лейкопенией — 15,9 % и тромбоцитопенией — 17,1 %. Изолированная анемия обнаруживалась у 14,6 % больных. По данным другого отечественного исследования (71 больной первичным МДС), одноростковая цитопения определялась у 33,9 % больных, двухростковая — у 40,8 %, панцитопения выявлялась наиболее редко — у 25 %.
Обычно анемия носит макро- или нормоцитарный характер. В редких наблюдениях описана микроцитарная анемия, выражающаяся в преобладании микроцитов в общей популяции эритроцитов. По данным нашего исследования, наиболее часто отмечалась макроцитарная анемия (53 %), несколько реже — нормоцитарная (44 %). Микроцитарная анемия была выявлена только у 4 % пациентов.
Использование автоматических анализаторов крови позволяет точно измерить средний объем клеток и охарактеризовать распределение фракций по размеру в популяции эритроцитов. Увеличение среднего объема эритроцитов (MCV) более 100 фл свидетельствует о макроцитозе, уменьшение менее 85 фл — о микроцитозе. Показатель средней концентрации гемоглобина в эритроците (МСН) выше 31 пг свидетельствует о гиперхромном характере изменений, ниже 27 пг — о гипохромном.
В большинстве случаев у больных миелодиспластическими синдромами (МДС) констатируется нормохромная анемия. Следует отметить, что анемия у больных миелодиспластическими синдромами (МДС) может иметь смешанный характер и протекать на фоне хронической железодефицитной анемии, особенно у женщин, поэтому на основании данных автоматического анализатора анемия может быть квалифицирована как нормоили микроцитарная, а также нормо- или гипохромная. Только микроскопическое исследование мазков крови в этих случаях позволяет более точно охарактеризовать свойства эритроцитов.

Количество ретикулоцитов у больных миелодиспластическими синдромами (МДС) может колебаться достаточно широко, обычно их число нормальное или сниженное. Ретикулоцитоз может быть обусловлен появлением патологической фракции длительно живущих клеток (4 дня вместо 36 ч в норме), что позволяет обозначить этот процесс как «псевдоретикулоцитоз». В других случаях выраженность анемии при миелодиспластических синдромах (МДС) может усугубляться за счет продукции антиэритроцитарных антител и гемолиза эритроцитов, который сопровождается ретикулоцитозом. Аутоиммунный гемолиз с ретикулоцитозом определяют у 7—14 % больных, в связи с чем предложено выделять подвариант миелодиспластического синдрома с гемолитическим компонентом анемии.
Дисплазия эритроцитов выражается в изменении их формы, в частности, возникающем вследствие нарушения белков цитоскелета. В мазках крови выявляют пойкилоциты, овалоциты, эллиптоциты, стоматоциты и акантоциты. В литературе приводятся наблюдения о сфероцитозе эритроцитов, предшествовавшем развитию миелодиспластического синдрома. Для картины крови характерны также тельца Жолли, кольца Кеббота, базофильная пунктация цитоплазмы и ядросодержащие эритроциты. Подобные признаки не являются строго специфичными для миелодиспластического синдрома и могут быть обнаружены при различных других патологических состояниях.
Наличие нормоцитов в периферической крови наблюдается у 1/4— 1/3 больных миелодиспластическими синдромами (МДС). По нашим наблюдениям, нормоциты присутствуют у 26 % больных первичными миелодиспластическими синдромами (МДС), среднее количество нормоцитов составляет 1,7 ± 1,4 на 100 лейкоцитов.
Данные автоматических анализаторов и тщательное морфологическое исследование мазков являются важными условиями для правильной оценки количественных и качественных параметров красной крови.
В пунктате костного мозга определяется либо резкое уменьшение (до 5 % всех ядросодержащих клеток), либо расширение (до 90 %) красного ростка. Наиболее частым признаком дизэритропоэза является его мегалобластоидный характер, наблюдаемый почти у 90 % больных. В этих случаях определяются макронормобласты как с базофильной окраской цитоплазмы, так и с оксифильной. Встречаются многоядерные формы нормобластов и клетки с цитоплазматической перемычкой. Цитоплазма клеток окрашена неравномерно, включает тельца Жолли и имеет неправильные очертания. Ядра дольчатые, фрагментированные, клетки соединяются ядерными мостиками вследствие нарушенного митоза. Встречаются двух- и многоядерные формы. Структура хроматина — разреженная.
При цитохимическом исследовании реакции Перлса в части случаев в нормобластах определяют резкое увеличение числа (более 10) сидерофильных гранул, расположенных венчиком вокруг ядра. Они представляют собой митохондрии с избыточным накоплением железа. Такие клетки обозначаются как кольцевые сидеробласты. В отдельных работах имеются указания на то, что сидеробластоз при миелодиспластическх синдромах (МДС) может ассоциироваться с редко встречающимся микроцитарным характером анемии].
Нарушение строения органелл эритроцитов сопровождается образованием патологических форм гемоглобина. В литературных источниках указывается, что HbF обнаруживается у 87,5 % пациентов РА, причем преимущественно в эритробластах (F-бластах), но не в эритроцитах, что свидетельствует, по мнению авторов, о неспособности эритробластов к нормальной дифференцировке.
Диспластические нарушения клеток эритроидного ростка включают изменения энзимного спектра клеток. Снижается активность ферментов гликолиза, повышается содержание а-нафтилацетатэстеразы и кислой фосфатазы в нормобластах и эритроцитах. В части случаев наблюдается увеличение содержания ШИК-положительного вещества в диффузной и гранулярной форме. Однако эти цитохимические особенности не являются специфичными для миелодиспластических синдромов (МДС) и могут быть обнаружены при других гемобластозах.
Представляют интерес наблюдения миелодиспластических синдромов (МДС), при которых в клетках эритроидного ростка обнаружены ферменты, характерные только для нейтрофилов. Так, в нормобластах костного мозга цитохимическим методом обнаружена щелочная фосфатаза, а электронно-микроскопическим — пероксидаза. По нашим данным, щелочная фосфатаза в нормобластах присутствует у 69 % больных миелодиспластическими синдромами, число ферментсодержащих клеток составляет 2—63 %. Указанные цитохимические особенности эритроидных предшественников выявляются при любых вариантах заболевания и свидетельствуют о глубоких нарушениях процесса дифференцировки.
– Также рекомендуем “Диагностика миелодиспластических синдромов – нарушения грануломоноцитопоэза”
Оглавление темы “Миелодиспластические синдромы (МДС)”:
- Патогенез миелодиспластических синдромов (МДС) – причины апоптоза
- Ангиогенез при миелодиспластических синдромах – механизмы
- Клетки крови при миелодиспластических синдромах – нарушения функции
- Клиника миелодиспластических синдромов – признаки
- Диагностика миелодиспластических синдромов – нарушения эритропоэза
- Диагностика миелодиспластических синдромов – нарушения грануломоноцитопоэза
- Диагностика миелодиспластических синдромов – дисмегакариоцитопоэз
- Диагностика бластных клеток при миелодиспластических синдромах
- Трепанобиопсия костного мозга при миелодиспластических синдромах (МДС)
- Цитогенетическое исследование при миелодиспластических синдромах – диагностика аномалий хромосом
Источник
Эритроцитопоэз. Гранулоцитопоэз. Этапы эритропоэза и гранулоцитопоэза.Эритроцитопоэз начинается со стволовой кроветворной клетки. Через стадию колониеобразующей мультипотентной клетки (КОЕТЭММ) формируются бурстобразующая (БОЭ-Э) и далее колониеобразующая единица эритроцитов (КОЕ-Э). Клетки этих колоний чувствительны к факторам регуляции пролиферации и дифференцировки. Например, эритропоэтин, вырабатываемый клетками почки, стимулирует пролиферацию и дифференцировку клеток в эритробласты. В IV-й класс включаются базофильный, полихроматофильный и оксифильный эритробласты. Проэритроциты, потом ретикулоциты составляют V-й класс и, наконец, формируются эритроциты (VI-й класс). В эритропоэзе на стадии оксифильного эритробласта происходит выталкивание ядра. В целом цикл развития эритроцита до выхода ретикулоцита в кровь продолжается до 12 суток. Общее направление эритропоэза характеризуется следующими основными структурно-функциональными изменениями: постепенным уменьшением размеров клетки, накоплением в цитоплазме гемоглобина, редукцией органелл, снижением базофилии и повышением оксифилии цитоплазмы, уплотнением ядра с последующим его выделением из состава клетки. В эритробластических островках эритробласты поглощают путем микропиноцитоза железо, поставляемое макрофагами, для синтеза гемоглобина. Развитие эритроцитов происходит в миелоидной ткани красного костного мозга. В периферическую кровь поступают только зрелые эритроциты и немного ретикулоцитов.
Гранулоцитопоэз.Образование гранулоцитов происходит в миелоидной ткани красного костного мозга. Исходная стволовая клетка превращается в мультипотентную клетку — предшественник миелопоэза (КОЕ-ГЭММ) и далее под воздействием колониестимулирующих факторов дифференцируется в общую родоначальную клетку для гранулоцитов и моноцитов (КОЕ-ГМн). В дальнейшем в результате дивергенции возникают родоначальные клетки для гранулоцитов (КОЕ-Гн), которые дифференцируются в идентифицируемые миелобласты (IV-й класс клеток). В ряду дальнейшей клеточной дифференцировки (V-й класс клеток) различают стадии: промиелоцита, миелоцита, метамиелоцита. Начиная со стадии промиелоцита, клетки подразделяются на 3 разновидности: нейтрофильные, эозинофильные, базофильные. Более отчетливо это подразделение можно провести на стадии миелоцитов, когда в клетках накапливается достаточное количество специфической зернистости. До стадии миелоцитов включительно клетки гранулоцитопоэза делятся митозом. Метамиелоциты митозом уже не делятся. В этих клетках ядро приобретает вначале палочковидную, а затем сегментированную форму. Общее направление дифференцировки клеток гранулопоэза характеризуется: постепенным уменьшением размеров клетки, снижением базофилии цитоплазмы, появлением в цитоплазме специфических гранул, уменьшением размеров ядра, появлением сегментированности ядра и его уплотнением, сдвигом ядерно-цитоплазменного отношения в сторону преобладания размеров цитоплазмы над размерами ядра. В периферическую кровь поступают зрелые гранулоциты (VI-й класс клеток) — нейтрофилы, эозинофилы и базофилы, а также небольшое количество малодифференцированных (юных) гранулоцитов. Физиологическая регенерация обеспечивается делением преимущественно клеток V-ro класса — миелоцитов. – Также рекомендуем “Тромбоцитопоэз. Моноцитопоэз. Лимфоцитопоэз и иммуноцитопоэз.” Оглавление темы “Лимфоциты. Соединительные ткани.”: |
Источник
© Автор: Солдатенков Илья Витальевич, врач терапевтического отделения, специально для СосудИнфо.ру (об авторах)
Эритропоэз — физиологический процесс образования и дифференцировки красных кровяных клеток – эритроцитов. Данный термин в переводе с древнегреческого языка дословно означает «красный, делать». Эритроциты берут начало от гемопоэтической стволовой клетки — основной единицы кроветворения. Процесс их деления и созревания длится в среднем 3—7 дней. Клетки-предшественники чувствительны к гликопротеину, эритропоэтину и прочим стимулирующим факторам.
Красные кровяные тельца были описаны в 1913 году ученым из Англии Артуром Бойкоттом. Жизненный цикл эритроцитов составляет в среднем сто дней. Для поддержания их стабильного уровня в крови постоянно формируются новые эритроидные клетки. Погибающие клетки захватываются и перевариваются макрофагами. Из кроветворной ткани в кровоток каждую минуту выходит 1,8×109 ретикулоцитов. Кровопотеря, гемолиз и прочие факторы максимально стимулируют гемопоэз, который увеличивается в 10-12 раз.
Видео: основное об эритропоэезе и гемопоэзе
Эритроциты
Развитие эритроцитов и создание уникальной структурно-функциональной модели происходит путем дифференцировки. Красные клетки крови созревают у детей первых пяти лет жизни в костном мозге всех костей скелета. Бедренная и берцовые кости перестают участвовать в кроветворении к 24 годам. В позвонках, грудине, ребрах, черепе и прочих плоских костях клетки крови образуются всю жизнь.
Эритроциты выполняют жизненно важные функции:
- дыхательная — транспорт кислорода к тканям и выведение углекислоты из организма;
- трофическая — доставка аминокислот и прочих питательных веществ к внутренним органам, обеспечение регенерации и репарации;
- детоксикационная — адсорбция токсинов и их инактивация;
- метаболическая — содержание большого числа энзимов;
- коагуляционная — наличие на поверхности клеток плазменных факторов свертывания крови;
- буферная — регулирование КОС и водно-минерального обмена;
- депонирующая — хранение воды и микроэлементов;
- иммуномодулирующая – участие в формировании иммунитета.
Особенности физиологии красных телец:
- Эритроциты способны выпадать в осадок. Это свойство напрямую зависит от белкового состава крови – чем больше в плазме содержится грубодисперсных глобулинов, тем выше СОЭ.
- При замедлении системного кровотока и сгущении крови эритроциты начинают объединяться в крупные агрегаты. Они называются ложными, поскольку распадаются на функционально активные клетки, сохраняющие свою структуру.
- Пластичность – обратимая деформация клеток, проходящих через капилляры, артериолы и венулы. Это свойство обусловлено наличием в мембране спектрина – особого белкового соединения.
- К физиологическим свойствам красных кровяных телец также относится осмотическая устойчивость и деструкция после длительной циркуляции в кровотоке.
Структура красных кровяных телец максимально адаптирована для реализации жизненно важных функций. Эти узкоспециализированные клетки мобильны. Они обеспечивают диффузию газов, взаимодействуют с гемоглобином, быстро делятся и проникают в системный кровоток. Эритроциты на 50% состоят из протеинов, на 40% из липидов и на 10% из углеводов. Клетки способны деформироваться и циркулировать по сосудам малого калибра. Такая способность обусловлена их гибкостью и пластичность. Эритроциты имеют дисковидную форму с углубленным центром. Эти безъядерные элементы не содержат органелл – их цитоплазма наполнена гемоглобином.
Для изучения формы, структуры и размера эритроцитов проводят микроскопическое исследование мазка крови. Морфологические и тинкториальные свойства клеток помогают поставить диагноз разных видов анемии.
Физиология
Эритропоэз начинается под воздействием стимулирующих факторов. Основным из них является гипоксия тканей — нехватка кислорода и ишемия органа. В ответ на происходящие изменения в организме почки синтезируют гормон эритропоэтин. Именно он запускает процесс образования эритроцитов. Влиянием этого биологически активного вещества обусловлена пролиферация и дифференциация клеток-предшественников. Процесс кроветворения ускоряется, эритроциты массово выходят в системный кровоток. Гормоны оказывают непосредственное воздействием на процесс образования железосодержащего белка — гемоглобина. Они стимулируют синтез рибонуклеиновой кислоты, обеспечивающей секрецию необходимых энзимов. Эритропоэтины улучшают кровоснабжение кроветворной ткани и ускоряют, таким образом, гемопоэз, протекающий в эритробластических островках костного мозга.
- На начальных стадиях развития плода эритропоэз осуществляется в зародышевом органе – желточном мешке.
- С 5 недели эмбрионального развития – в печени.
- С 16 недели беременности эритроциты продуцируются в фетальной селезенке.
- С 20 недели гестации этот процесс осуществляется в костном мозге.
Процесс образования форменных элементов происходит вне синусов костного мозга и называется эктраваскуляторным. Когда ребенок появляется на свет, его кроветворная ткань уже полностью сформирована. Постнатальный гемопоэз обеспечивает физиологическую регенерацию крови – ее обновление.
Факторы, стимулирующие эритропоэз:
- физическое перенапряжение,
- кровопотеря,
- курение,
- подъем в горы,
- кардиоваскулярные патологии,
- хронические бронхолегочные заболевания,
- химиотерапия,
- длительная и интенсивная витаминотерапия.
Результатом повышенной продукции эритроцитов является эритроцитоз. Он бывает физиологическим и патологическим.
Факторы, угнетающие эритропоэз:
- стойкая дисфункция почек,
- гипопротеинемия,
- авитаминозы,
- нехватка железа в организме и прочих микроэлементов,
- хронические патологии в стадии декомпенсации,
- острые инфекции,
- неоплазии недоброкачественного течения,
- тяжелые интоксикации,
- поражение костномозговых структур,
- онкогематологические расстройства — лейкоз.
Нарушение кроветворения приводит к развитию серьезного заболевания крови – анемии.
В крайне редких случаях эритропоэз осуществляется не в костном мозге, а в печеночной ткани и селезенке. Причинами подобного отклонения являются особые состояния, патологические процессы и некоторые обстоятельства.
Схема и стадии
Эритроциты во время своего развития проходят несколько сменяющих друг друга стадий. Гемангиобласт – первичная стволовая клетка, закладывающаяся в онтогенезе. Этот предок всех эндотелиальных и кровеобразующих структур трансформируется в гемоцитобласт – плюрипотентную клетку. Из нее образуется множество различных клеточных элементов, но не целый организм. Мультипотентная стволовая клетка – общий миелоидный предшественник, способный формировать клетки тканей, из которых сам был получен, и превращаться в унипотентную клетку. Она дифференцируется в сторону эритропоэза. Именно с этого звена гемопоэза начинается эритроидная линия.
Схема процесса:
- Колониеобразующая единица эритроцитопоэза — лимфоцитоподобная клетка, не имеющая специальных морфологических характеристик, способная к самообновлению и дифференциации.
- Она непрерывно делится и дает начало базофильным клеткам — проэритробластам. Это первый визуально определяемый элемент эритроцитарного ряда, способный к образованию гемоглобина. Его круглое ядро занимает более половины клетки, окрашивается в темно-фиолетовый цвет и имеет тонкодисперсную структуру хроматина.
- В результате его деления образуются базофильные эритробласты. В отличии от своих предшественников они содержат относительно мелкие ядра, базофильную цитоплазму и много рыхлого гетерохроматина.
- Митотическое деление базофильных эритробластов заканчивается появлением полихроматофильных эритробластов, имеющих в ядре конденсированный хроматин.
- Митозы этих клеток дают начало нормобластам, которые прочным кольцом окружают ретикулярную клетку, охватывают ее своими утолщенными отростками и образуют эритробластические островки. Ортохроматические эритробласты не имеют органелл. В их цитоплазме содержится много гемоглобина, а в ядре – глыбок гетерохроматина.
- После выталкивания ядра из тела клетки образуются ретикулоциты. Они синтезируют и накапливают гемоглобин благодаря работе особого рибосомального аппарата. Ретикулоциты выходят из органа кроветворения и попадают в просвет кровеносных сосудов.
- Непосредственно в кровотоке они трансформируются в зрелые эритроцитарные клетки, не имеющие ядра, органелл и рецепторных белков на поверхности. Эритроциты доставляют кислород к органам и удаляют из низ углекислый газ. Процесс созревания длится 24 часа.
Эритроциты на каждой стадии кроветворения имеют особые морфологические, тинкториальные, микроскопические, биохимические и иммунологические свойства. Во время дифференцировки клеток уменьшается размер ядра. Оно постепенно сморщивается и полностью исчезает. Цитоплазма, наоборот, увеличивается в объеме, изменяет свой цвет, накапливает гемоглобин.
Регуляция
Существуют различные виды регуляция эритропоэза — гуморальная, нервная, с помощью ретикулярных клеток, витаминов и минералов.
Гуморальная регуляция осуществляется по принципу отрицательной обратной связи. Благодаря гормону эритропоэтину процессы образования юных эритроидных клеток и распада старых, деформированных телец четко сбалансированы и непрерывны. Уровень эритроцитов в крови сохраняется относительно стабильным и обеспечивает полноценное кровоснабжение и оксигенацию тканей. Гипоксия органов, вызванная сосудистым спазмом, малокровием или иной патологией, стимулирует секрецию эритропоэтина, который усиливает продукцию красных телец и повышает их концентрацию в крови. Когда кровоснабжение органов восстанавливается, секреция эритропоэтина понижается.
К другим гормонам, контролирующим эритропоэз, относятся: кортизол, андрогены, глюкокортикоиды, инсулин, соматотропный и тиреоидные гормоны, катехоламины, интерлейкины, плацентарный пролактин. Они увеличивают продукцию эритропоэтина или непосредственно стимулируют гемопоэз. Подавляют эритропоэз эстрогены, кейлоны, глюкагон, ацетилхолин, интерфероны, факторы некроза опухолей.
- Рост и развитие организма человека сопровождаются усилением интенсивности эритропоэза.
- При гипергликемии и гипотиреозе развивается анемия, а при тиреотоксикозе возникает эритроцитоз.
- При сильном стрессе повышается продукция эритроцитов, и улучшается кровоснабжение тканей.
- Гипофункция надпочечников сопровождается эритропенией, а гиперкортицизм — эритроцитозом.
Нервная регуляция происходит следующим образом: симпатическая система активизирует эритропоэз, а парасимпатическая – тормозит.
Ретикулярные клетки влияют на процесс кроветворения двумя способами:
- Фагоцитоз — процесс поглощения и переваривания клеточных оболочек, разрушения зрелых эритроцитов с пороками развития, прекращения метаболизма ядер эритробластов.
- Рофеоцитоз — перенос ферритина, образовавшегося после распада аномальных эритроцитов, молодым ортохроматическим эритробластам.
Макрофаги оказывают непосредственное воздействие на пролиферацию и созревание эритроидных клеток. Они поглощают ядра нормобластов, обеспечивают эритробласты железом и питательными веществами, стимулируют синтез эритропоэтина и гликозаминогликанов, которые повышают концентрацию факторов роста в островках.
Для осуществления эритропоэза критически необходимы некоторые витамины и минералы:
- кобаламин — запускает секрецию глобина,
- фолиевая кислота — принимает участие в образовании ДНК ядерных форм,
- пиридоксин – обеспечивает продукцию гема,
- рибофлавин — формирование липидной оболочки эритроцитов,
- витамин С — ускоряет усвоение железа,
- витамин РР – укрепляет строму из липидов и предотвращает гемолиз,
- медь — позволяет железу быстрее всосаться в кишечнике и включиться в структуру гема,
- никель и кобальт – образование железосодержащего белка крови,
- цинк — входит в состав жизненно необходимых энзимов,
- селен — защита клеток от свободных радикалов.
Нехватка одного из них может вызвать нарушение эритроцитопоэза, а именно дифференцировки и деления стволовых клеток.
Видео: подробные лекции о гемопоэзе
Патология
Под воздействием неблагоприятных эндогенных и экзогенных факторов эритропоэз нарушается. Основные гематологические синдромы обусловлены количественными и качественными изменениями структуры и функций эритроцитов. У больных развиваются тяжелые заболевания, в основе которых лежит эритропения или эритроцитоз.
Анемия — патологический процесс, обусловленный низким уровнем эритроцитов и гемоглобина в крови. Это самое распространенное гематологическое расстройство. Оно бывает самостоятельным — вызванным нарушением гемопоэза, а также вторичным — возникающим при заболеваниях внутренних органов.
К анемиям, обусловленным нарушением кровообразования относятся:
нормобластный и мегалобластный типы эритропоэза (при анемии)
- Мегалобластная анемия отличается пониженной концентрацией крупных эритроцитов, содержащих много гемоглобина. В происхождении патологии «виноваты» клетки-предшественники – мегалобласты. В клетках костного мозга нарушается синтез ДНК. Вместо нормальных эритроцитов образуются эритробласты. Они являются функционально неактивными – не связывают кислород и не транспортируют его к органам и тканям. Патологический процесс обусловлен дисбалансом между ядром и протоплазмой, нарушением деления клеток и развития хромосом.
- Железодефицитная анемия связана с нехваткой железа в организме и низким уровнем гемоглобина в эритроцитах. Микроэлемент поступает в ЖКТ с пищей, связывается в кишечнике с белком трансферрином, всасывается в кровь и направляется в костный мозг, где встраивается в молекулу гемоглобина. Патология проявляется трофическими расстройствами — шелушением кожи, сухостью слизистых, выпадением волос, ломкостью ногтей.
- В12 – дефицитная анемия – недостаточность витамина В12, необходимого для дифференциации красных кровяных телец. Данный элемент поступает в организм с пищей, связывается с внутренним фактором Касла и участвует в кроветворении. Он необходим для синтеза ДНК и является катализатором этой реакции. У больных с анемией возникают признаки поражения ЖКТ и нервной системы.
различные изменения в созревании эритроцитов
К более редким формам анемии, обусловленной нарушением эритропоэза, относятся: метапластическая, фолиеводефицитная, сидеробластная, апластическая. Клинически все виды анемии проявляются признаками астеновегетативного синдрома – бледностью кожи, тахикардией, головокружением, слабостью, бессилием, плохим настроением.
Эритроцитоз — патологическое состояние, при котором увеличивается количество эритроцитов и гемоглобина в крови. Сама жидкость густеет, что затрудняет ее движение по сосудам и нарушает кислородный обмен. Количество эритроцитов и гемоглобина в крови увеличивается под воздействием различных факторов — физиологических и патологических.
При обезвоживании организма, связанном с профузными поносами, рвотой, гипергидрозом, или задержке жидкости, вызванной отеком легких, шоком, кардиоваскулярной недостаточностью, увеличивается концентрация красных телец в крови. Когда количество эритроцитов становится чрезмерным, повышается вязкость крови — она сгущается. Возможна агглютинация, склеивание эритроцитов и увеличение объема циркулирующей крови. У больных поднимается кровяное давление, возникает головная боль, головокружение и багровый цианоз, нарушается зрение, увеличиваются печень и селезенка, развиваются носовые кровотечения, тромбозы, инфаркты, инсульты.
Видео: лекция об анемиях – от костного мозга до селезенки
Рекомендации читателям СосудИнфо дают профессиональные медики с высшим образованием и опытом профильной работы.
На ваш вопрос в форму ниже ответит один из ведущих авторов сайта.
В данный момент на вопросы отвечает: А. Олеся Валерьевна, к.м.н., преподаватель медицинского вуза
Поблагодарить специалиста за помощь или поддержать проект СосудИнфо можно произвольным платежом по ссылке.
Источник