Стопы и кисти при синдром
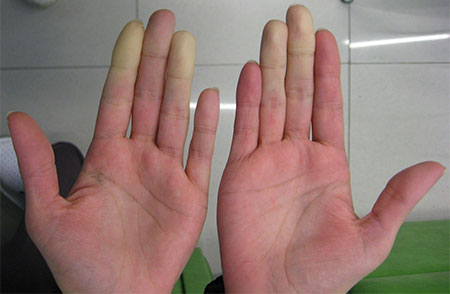
Болезнь или синдром Рейно – это патология, поражающая верхние и нижние конечности. Характеризуется синдром приступообразным нарушением кровоснабжение кистей рук и стоп вследствие внезапного спазма сосудов, что проявляется резко очерченными изменениями цвета кожи пальцев. Изредка при синдроме Рейно отмечаются нарушения кровоснабжения в кончике носа или языка, в тканях подбородка или ушных раковин. Что это такое – синдром Рейно? Каковы его причины, признаки и последствия?
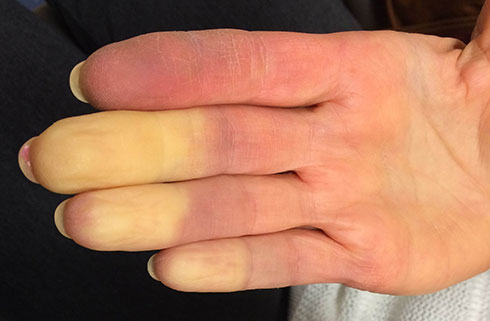
Что это такое – синдром или болезнь Рейно
Синдром назван по имени французского невропатолога Мориса Рейно, впервые описавшего его еще в 1862 году. Врач заметил, что кисти рук у работниц, которым ежедневно приходилось полоскать бельё в холодной воде, имели синюшную окраску. Женщины жаловались на частое онемение и неприятное покалывание в пальцах.
Рейно сделал вывод, что длительное охлаждение рук приводит к затяжному спазму сосудов и нарушению кровообращения. По его мнению, синдром – это особая форма невроза. Однако, подтверждения этой гипотезы до сих пор не найдено. Несмотря на то, что болезнь известна так давно, не удается пока установить причины ее возникновения.
Итак, синдром Рейно характеризуется приступообразным вазоспазмом – сужением периферических кровеносных сосудов кистей и стоп в ответ на воздействие холода, эмоциональное или физическое напряжение.
Под внешним воздействием внезапно возникает обратимый дискомфорт и изменение цвета кожи (бледность, синюшность, сильное покраснение или их комбинации) в одном или более пальцах. Иногда страдают и другие дистальные органы (в частности, нос, язык, подбородок, ушные раковины).
Формы и причины синдрома
Выделяют две формы синдрома Рейно – первичная и вторичная. Клинические проявления их абсолютно идентичны, различия имеются лишь в причинах появления.
Первичная форма или собственно болезнь Рейно
Встречается более чем в 80% случаев чаще, чем вторичная. Развивается как самостоятельное заболевание без признаков других патологий, характеризуется двусторонним проявлением и более ранним вовлечением рук, чем ног.
Встречается заболевание у 3-5% населения, причем в 90% случаев от общего количества заболевших – это женщины молодого возраста (25-35 лет).
Очень редко наблюдается синдром Рейно у детей и пожилых людей. Известно также, что определенную роль в возникновении болезни играют наследственная предрасположенность и инфекционные заболевания.

Вторичная форма
Вторичная форма синдрома Рейно возникает на фоне различных заболеваний:
- Ревматологические болезни.
Для женщин, чаще других, это системная красная волчанка, системная склеродермия, ревматоидный артрит.
Для мужчин – подагра, болезнь Бехтерева, реактивный и псориатический артриты. - Гематологические заболевания (болезнь холодовых агглютининов, истинная полицитемия, синдром повышенной вязкости крови).
- Патологии с компрессионным нейрососудистым синдромом (шейное ребро, синдром передней лестничной мышцы или малой грудной мышцы, синдром карпального канала, компрессионный синдром верхней апертуры грудной клетки).
- Некоторые болезни позвоночника (остеохондроз, деформирующий спондилёз, сколиоз, кифоз).
- Неврологические заболевания (сирингомиелия, радикулит, рассеянный склероз, полиомиелит).
Синдром, в отличие от болезни Рейно, имеет чаще односторонний характер.
Почему возникает синдром Рейно
Среди факторов, способствующих дебюту синдрома Рейно, можно назвать:
- постоянные переохлаждения конечностей;
- профессиональные факторы (воздействие вибрации – вибрационная болезнь, интенсивная и продолжительная физическая нагрузка на кисти и пальцы, хроническое отравление химическими веществами в условиях вредного производства);
- травмы пальцев, обморожение;
- тяжелые стрессовые ситуации;
- нарушения работы эндокринной системы (дисфункция надпочечников, щитовидной или половых желез);
- приём некоторых лекарственных или наркотических препаратов, в том числе никотина.
Течение заболевания медленно прогрессирующее, однако независимо от стадии синдрома Рейно возможны случаи обратного развития процесса – при наступлении климактерического периода, беременности, после родов, а также в связи с изменением климатических условий.
Симптомы и признаки
Симптоматика синдрома Рейно обусловлена пароксизмальным вазоспазмом и развивающимися вследствие этого повреждениями тканей. Клиническая картина заболевания соответствует стадии его развития. Чем дольше развивается патология, тем более выражены симптомы.
Ангиоспастическая стадия.
Типичными являются кратковременные спазмы сосудов концевых фаланг 2-4 пальцев стоп и кистей. Приступы ишемии вначале возникают редко и длятся недолго. Провоцирующими факторами могут являться: воздействие холодных температур, стрессовая ситуация, курение.
Кончики пальцев белеют, становятся холодными на ощупь, кожа теряет чувствительность. Затем неожиданно парестезия сменяется жжением, ломящей болью, чувством распирания.
После прекращения внешнего воздействия приступ завершается резкой гиперемией кожи и ощущением жара. Согревание стоп и кистей ускоряет восстановление ощущений и нормального цвета кожи.
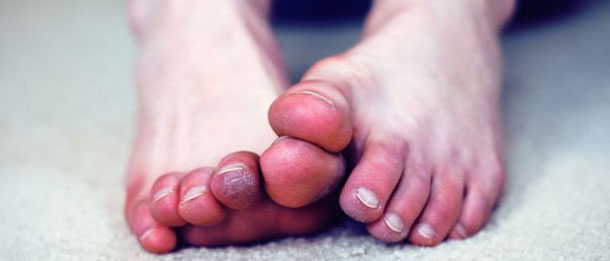
Ангиопаралитическая стадия.
Характеризуется частыми приступами, возникающими без видимой причины и длящимися от нескольких минут до нескольких часов. Изменения цвета затрагивают 3 средних пальца, в редких случаях – большие пальцы. Они становятся бледного или синюшного цвета (цианоз).
По мере развития приступа пальцы могут приобретать двухцветный (цианоз, эритема) или трехцветный окрас (бледность, сопровождаемая цианозом, а после согревания эритемой из-за реактивной гиперемии) с чёткими границами изменения цвета. К концу приступа сохраняется ярко выраженное покраснение кистей и стоп с отечностью и пастозностью пальцев.
Трофопаралитическая стадия.
Приступообразные проявления синдрома Рейно возникают все чаще, в промежутках между ними стопы и кисти остаются синюшными, холодными, влажными.
Длительное и тяжелое течение болезни приводит к тяжелым последствиям. Результатом нарушения кровоснабжения и постоянной ишемии тканей могут стать трофические изменения в виде плохо заживающих трофических язв, участков некрозов мягких тканей, разрушению ногтевых пластин, деформации фаланг пальцев, развитию гангрены.
При первичном синдроме Рейно сосудистый спазм может длиться от минут до часов, но редко бывает настолько тяжелым, чтобы вызвать некроз.
Вторичная форма или болезнь Рейно, развивающаяся на фоне заболеваний соединительной ткани, может прогрессировать до болевой гангрены и даже самоампутации кончиков пальцев.
Синдром Рейно – к какому врачу обратиться
Установление в каждом конкретном случае диагноза болезни или синдрома Рейно имеет принципиальное значение, так как стойкие положительные результаты обычно комплексной и длительной терапии при вторичном синдроме Рейно возможны лишь при устранении или воздействии на его первопричину.

При появлении симптомом заболевания пациенту необходимо посетить терапевта для общего осмотра и сбора анамнеза. Врач общей квалификации направит на консультацию к узким специалистам, занимающихся диагностикой и лечением болезни Рейно:
- ревматолог;
- сосудистый хирург;
- невролог.
Диагностика патологии
Главная задача – дифференцировать болезнь и синдром Рейно. При этом внимание обращают на сосудистый спазм, возникновение которого происходит во время действия холода или стресса, симметричность проявления симптомов болезни и повторения спазмов, которые присутствуют на протяжении нескольких лет.
Для окончательной постановки диагноза необходимо наблюдение за больными с подозрением на болезнь Рейно не менее 2 лет, так как в эти сроки обычно выявляются заболевания, сопровождаемые синдромом Рейно.
- Первоначальная диагностика болезни Рейно – холодовая проба П.П.Алексеева, позволяющая определить время восстановления температуры в конечности после ее охлаждения.
Пациенту в комнате при 20-21 °С измеряют кожную температуру на кончиках пальцев кисти или стопы. После этого кисть (стопу) на 5 минут опускают в охлажденную до 5 °С воду. После охлаждения на тех же точках вновь регистрируют неоднократно кожную температуру вплоть до восстановления ее первоначального значения.
У здоровых людей ренагрев конечности происходит через 10-12 минут, а при болезни Рейно за этот период времени температура в конечности восстанавливается лишь наполовину. Для полного же ренагрева требуются десятки минут.
- При синдроме Рейно выявить стенозирование пальцевых артерий, отсутствие капиллярных сетей и коллатералей позволяет ангиография периферического сосудистого русла.
- Интенсивность и объем кровотока в артериях конечностей исследуют с помощью реовазографии.
- Для определения тонуса сосудов используют плетизмографию.
- Проводят капилляроскопию – визуальное исследование дистального ряда капилляров ногтевого ложа, позволяющую обнаружить морфологические изменения микрососудистого рисунка, свидетельствующие о нарушения кровоснабжения.
- Лазерная доплеровская флоуметрия, применяемая для оценки периферической микроциркуляции, позволяет выявить дефекты метаболической и миогенной регуляции кровообращения, снижение вено-артериальных реакций и симпатической активности.
Лабораторные методы исследования крови при болезни Рейно показывают существенное повышение вязкости крови, рост титра холодовых и противососудистых антител на поздних стадиях, а также используются для выявления или исключения сопутствующих заболеваний.
Как лечить и предотвратить синдром Рейно
Меры профилактики и помощи в домашних условиях
В первую очередь можно самостоятельно можно уменьшить частоту приступов и выраженность клинических проявлений патологии. Для этого необходимо максимально устранить влияние факторов риска:
- Следить за поддержанием нормальной температуры конечностей, не допускать переохлаждений.
- Полноценно и регулярно питаться.
- Отказаться от пагубных привычек (алкоголь, курение).
- Переехать для жительства в местность с теплым и мягким климатом.
- Отдыхать, соблюдать оптимальный режим бодрствования и сна.
- Избегать чрезмерных эмоциональных нагрузок, стрессов, вибраций.
- Ежедневно делать гимнастику и самомассаж рук и ног.
Очень важно отказаться от курения, так как никотин, содержащийся в табаке, способствует сужению сосудов и нарушению кровообращения.
Лечение этого заболевания комбинированное. Оно включает медикаментозную терапию, психотерапию, различные виды физиолечения, иглорефлексотерапию.
Консервативное лечение синдрома Рейно
Консервативное лечение при синдроме Рейно идентично таковому при болезни Рейно, однако главное внимание у этих больных необходимо уделить воздействию на причинный фактор – основное заболевание, провоцирующее спазм сосудов конечностей.
Из лекарств обычно используют:
- сосудорасширяющие (Фентоламин) и гипотензивные лекарственные препараты;
- седативные средства – Диазепам, Реланиум, Сибазон;
- блокаторы кальциевых каналов – Циннаризин, Коринфар, Изоптин, Верапамил;
- препараты, улучшающие реологические свойства (вязкость, текучесть) крови – Пентоксифиллин, Вазонит, Трентал, в некоторых случаях показан плазмаферез;
- для устранения болевого синдрома – новокаиновые блокады, анальгетики, нейролептики;
- витамины В, А, Е, С, РР, способствующих улучшению состояния сосудов и трофики тканей;
- иммуномодуляторы.
Хороший эффект дают физиотерапевтические процедуры – амплипульстерапия, магнитотерапия, ультразвук на кисти рук и стопы, бальнеолечение, а также чрескожная стимуляция нервов.
Хирургическое лечение
Хирургическим методом лечения является симпатэктомия. Суть лечения заключается в «выключении» нервных волокон, по которым идут патологические импульсы, заставляющие кровеносные сосуды спазмироваться. Существуют несколько видов симпатэктомии. Наименее травматичной является эндоскопическая симпатэктомия.
Результаты симпатэктомий при болезни, и особенно при синдроме Рейно, труднопредсказуемы. Возможны рецидивы болезни через 1-2 года. Тем не менее у большинства прооперированных больных наблюдается отчетливый положительный эффект.
Как крайняя и вынужденная мера может быть применена ампутация пораженных фаланг пальцев.
Прогноз для жизни
Комбинация консервативных и хирургических методов лечения эффективны 79—83 % больных. Стабильность результатов обеспечивается благодаря соблюдению мер профилактики, а также длительностью диспансерного наблюдения и лечения пациентов с болезнью и синдромом Рейно.
Источник
 16.01.2021
16.01.2021
Пороки развития стопы и кисти при синдроме Горлина-Гольтца (описание двух клинических случаев)
При синдроме Горлина-Гольтца множественные базально-клеточные опухоли чаще появляются в позднем детском возрасте, но могут быть и врожденными
ВВЕДЕНИЕ
Синдром Горлина-Гольца (синдром базальноклеточных невусов) – syndromum Gorlin- Golz (basal cell nevus syndromum), код по МКБ-10 – D36.9.
Синонимы: фокальная дермальная дисплазия, гипоплазия мезоэктодермальная очаговая, синдром базальноклеточного невуса, невобазоцеллюлярный синдром, аномалия наследственно-семейная эктомезодермальная, невоидные базальноклеточные карциномы, дисплазия эктомезодермальная очаговая, синдром Гольтца, фокальная дермальная гипоплазия, синдром мезоэктодермальной дисплазии.
В зарубежной литературе этот симптомокомплекс называется синдромом Gorlin-Golz или синдромом Golz, что более адекватно отражает хронологию выделения данной патологии.
Впервые о синдроме (невобазоцеллюлярный синдром) сообщалось в 1894 году [13, 20]. Но заболевание существует уже давно – Satinoff и Wells нашли аномалии скелета, опухоли кожи, кисты челюстей и пигментированные вдавления на ладонях и подошвах у двух древнеегипетских мумий [18]. Детально описали синдром в 1960 году американский дерматолог и гистопатолог Robert W. Goltz и американский стоматолог Robert James Gorlin [11].
Распространенность синдрома колеблется от 1/57000 до 1/256 000 [16]. Большинство заболевших – представители европеоидной расы [6, 15]. Отмечается высокая летальность для плодов мужского пола.
Синдром Горлина-Гольца может ассоциироваться сдругими поражениями кожи: эпидермальными кистами, милиумом, фибромами, ладонноподошвенным гиперкератозом [3].
При синдроме Горлина-Гольтца множественные базально-клеточные опухоли чаще появляются в позднем детском возрасте, но могут быть и врожденными. Количество базалиом может достигать нескольких сотен. В основном поражаются лицо, шея, туловище и конечности [19]. Вначале процесс представлен поверхностными базалиомами диаметром от 1 до 3 см, развивающимися медленно и практически не меняющимися, но после 30 лет отдельные новообразования
могут быстро увеличиваться до 5-10 см [12]. 30-65 % пациентов до 10 – летнего возраста, до 80 % пациентов в возрасте до15 лет и 85 % больных старше 20 лет имеют точечные пигментированные углубления на ладонях и подошвах, которые нередко возникают раньше других кожных проявлений синдрома [9].
Множественные базально-клеточные опухоли ассоциируются с разнообразными пороками развития скелета, глаз, нервной, эндокринной систем и других органов и тканей [1, 4, 15, 16].
У 75-90 % больных встречаются изменения со стороны костной системы: кисты верхних и нижних челюстей, кифосколиоз, расщепление ребер, синостозы, прогнатия, истинный гипертелоризм, субкортикальные кистозные изменения длинных трубчатых и плоских костей. Наиболее характерный признак – расщепление переднего отдела стоп и кистей.
Встречаются дополнительные пальцы на руках и ногах, различные виды синдактилий пальцев кисти [4, 5, 17].
Аномалии глаз отмечаются у 26 % больных и проявляются врожденной слепотой, катарактой, глаукомой, колобомой, сторобизмом, косоглазием, врожденной катарактой [12].
Аномалии нервной системы проявляются гидроцефалией, недоразвитием каллезного тела головного мозга, эпилепсией, деменцией, кистами прозрачной перегородки, агенезией мозолистого тела, интрапаренхимальными кистами головного мозга, менингиомами, медуллобластомами. Умственная отсталость встречается примерно в 5 % случаев [8, 10, 15].
Нарушения эндокринной системы у больных могут проявляться крипторхизмом, бесплодием, фиброматозом яичников. С синдромом Горлина-Гольца могут сочетаться нейрофиброматоз I типа, лимфогранулематоз, медуллобластома [7].
. Дородовая диагностика возможна с помощью УЗИ и анализа ДНК, выделенной из клеток плода (полученных путем амниоцентеза или биопсии хориона).
Дифференциальная диагностика проводится с БАЗЕКС синдромом, trichoepithelioma papulosum мультиплекс и синдромом Торре (синдром Muir-Торре) [16]. Диагноз синдрома Горлина-Гольтца устанавливается на основании совокупности цитогенетических, серологических, клинических исследований и результатов обследования стоматологом, челюстно-лицевым хирургом, невропатологом, окулистом, эндокринологом, гинекологом; обязательна рентгенография плоских костей, а для выявления пластинчатого обызвествления серпа большого мозга – рентгенологическое исследование черепа. Дифференциальный диагноз проводят с первично-множественными базалиомами [1, 7, 15].
. При синдроме Горлина-Гольца специфическое лечение до сих пор не разработано и является симптоматическим.
Существующие методы лечения базалиом направлены на ликвидацию первичного очага поражения, предупреждение рецидива опухоли и получение хорошего косметического результата. Применяются лучевая и лазеротерапия, хирургическое лечение, криодеструкция, электрокоагуляция, химиотерапия (локальная и общая), иммунотерапия, фотодинамическая терапия, лечение синтетическими ретиноидами и препаратами, нормализующими активность ферментов циклазной системы. Однако у больных с синдромом Горлина-Гольца наблюдается повышенная чувствительность к лучевому воздействию, образование грубых рубцов после рентгенотерапии.
Хирургическое иссечение, криодеструкция, лучевая терапия, электродиссекция и лазерное удаление эффективны при одиночных очагах.
Для лечения множественных и рецидивирующих базалиом применяют комплексные методы лечения с системным введением цитостатиков, но при этом цитотоксический препарат оказывает выраженное токсическое действие на организм больного.
В последние годы в качестве терапии применяются препараты группы интерферонов. В результате адьювантной иммунотерапии опухоли могут либо полностью регрессировать, либо иноперабельные новообразования могут превратиться в доступные для удаления [2].
Рекомендуется проведение курса терапии, сходной с лечением склеродермии и атрофии кожи. При алопециях целесообразно назначение препаратов цинка, а имеющиеся папилломы удаляют хирургическим способом, криодеструкцией, лазером. В.А.Маланчук и соавт. (2008) из Национального медицинского университета им. А.А.Богомольца разработали алгоритм действий врача в случае диагностирования синдрома Горлина-Гольца, обеспечивающий комплексный диагностический и лечебный подход и помогающий создать индивидуальный план лечения, который может улучшить, а иногда и сберечь жизнь пациенту.
Подход к лечению ортопедической патологии индивидуален и проводится по строгим показаниям при наличии деформаций, препятствующих самообслуживанию и передвижению.
Под нашим наблюдением находится двое детей с клиническими проявлениями данного синдрома.
Клинические примеры:
1. Пациентка А., 7 месяцев, поступила с диагнозом: порок развития кистей и стоп. Из анамнеза известно, что ребенок от первой беременности, первых срочных родов, протекавших без особенностей. Родственники наличие наследственных заболеваний отрицают. Ребенок отстает в психомоторном развитии.
При клиническом обследовании на коже туловища– пигментные пятна светло-малинового цвета (аналогично линиям Блашко), расположенные вдоль крупных сосудисто-нервных пучков, и втяжения на коже (рис. 1).
При осмотре: голова неправильной формы, с увеличением лобной и теменной частей, расположена по средней линии. Отмечается деформация ушных раковин (рис. 2).
Ось позвоночника правильная. Амплитуда движений в крупных суставах верхних конечностей не ограничена.
Строение левой кисти без особенностей. Правая кисть: расщепление до пястных костей в третьем межпальцевом промежутке, базальная синдактилия 2-3 пальцев, первый палец приведен (рис. 3).
Амплитуда движений в тазобедренных, коленных и голеностопных суставах не ограничена
Левая стопа: укорочение и латеральная девиация пятой плюсневой кости, пятый палец отведен, расщепление в четвертом межпальцевом промежутке до уровня плюсневых костей (рис. 4, а; рис. 5). Изменений со стороны кожных покровов не отмечается.
Правая стопа представлена тремя пальцами. Второй и третий пальцы в положении приведения, первый палец отведен, располагается по тыльной поверхности стопы, имеется расщепление в первом межпальцевом промежутке до уровня клиновидных костей. Второй палец располагается по подошвенной поверхности стопы, имеется клинодактилия средней фаланги, сгибательная контрактура в дистальном межфаланговом суставе. Под головкой второй плюс-невой кости – жировая подушка, свидетельствующая о максимальной нагрузке на данный сегмент при опоре. Стопа без нагрузки находится в положении супинации (рис. 4, б; рис. 5).
На основании результатов обследования и дифференциальной диагностики ребенку по совокупности клинических признаков установлен диагноз синдрома
Горлина-Гольца.
По поводу расщепления правой кисти ребенку в возрасте 7,5 месяцев выполнено реконструктивное мягкотканное вмешательство, направленное на формирование нормальной анатомии и восстановление функции конечностиВ возрасте 1,5 лет в связи с затруднением подбора и ношения обуви, неустойчивостью в опорную фазу шага пациентке были выполнены реконструктивные вмешательства на стопах.
На левой стопе из-за значительного укорочения пятой плюсневой кости и глубокого расщепления наружного межпальцевого промежутка произведено удаление пятого луча.
Сухожилие короткой малоберцовой мышцы транспонировано на наружный край резецированной кубовидной кости.
На правой стопе выполнено формирование первого межпальцевого промежутка с устранением расщепления. В качестве костного мостика между первой и второй плюсневыми костями использован аутотрансплантат, сформированный из удаленной плюсневой кости левой стопы. Соблюдено соответствие ширины и объема стоп, что позволит ребенку в дальнейшем пользоваться стандартной обувью (рис. 6).
2. Пациентка П., 11 лет, поступила с диагнозом:врожденная деформация кистей и стоп.
Из анамнеза известно, что ребенок от второй беременности, первых срочных родов, протекавших без особенностей. О наличии наследственных заболеваний в роду данных нет. При осмотре неврологом выявлена задержка психомоторного развития.
Девочка ходит самостоятельно, хромая на правую ногу. На коже туловища пигментные пятна светло-малинового цвета с элементами телеангиоэктазий, расположенные в области крупных сосудисто-нервных пучков, втяжения кожных покровов (рис. 7).
Голова неправильной формы, располагается по средней линии. Лобные бугры увеличены. Отмечается деформация ушных раковин.
Ось позвоночника правильная. Амплитуда движений в суставах верхних конечностей не ограничена.
Правая кисть: состояние после оперативного лечения тотальной синдактилии второго-третьего пальцев.
Левая кисть: состояние после устранения тотальной синдактилии третьего-четвертого пальцев (рис. 8). Послеоперационные рубцы эластичные, смещаемые, без
изменения цвета кожных покровов. На ладонной поверхности имеются незначительные втяжении кожи. Амплитуда движений в тазобедренных, коленных и
голеностопных суставах не ограничена.
Левая стопа представлена двумя лучами. Расщепление в первом межпальцевом промежутке до уровня клиновидных костей. Первый и пятый пальцы приведены (рис. 9, 10).
Плюсневые кости длинные, располагаются на одинаковом уровне. Правая стопа представлена пятью пальцами, второй и третий пальцы в тотальной синдактилии (рис. 9, 10).
На основании результатов проведенных обследований и дифференциальной диагностики пациентке клинически установлен диагноз синдрома Горлина-Гольца.
Девочке проведено устранение расщепления левой стопы с формированием костного мостика между первой и пятой плюсневыми костями с использованием кортикального костного аллотрансплантата для расширения переднего отдела стопы, устранения приведения пальцев и улучшения возможностей в подборе и ношении обуви.
Необходимо отметить, что сроки приживления костных трансплантатов у обеих пациенток были стандартными. Заживление послеоперационных ран (в область разрезов не попадали измененные кожные покровы) было первичным натяжением, без трофических нарушений, в обычные сроки.
ЗАКЛЮЧЕНИЕ
Пороки развития кистей и стоп могут встречаться как в виде изолированных аномалий, так и являться проявлением различных генетических заболеваний.
Сочетание синдактилии пальцев кисти и расщепления стоп с изменением цвета кожных покровов в виде широких полос (аналогично линиям Блашко), расположенных по ходу крупных сосудисто-нервных пучков, кожными втяжениями, опухолевидными образованиями, увеличением лобных бугров и другими изменениями дает основание подозревать у пациента синдром Горлина-Гольца, что требует углубленного неврологического, соматического и генетического обследований.
Хирургическое вмешательства по поводу ортопедической патологии у данной категории больных должно проводиться в соответствии с основными принципами лечения детей с ортопедическими заболеваниями, при этом необходимо принимать во внимание характер и степень поражения других органов и систем. Наш опыт лечения двух пациентов с таким редким генетическим заболеванием, как синдром Горлина-Гольца показывает, что при соблюдении хирургической техники риск осложнений оперативного лечения не превышает таковой при изолированных пороках. Настороженность в отношении наследственной сочетанной патологии и своевременное медико-генетическое консультирование позволяют выявлять наследственные синдромы, что важно для определения прогноза заболевания и выбора тактики лечения.
ЛИТЕРАТУРА
1.Маланчук В.А., Копчак А.В., Ковнацкий О.Л. Синдром Горлина-Гольц : клиническая картина и описание случая // Украинский мед. журн. online. 2008. No 1(63)
2.Молочков В.А., Писклакова Т.П., Манишкина Р.П. Особенности системы HLA у больных с множественными базалиомами кожи и синдромом Горлина-Гольтца // Рос. журн. кожных и венер. болезней. 2000. No 2. С. 11-17.
3.Мордовцев В.Н. Наследственные болезни и пороки развития кожи: атлас. М.: Наука, 2004. 174 с.
4.Клиническое наблюдение больного с синдромом Горлина-Гольца / А.А. Никитин, В.П. Лапшин, М.Н. Косяков, Н.В. Титова // Клин. стоматология. 2008. No 2. С. 52-55.
5.Никитин А.А., Лапшин В.П., Косяков М.Н. Особенности лечения одонтогенных кератокист и множественных базалиом у больных синдромом Горлина-Гольтца // Воен.-мед. журнал. 2009. No 2. С. 75-76.
6.Панова И. Е., Важенин А. В., Усова Р. А. Эпидемиология, клинико-морфологическая характеристика, дифференциальная диагностика базально-клточного рака кожи век : учеб. пособие. Челябинск, 2003. 14 с.
7.Побилат А. Е., Прохоренков В. И., Карачева Ю. В. Применение дерматоскопии в диагностике синдрома Горлина-Гольца // Клин. дерматология и венерология. 2009. No 5. С. 82-84.
8.Nevoid basal cell carcinoma syndrome: relation with desmoplastic medulloblastoma in infancy. A population-based study and review of the literature / S.F. Amlashi, L. Riffaud, G. Brassier, X. Morandi // Cancer. 2003. Vol. 98, No 3. P. 618-624.
9.Friedlander A.H., Herbosa E.G., Peoples J.R. 3rd. Ocular hypertelorism, facial basal cell carcinomas, and multiple odontogenic keratocysts of the jaws // J. Am. Dent. Assoc. 1988. Vol. 116, No 7. P. 887-889.
10.Nevoid Basal cell carcinoma syndrome with medulloblastoma and meningioma – case report / Y. Fukushima, H. Oka, S. Utsuki, K. Iwamoto, K. Fujii // Neurol. Med. Chir (Tokyo). 2004. Vol. 44, No 12. P. 665-668.
11.Gorlin R.J., Goltz R.W. Multiple nevoid basal-cell epithelioma, jaw cysts and bifid rib. A syndrome // N. Eng. J. Med. 1960. Vol. 262. P. 908-912.
12.Gorlin R.J. Nevoid basal cell carcinoma (Gorlin) syndrome // Genet. Med. 2004. Vol. 6, No 6. P. 530-539.
13.Jarisch W. Zur lehre von den Hautgeschwulsten // Arch. Dermatol. Syphil. 1894. No 28. S. 163-222.
14.Human homolog of patched, a candidate gene for the basal cell nevus syndrome / R.L. Johnson, A.L. Rothman, J. Xie, L.V. Goodrich, J.W. Bare, J.M. Bonifas, A.G. Quinn, R.M. Myers, D.R. Cox, E.H. Jr Epstein, M.P. Scott // Science. 1996. Vol. 272, No 5268. P. 1668-1671.
15.Radiological features in 82 patients with nevoid basal cell carcinoma (NBCC or Gorlin) syndrome / V.E. Kimonis, S.G. Mehta, J.J. Digiovanna, S.J. Bale, B. Pastakia // Genet. Med. 2004. Vol. 6, No 6. P. 495-502.
16.Lo Muzio L. Nevoid basal cell carcinoma syndrome (Gorlin syndrome) // Orphanet. J. Rare Dis. 2008. Vol. 3. P. 32.
17.The odontogenic keratocyst: a 20-year clinicopathologic review / J.G. Meara, S. Shah, K.K. Li, M.J. Cunningham // Laryngoscope. 1998. Vol. 108, No 2. P. 280-283.
18.Gorlin-Goltz syndrome with odontogenic keratosis. Report on a patient followed for 10 years / T. Sabbia, S. Bovone, A. Camera, C. Gambini, P. Balbi // Minerva Stomatol. 1994. Vol. 43, No 7-8. P. 359-363.
19.Wang S.Q., Goldberg L.H. Multiple polypoid basal cell carcinomas on the perineum of a patient with basal cell nevus syndrome // J. Am. Acad. Dermatol. 2007. Vol. 57, Suppl. No 2. P. S36-37.
20.White J.C. Multiple benign cystic epitheliomas // J. Cutan. Genitourin. Dis. 1894. Vol. 12. P. 477-484.
Сведения об авторах:
1. Коваленко-Клычкова Надежда Александровна – ФГБУ «НИДОИ им. Г.И. Турнера», г. Санкт-Петербург, очный аспирант отделения патологии стопы, нейроортопедии и системных заболеваний
2. Кенис Владимир Маркович – ФГБУ «НИДОИ им. Г.И. Турнера», руководитель отделения патологии стопы, нейроортопедии и системных заболеваний
3. Клычкова Ирина Юрьевна – ФГБУ «НИДОИ им. Г.И. Турнера», г. Санкт-Петербург, заведующая отделением патологии стопы, нейроортопедии и системных заболеваний, г. Санкт-Петербург
4. Авдейчик Наталья Валерьевна – ФГБУ «НИДОИ им. Г.И. Турнера», г. Санкт-Петербург, врач отделения патологии кисти и микрохирургии
Теги: дисплазия
234567
Начало активности (дата): 16.01.2021 16:53:00
234567
Кем создан (ID): 989
234567
Ключевые слова:
дермальная дисплазия, пороки развития кистей и стоп, системные заболевания скелета и кожи
12354567899
Источник
