Что такое жировой синдром печени
Жировой гепатоз – это вторичный или самостоятельный патологический синдром, характеризующийся накоплением жира в ткани печени. Причиной развития данного состояния является употребление алкоголя; заболевания, сопровождающиеся метаболическими нарушениями (сахарный диабет, патология щитовидной железы, мальабсорбция и другие), а также прием некоторых лекарственных препаратов. Жировой гепатоз не имеет специфической клинической картины и длительное время протекает бессимптомно. Диагностика заключается в проведении биопсии печени, а также визуализирующих исследований (МРТ печени, сцинтиграфии, УЗИ). Лечение консервативное, прогноз благоприятный.
Общие сведения
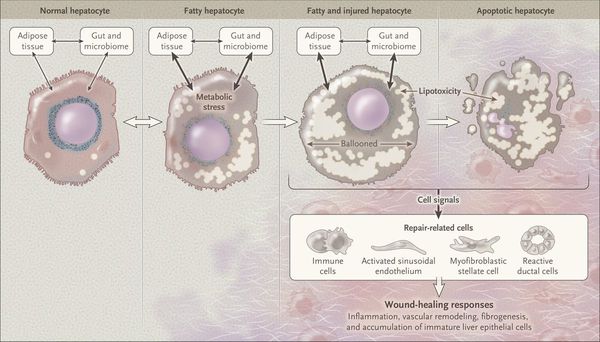
Жировой гепатоз – патологический процесс, заключающийся в перерождении печеночной ткани с жировой дистрофией гепатоцитов. Морфологические изменения характеризуются внутриклеточным и/или межклеточным накоплением капель жира. Данная патология встречается у трети пациентов с неалкогольной жировой болезнью печени и у большинства больных с алкогольным поражением.
Жировой гепатоз является начальным этапом алкогольной болезни печени и может привести к необратимым цирротическим изменениям и летальному исходу. В настоящее время жировой гепатоз считается глобальной проблемой не только гастроэнтерологии, но и интегральной медицины, поскольку данное заболевание связано с повышенным риском развития цирроза печени, сердечно-сосудистой патологии, эндокринных и обменных нарушений, аллергическими заболеваниями, варикозной болезнью и другими тяжелыми изменениями.
Жировой гепатоз
Причины
Этиологические факторы жирового гепатоза многообразны и разноплановы. Дистрофические изменения гепатоцитов могут развиваться вследствие токсического воздействия, особенностей питания, нарушений углеводного и жирового метаболизма. Нарушения питания, прием алкоголя, использование лекарственных препаратов – факторы, которые имеют место практически у каждого пациента. Среди основных причин рассматриваются:
- Употребление алкоголя. Важнейшим фактором развития жировой дистрофии печени является алкогольное повреждение гепатоцитов. Выраженность морфологических изменений и риск перехода в цирроз напрямую зависят от количества и продолжительности употребления алкогольных напитков.
- Прием лекарственных препаратов. Токсическое действие на печень оказывают кортикостероиды, синтетические эстрогены, нестероидные противовоспалительные средства, метотрексат, антибиотики (тетрациклин).
- Сахарный диабет. Гипергликемия с инсулинорезистентностью приводят к повышению концентрации свободных жирных кислот в крови, вследствие чего в печени усиливается синтез триглицеридов. Если скорость их образования превышает обменные реакции с формированием комплексов ЛПОНП-ТГ, происходит отложение жиров в печени.
- Ожирение. Главную роль играет не процент жировой ткани в организме, а возникающая при метаболическом синдроме инсулинорезистентность. В проведенных исследованиях количество жира в печени, определяемое методом протонной спектроскопии, напрямую зависело от уровня инсулина натощак.
- Другие нарушения обмена веществ. Причинами жирового гепатоза могут быть и другие заболевания, сопровождающиеся метаболическими нарушениями: микседема, синдром Иценко-Кушинга, тиреотоксикоз, хронические заболевания желудочно-кишечного тракта с нарушением всасывания (в том числе хронический панкреатит), болезнь Вильсона-Коновалова, патология сердечно-сосудистой системы (гипертоническая болезнь, ишемическая болезнь сердца), иные хронические болезни, приводящие к истощению пациента (онкопатология, легочная и сердечная недостаточность).
- Особенности питания. К нарушению метаболизма жиров, углеводов и жировой дистрофии гепатоцитов приводит и так называемая «западная» диета – питание с высоким содержанием гидрогенизированных жиров, простых углеводов, а также образ жизни с низким уровнем физической активности.
- Наследственные энзимопатии. Отдельная группа факторов, способствующих накоплению жира в печени, – наследственный дефицит ферментов, участвующих в метаболизме липидов. Зачастую выявить этиологический фактор невозможно, поскольку не бывает чистого повреждения печени того или иного генеза.
Патогенез
Кезависимо от первичной причины заболевания, при жировом гепатозе (особенно неалкогольной этиологии) имеет место инсулинорезистентность, в свою очередь, дистрофические изменения в печени являются одним из патогенетических звеньев метаболического синдрома. Накопление жира в гепатоцитах и между ними обусловлено избыточным поступлением жиров вследствие гиперлипидемии или алкогольного поражения, нарушением их утилизации в процессе перекисного окисления, а также сниженным выведением молекул жиров из клеток вследствие нарушения синтеза апопротеина, образующего транспортные формы жиров (этим объясняется алипотропное ожирение печени).
Классификация
Выделяют две формы жирового гепатоза, являющиеся самостоятельными нозологическими единицами: алкогольную жировую дистрофию печени и неалкогольный стеатогепатит. Среди всех пациентов, которым проводится биопсия печени, неалкогольный стеатоз регистрируется в 7-8% случаев. Алкогольное поражение более распространено – встречается в 10 раз чаще.
В зависимости от типа отложения жира в дольке печени различают следующие морфологические формы: очаговую диссеминированную (зачастую не имеет клинических проявлений), выраженную диссеминированную, зональную (жир накапливается в разных отделах печеночной дольки) и диффузную (микровезикулярный стеатоз).
Жировой гепатоз классифицируют на:
- Первичный. Обусловлен эндогенными метаболическими нарушениями (ожирение, сахарный диабет, гиперлипидемия).
- Вторичный. Его причиной являются внешние воздействия, на фоне которых развиваются обменные нарушения. К вторичному гепатозу относят поражение печени при приеме некоторых лекарственных препаратов, синдроме мальабсорбции при оперативных вмешательствах на органах ЖКТ (илео-еюнальный анастомоз, гастропластика как метод лечения ожирения, резекция отделов кишечника); при длительном парентеральном питании, голодании и т. д.
Симптомы жирового гепатоза
Сложность данной патологии заключается в том, что, несмотря на значительные морфологические изменения, у большинства пациентов отсутствуют специфические клинические признаки. 65-70% пациентов – женщины, причем большинство из них имеют избыточный вес. У многих больных имеет место инсулиннезависимый сахарный диабет. У подавляющего большинства пациентов отсутствуют симптомы, характерные для поражения печени.
Возможно неопределенное ощущение дискомфорта в брюшной полости, слабо выраженные ноющие боли в области правого подреберья, астенизация. Печень увеличена, при пальпации может быть незначительно болезненна. Иногда заболевание сопровождается диспепсическим синдромом: тошнотой, рвотой, нарушением стула. Возможна некоторая желтушность кожных покровов. При диффузном поражении печени могут возникать эпизоды геморрагий, гипотензия, обморочные состояния, что объясняется высвобождением в результате воспалительного процесса туморонекротизирующего фактора.
Диагностика
Клинические симптомы неспецифичны, консультация гепатолога позволяет предположить жировой гепатоз и определить диагностическую тактику. Биохимические пробы печени также не выявляют существенных изменений, сывороточные трансаминазы могут быть повышены в 2-3 раза, при этом их нормальные показатели не исключают наличие жирового гепатоза. Основные методы диагностики направлены на исключение других заболеваний печени:
- Анализы крови. Обязательно проводится исследование крови на наличие специфических антител к возбудителям вирусных гепатитов, цитомегаловирусу, вирусу Эпштейна-Барр, краснухи; определение маркеров аутоиммунного повреждения печени. Исследуется уровень гормонов щитовидной железы в крови, поскольку гипотиреоз может быть причиной жирового гепатоза.
- УЗИ органов брюшной полости. Позволяет выявить признаки жирового стеатоза, если поражение охватывает более трети ткани печени.
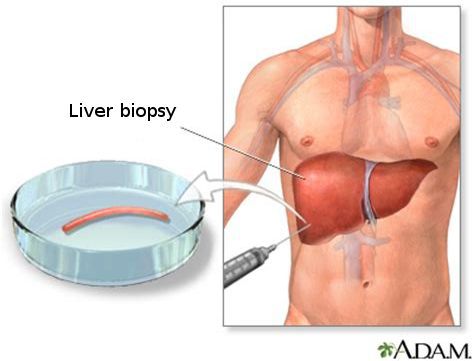
- Биопсия печени. Важная роль отводится биопсии печени с морфологическим исследованием биоптата. Гистологические признаки жирового гепатоза включают явления жировой дистрофии, внутридолькового воспаления, фиброза, стеатонекроза. Чаще всего выявляется наличие крупнокапельной дистрофии.
- Методы визуализации и оценки функции. Высокоинформативный метод диагностики, позволяющий обнаружить изменения паренхимы, – МРТ печени. Для выявления очагового стеатоза применяют радионуклидное сканирование печени, КТ.
Диагностическая программа обязательно включает методы оценки сопутствующих заболеваний, которые влияют на прогрессию повреждения печени и прогноз для пациента. С целью оценки детоксикационной функции печени проводят С13-метацетиновый дыхательный тест. Результаты данного исследования позволяют судить о количестве функционирующих гепатоцитов.

КТ органов брюшной полости. Диффузное снижение плотности печени до +15 ед. Хаунсфилда.
Лечение жирового гепатоза
Лечение пациентов проводится амбулаторно или в отделении гастроэнтерологии. Лечение консервативное, проводится в нескольких направлениях. Обязательно оценивается алиментарный статус и назначается диетотерапия. С целью уменьшения действия основного патогенетического фактора (инсулинорезистентности) обязательна коррекция избыточной массы тела. Потеря даже 5-10% массы тела приводит к значительному улучшению углеводного и жирового обмена. Однако скорость похудения должна составлять 400-700 г в неделю, более быстрое снижение веса может привести к прогрессированию жирового гепатоза и развитию печеночной недостаточности, а также формированию конкрементов в желчном пузыре. Основные направления:
- Диетотерапия. В некоторых случаях именно диета является ключевым и единственным методом лечения жирового гепатоза. Лечебное питание предусматривает ограничение животных жиров, употребление белка в количестве 100-110 г в сутки, достаточное поступление витаминов и микроэлементов.
- Гиполипидемическая терапия. Применяются липотропные препараты, которые устраняют жировую инфильтрацию печени: фолиевая кислота, витамин В6, В12, липоевая кислота, эссенциальные фосфолипиды. Однако окончательно не установлено, безопасен ли прием статинов при жировом гепатозе, поскольку данные препараты сами обладают способностью повреждать гепатоциты.
- Гепатопротектекция. Для нормализации функций печени назначаются гепатопротекторы. Применяется витамин Е, урсодезоксихолевая кислота, бетаин, таурин. Проводятся исследования эффективности пентоксифиллина и блокаторов рецепторов ангиотензина при данной патологии.
- Снижение инсулинорезистентности. Для повышения активности процессов окислительного фосфорилирования в мышцах, а, следовательно – утилизации жирных кислот, показаны физические нагрузки, которые также улучшают чувствительность рецепторов к инсулину. Фармакотерапия инсулинорезистентности проводится с использованием тиазолидиндионов и бигуанидов.
Таким образом, ключевыми моментами лечения жирового гепатоза являются устранение этиологического фактора (в том числе употребления алкоголя), нормализация веса и питания. Медикаментозная терапия имеет вспомогательное значение. Для пациентов, страдающих алкоголизмом, первоочередным является лечение у нарколога.
Прогноз и профилактика
Жировой гепатоз имеет относительно благоприятный прогноз. В большинстве случаев устранения причины заболевания достаточно для восстановления печени. Трудоспособность пациентов сохранена. Обязательно следует выполнять рекомендации гастроэнтеролога по режиму питания, физической активности, исключить употребление алкоголя. В случае продолжающегося действия гепатотропных факторов воспалительные и дистрофические изменения печени прогрессируют, возможен переход заболевания в цирроз.
Профилактика состоит в исключении действия токсических повреждающих факторов, в том числе ацетальдегида, своевременном выявлении эндокринных и других заболеваний и их эффективном лечении , поддержании нормального веса и достаточного уровня активности.
Источник
Над статьей доктора
Васильева Романа Владимировича
работали
литературный редактор
Маргарита Тихонова,
научный редактор
Сергей Федосов
Дата публикации 23 июля 2018Обновлено 19 июля 2019
Определение болезни. Причины заболевания
Неалкогольная жировая болезнь печени / НАЖБП (стеатоз печении или жировой гепатоз, неалкогольный стеатогепатит) — это неинфекционное структурное заболевание печени, характеризующееся изменением ткани паренхимы печени вследствие заполнения клеток печени (гепатоцитов) жиром (стеатоз печени), которое развивается из-за нарушения структуры мембран гепатоцитов, замедления и нарушения обменных и окислительных процессов внутри клетки печени.
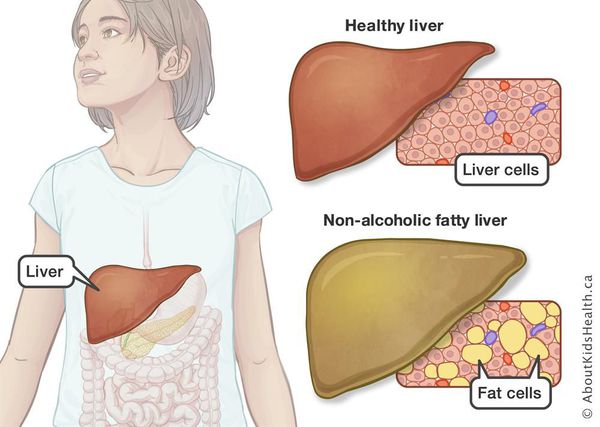
Все эти изменения неуклонно приводят к:
- разрушению клеток печени (неалкогольный стеатогепатит);
- накоплению жировой и формированию фиброзной ткани, что вызывает уже необратимые, структурные (морфологические) изменения паренхимы печени;
- изменению биохимического состава крови;
- развитию метаболического синдрома (гипертоническая болезнь, ожирение, сахарный диабет);
- в конечном итоге, циррозу.
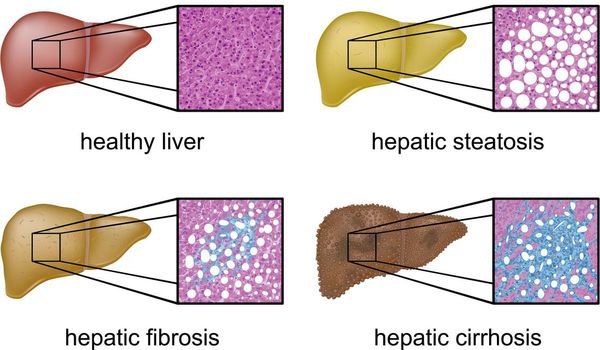
Метаболический синдром — широко распространённое состояние, характеризующееся снижением биологического действия инсулина (инсулинорезистентность), нарушением углеводного обмена (сахарный диабет II типа), ожирением центрального типа с дисбалансом фракций жира (липопротеинов плазмы и триглицеридов) и артериальной гипертензией.[2][3][4]
В большинстве случаев НАЖБП развивается после 30 лет.[7]
Факторами риска данного заболевания являются:
- малоподвижный образ жизни (гиподинамия);
- неправильное питание, переедание;
- длительный приём лекарственных препаратов;
- избыточная масса тела и висцеральное ожирение;
- вредные привычки.
Основными причинам развития НАЖБП являются:[11]
- гормональные нарушения;
- нарушение жирового обмена (дисбаланс липопротеидов плазмы);
- нарушение углеводного обмена (сахарный диабет);
- артериальная гипертензия;
- ночная гипоксемия (синдром обструктивного апноэ сна).
При наличии гипертонической болезни, ожирения, сахарного диабета, регулярном приёме лекарств или в случае присутствия двух состояний из вышеперечисленных вероятность наличия НАЖБП достигает 90 %.[3]
Ожирение определяется по формуле вычисления индекса массы тела (ИМТ): ИМТ = вес (кг) : (рост (м))2. Если человек, например, весит 90 кг, а его рост — 167 см, то его ИМТ = 90 : (1,67х1,67) = 32,3. Этот резултат говорит об ожирении I степени.
- 16 и менее — выраженный дефицит массы;
- 16-17,9 — недостаточная масса тела;
- 18-24,9 — нормальный вес;
- 25-29,9 — избыточная масса тела (предожирение);
- 30-34,9 — ожирение I степени;
- 35-39,9 — ожирение II степени;
- 40 и более — ожирение III степени (морбидное).
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением – это опасно для вашего здоровья!
Симптомы жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
У большинства больных данное заболевание на ранних стадиях протекает бессимптомно — в этом и заключается большая опасность.
У 50-75% больных могут появляться симптомы общей (хронической) усталости, снижение работоспособности, недомогание, слабость, тяжесть в области правого подреберья, набор веса, длительное повышение температуры тела без всякой причины, красные точки на коже в области груди и живота. Печень часто увеличена. Возникают расстройства пищеварения, повышенное газообразование, кожный зуд, редко — желтуха, «печёночные знаки».
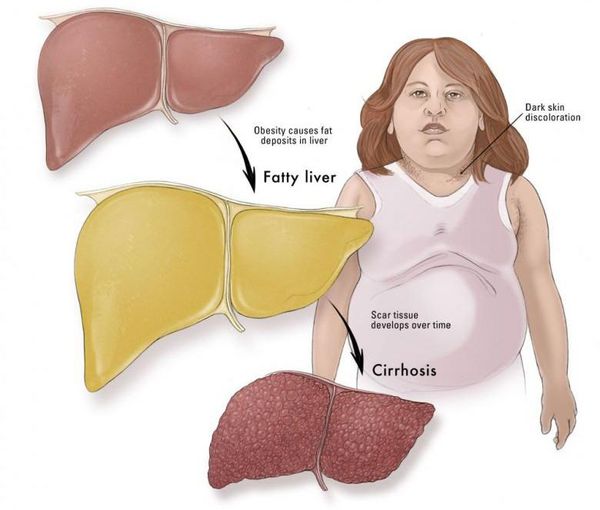
Часто НАЖБП сопутствуют заболевания желчного пузыря: хронический холецистит, желчнокаменная болезнь. Реже, в запущенных случаях, возникают признаки портальной гипертензии: увеличение селезёнки, варикозное расширение вен пищевода и асцит (скопление жидкости в брюшной полости). Как правило, данные симптомы наблюдаются на стадии цирроза печени.[7]
Патогенез жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
К накоплению холестерина, а именно липидов (жироподобных органических соединений) в печени, приводят, прежде всего, следующие факторы:
- избыточное поступление свободных жирных кислот (FFA) в печень;
- усиленный синтез свободных жирных кислот печени;
- пониженный уровень бета-окисления свободных жирных кислот;
- снижение синтеза или секреции липопротеинов очень высокой плотности.[7]
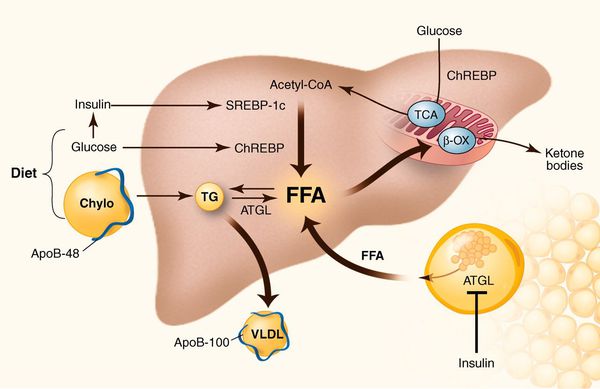
У пациентов с ожирением в ткани печени повышенно содержание свободных жирных кислот, что и может быть причиной нарушения функций печени, так как жирные кислоты химически активны и могут привести к повреждению биологических мембран гепатоцитов, образуя в них ворота для поступления в клетку эндогенного жира, в частности липидов (преимущественно низкой и очень низкой плотности), а транспортом является сложный эфир — триглицерид.[2]
Таким образом, гепатоциты заполняться жиром, и клетка становиться функционально неактивной, раздувается и увеличивается в размерах. При поражении более миллиона клеток макроскопически печень увеличивается в размерах, в участках жировой инфильтрации ткань печени становиться плотнее, и данные участки печени не выполняют своих функций либо выполняют их с существенными дефектами.
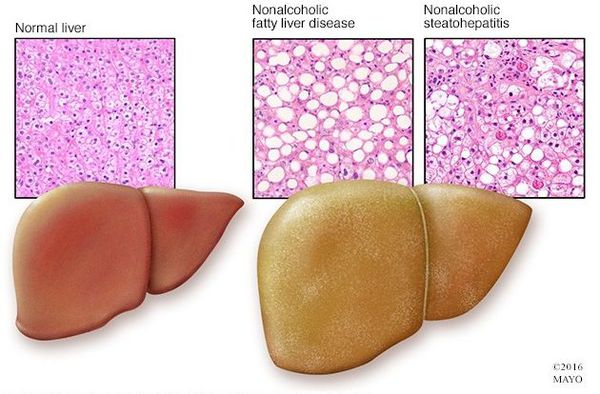
Перекисное окисление липидов в печени приводит к синтезу токсичных промежуточных продуктов, которые могут запускать процесс апоптоза (запрограммированной гибели) клетки, что может вызывать воспалительные процессы в печени и сформировать фиброз.[2]
Также важное патогенетическое значение в формировании НАЖБП имеет индукция цитохрома P-450 2E1 (CYP2E1), который может индуцироваться как кетонами, так и диетой с высоким содержанием жиров и низким содержанием углеводов.[7] CYP2E1 генерирует токсические свободные радикалы, приводящие к повреждению печени и последующему фиброзу.
Кроме того, патогенетическое значение в формировании НАЖБП имеет эндотоксин-опосредованное повреждение, которое, в свою очередь, усиливает выработку провоспалительных цитокинов (ФНО-α, ИЛ-6 и ИЛ-8), приводящих к нарушению целостности мембран гепатоцитов и даже к их некрозу[9], а также к развитию воспалительной клеточной инфильтрации как в портальных трактах, так и в дольках печени, что приводит к стеатогепатиту.

Продукты перекисного окисления липидов, некрозы гепатоцитов, ФНО и ИЛ-6 активируют стеллатные (Ito) клетки, вызывающие повреждение гепатоцитов и формирование фиброзных изменений.
Классификация и стадии развития жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
В настоящий момент общепринятой классификации НАЖБП не существует, однако ряд авторов выделяет стадии течения заболевания и степени неалкогольного стеатогепатита (НАСГ).
Оценка стеатоза печени и гистологической активности НАЖБП по системе E.M. Brunt:[9][10][11]
- I степень (мягкий НАСГ) — стеатоз крупнокапельный, не более 33-66% поражённых гепацитов;
- II степень (умеренный НАСГ) — крупно- и мелкокапельный, от 33% до 66% поражённых гепацитов;
- III степень (тяжелый НАСГ) — крупно- и мелкокапельный, больше 60% поражённых гепацитов.
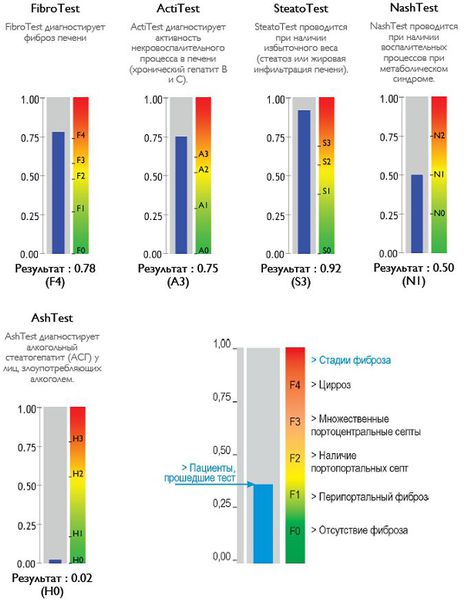
Также можно условно разделить степени стеатоза, фиброза и некроза по результату теста ФиброМакс — степени выраженности жировой инфильтрации:
- S1 (до 33% жировой инфильтрации);
- S2 ( 33-60% жировой инфильтрации)
- S3 (более 60% жировой инфильтрации)
- F1,F2, F3, цирроз.
Осложнения жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
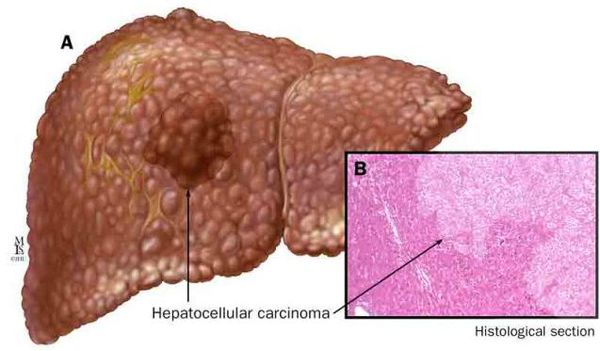
Наиболее частые осложнения НАЖБП — это гепатит, замещение нормальной паренхиматозной ткани печени фиброзной — функционально нерабочей тканью с формированием в конечном итоге цирроза печени.
К более редкому осложнению, но всё же встречающемуся, можно отнести рак печени — гепатоцеллюлярную карциному.[9] Чаще всего она встречается на этапе цирроза печени и, как правило, ассоциируется с вирусными гепатитами.
Диагностика жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
В диагностике НАЖБП используются лабораторные и инструментальные методы исследования.
В первую очередь оценивается состояние печени на предмет воспалительных изменений, инфекционных, аутоиммунных и генетических заболеваний (в том числе болезней накопления) с помощью общеклинических, биохимических и специальных тестов.[7]
Далее проводится оценка выполняемых печенью функций (метаболическая/обменная, пищеварительная, детоксикационная) по способности выработки определённых белков, характеристикам жиров и углеводов. Детоксикационная функция печени оценивается преимущественно при помощи С13-метацетинового теста и некоторых биохимических тестов.
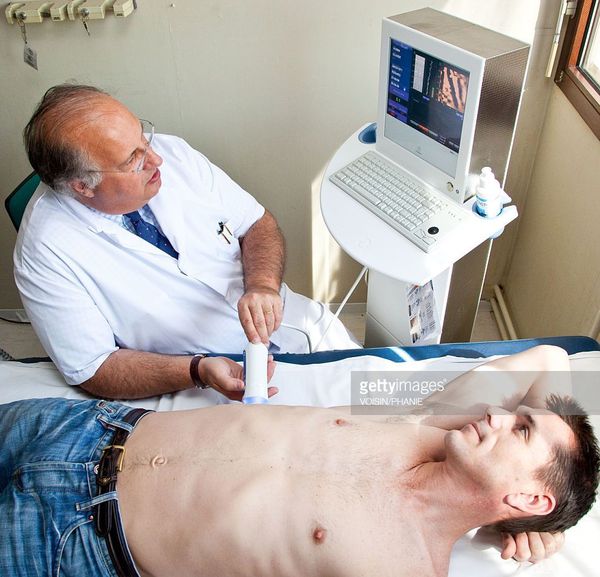
Кода первые два этапа завершены, исследуется структурное состояние печени при помощи УЗИ[4], МСКТ, МРТ и эластометрии (FibroScan), при необходимости исследуется морфологическое состояние — биопсия печени.[3]
С помощью эластометрии исследуется эластичность мягких тканей. Злокачественные опухоли отличаются от доброкачетсвенных повышенной плотностью, неэластичностью, они с трудом поддаются компрессии. На мониторе FibroScan более плотные ткани окрашены в голубой и синий цвет, жировая ткань — жёлто-красный, а соединительная ткань — зелёный. Высокая специфичность метода позволяет избежать необоснованных биопсий.
После проведённой диагностики, устанавливается окончательный диагноз и проводится соответствующее лечение.
Лечение жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
С учётом механизма развития заболевания разработаны схемы курсового лечения НАЖБП, направленные на восстановление структуры клеточных мембран, обменных и окислительных процессов внутри клеток печени на молекулярном уровне, очистку печени от внутриклеточного и висцерального жира, который затрудняет её работу.
В процессе лечения производится:
- коррекция углеводного, жирового (липидного) обмена веществ;
- нормализация процессов окисления в клетке;
- влияние на основные факторы риска;
- снижение массы тела;
- улучшение структуры печени на обратимых стадиях.
После лечения наступает заметное улучшение дезинтоксикационной (защитной), пищеварительной и метаболической (синтетической) функции печени, пациенты теряют в весе, улучшается общее самочувствие, повышается умственная и физическая работоспособность.
Курсовые программы лечения занимают от трёх до шести месяцев и подбираются в зависимости от степени выраженности метаболических нарушений. К ним относятся:
- программа «Лайт»;
- программа «Медиум»;
- программа «Премиум»;
- индивидуальная программа лечения — разрабатывается на основании сопутствующих заболеваний, текущего состояния пациента и необходимой интенсивности лечения.
Программы включают в себя предварительное обследование, постановку диагноза и медикаментозное лечение, которое состоит из двух этапов:
- инфузионная терапия с пролонгацией приёма препаратов внутрь, подбор диеты и физической активности;
- сдача контрольных анализов и оценка результатов.
Прогноз. Профилактика
На ранних стадиях заболевания прогноз благоприятный.
Профилактика НАЖБП предполагает правильное питание, активный образ жизни и регулярную календарную диспансеризацию.
К правильному питанию можно отнести включение в свой рацион питания омега-3 полиненасыщенных жирных кислот, коротких углеводов, ограничение потребления приправ, очень жирной и жаренной пищи. Разнообразие рациона питания также является ключевым моментом полноценного питания. Показано потребление продуктов, богатых растительной клетчаткой.
Для активного образа жизни достаточно ходить пешком от 8 000 до 15 000 шагов в сутки и уделять три часа в неделю физическим упражнениям.
В отношении календарной диспансеризации следует ежегодно выполнять УЗИ органов брюшной полости и оценивать уровень своих печёночных ферментов (АЛТ, АСТ, общий билирубин), особенно при приёме каких-либо лекарственных препаратов на постоянной основе.
Источник
