Двс синдром при кесарево сечении

При выполнении кесарева сечения могут возникнуть трудности и осложнения: рубцово-спаечный процесс (после абдоминального родоразрешения и реконструктивно-пластических операций на матке), который может значительно осложнять вхождение в брюшную полость и стать причиной ранения мочевого пузыря и кишечника; трудности при выведении головки плода; кровотечения после извлечения плода, а также аспирационный синдром, синдром аортокавальной компрессии, тромбоэмболические осложнения, эмболия околоплодными водами, острый ДВС-синдром.
Рубцово-спаечный процесс
Четкое знание топографической анатомии и строго послойное вскрытие брюшной полости позволяют избежать осложнений, обусловленных рубцово-спаечным процессом. При ранении мочевого пузыря производят его ушивание двухрядными викриловыми швами, а в послеоперационном периоде оставляют постоянный катетер в мочевом пузыре на 5 сут, регулярно промывают его антисептиками с обязательным применением препаратов нитрофуранового ряда. В случае повреждения стенки кишки восстановить ее должен хирург, владеющий техникой данной операции.
Трудности при выведении головки плода
Выведение головки плода чаще всего затрудняется при недостаточно длинном или слишком высоко произведенном разрезе матки, а длительные манипуляции с головкой плода могут привести к травмам шейно-грудного отдела позвоночника плода [Савельева Г.М. и др., 1989]. Для того чтобы избежать этого осложнения, нужно производить достаточно большой разрез на матке — не менее 10— 12 см, сопоставимый с большим сегментом головки плода [Козаченко В.П., 1979; Персианинов Л.С. и др., 1979; Серов В.Н. и др., 1989].
Кровотечение
Кровотечение в ходе выполнения кесарева сечения может быть обусловлено ранением сосудистого пучка или гипотонией матки. Повреждение восходящей ветви маточной артерии происходит при извлечении крупного плода, несостоятельности рубца на матке либо в результате недоучета топографического положения матки, т.е. разрез ротированной матки производят не в центре нижнего сегмента, а ближе к одному из ее ребер (чаще левому) и он переходит на сосудистый пучок.
Мерой профилактики данного осложнения является выполнение разреза матки строго по центру нижнего сегмента и дугообразно вверх; в ряде случаев (при рубцовых изменениях нижнего сегмента матки) возможно вскрытие матки в латеральных отделах по методу Дерфлера. При повреждении сосудистого пучка следует перевязать восходящую ветвь маточной артерии, а иногда при продолжающемся кровотечении возникает необходимость в перевязке внутренней подвздошной артерии или даже удалении матки.
При возникновении гипотонического кровотечения следует повторно ввести утеротонические препараты, произвести массаж матки, при необходимости наложить зажимы на магистральные сосуды (маточные, яичниковые артерии) и быстро ушить рану матки [Серов В.Н. и др., 1997]. Окончательно судить об эффективности данных мероприятий можно только при зашитой матке. В случае их неэффективности показано удаление матки — надвлагалищная ампутация, а при явлениях коагулопатии — экстирпация [Чернуха Е.А., 1990; Серов В.Н. и др., 1997].
Если кровотечение возникает в раннем послеоперационном периоде, то некоторые авторы допускают возможность осторожного выскабливания матки большой тупой кюреткой в расчете на то, что при этом будут удалены задержавшиеся дольки плаценты и децидуальная оболочка, которые явились причиной снижения тономоторной функции матки [Слепых А.С., 1986; Чернуха Е.А., 1990; Petiti T.J., 1985]. При неэффективности данных мероприятий показаны релапаротомия и удаление матки.
В ряде случаев затруднения при извлечении плода обусловлены предлежанием плаценты к линии разреза матки (placenta cesarea). В данной ситуации следует быстро отслоить плаценту до оболочек, вскрыть их и извлечь плод [Серов В.Н. и др., 1997]. Не рекомендуется рассекать плаценту и через нее извлекать плод, так как при этом новорожденный теряет много крови, что значительно осложняет течение раннего неонатального периода и обусловливает необходимость проведения ему гемотрансфузии.
Любое расширение объема операции в ходе выполнения кесарева сечения нежелательно и может быть проведено только по строгим показаниям: при миоме матки больших размеров (особенно с нарушением питания в узлах или при подслизистом расположении узлов), опухолях яичников, раке шейки матки [Слепых А.С., 1986; Серов В.Н. и др., 1989; Кулаков В.И. и Прошина И.В., 1996; Field Ch.S., 1988].
В этих клинических ситуациях объем оперативного вмешательства определяется характером сопутствующей патологии: при миоме матки производят удаление матки, а при доброкачественных опухолях яичников — резекцию их или удаление придатков матки. При выявлении во время беременности рака шейки матки показана экстирпация матки с придатками (простая или расширенная), в дальнейшем — сочетанная лучевая терапия. Если в ходе выполнения кесарева сечения обнаружена матка Кувелера, то после извлечения плода производят экстирпацию матки.
Наиболее часто абдоминальное родоразрешение расширяют, производя стерилизацию, что должно быть строго обосновано: врачебное заключение о наличии тяжелых заболеваний, повторное кесарево сечение (при котором извлечен живой здоровый ребенок), заявление женщины о ее согласии. Нежелательно расширение объема кесарева сечения за счет выполнения консервативной миомэктомии, так как при этом на матке образуются два рубца, что может привести к значительному ухудшению заживления рассеченной в нескольких местах стенки матки, т.е. намного увеличится риск развития несостоятельности шва на матке.
Консервативную миомэктомию можно производить только в крупных специализированных клиниках, имеющих опыт выполнения подобных оперативных вмешательств с тщательным дооперационным обследованием и подготовкой к вмешательству, адекватным ведением послеоперационного периода [Шмаков Г.С. и др., 1988; Кулаков В.И. и др., 1988].
Аспирационный синдром
Одним из наиболее тяжелых осложнений, возникающих во время выполнения кесарева сечения, является аспирационный синдром (синдром Мендельсона), развивающийся при регургитации желудочного содержимого с последующим попаданием его в легкие [Титова Т.В., 1986; Кулаков В.И., Прошина И.В., 1996; Серов В.Н. и др., 1997; Bassel G.M., 1985]. При этом желудочное содержимое разрушает альвеолярный эпителий, что приводит к уменьшению продукции сурфактанта, спадению альвеол и нарушению равновесия между вентиляцией и перфузией. Клиническая картина при этом синдроме характеризуется ларинго- и бронхоспазмом, острой дыхательной и сердечной недостаточностью, возникают цианоз, одышка, тахикардия, в легких выслушиваются сухие и влажные хрипы.
Наиболее эффективным методом лечения данного синдрома является бронхоскопия, при которой устраняют обструкцию дыхательных путей. Необходимо проводить продленную ИВЛ. Параллельно вводят глюкокортикоиды внутривенно и эндотрахеально. Профилактикой данного тяжелого осложнения являются применение антацидных средств (антацид, тагомет, циметидин) и обязательное опорожнение желудка перед проведением наркоза, в случае необходимости в желудок вводят зонд. При проведении вводного наркоза рекомендуют применять положение Фовлера (приподнятый головной конец).
В.И. Кулаков и И.В. Прошина (1996) с целью профилактики аспирационного синдрома предлагают использовать катетер Фолея, который вводят через нос на расстояние 20—25 см за второе физиологическое сужение пищевода, где раздувают манжетку катетера до фиксации ее в пищеводе. Таким образом, раздутая манжетка катетера препятствует попаданию желудочного содержимого в легкие, что, по мнению автора, является оптимальной мерой профилактики аспирационного синдрома.
Синдром аортокавальной компрессии
У беременной или роженицы в положении лежа на спине может развиться опасный синдром сдавления нижней полой вены, или, точнее, синдром аортокавальной компрессии. Он возникает в результате давления беременной матки (масса которой накануне родов вместе с плодом, плацентой и околоплодными водами составляет около 6000 г) на нижнюю полую вену и брюшную аорту. Затруднение кровотока в нижней полой вене приводит к уменьшению венозного возврата к сердцу и сердечного выброса, в результате чего развивается гипотензия, а затруднение продвижения крови в брюшной аорте обусловливает снижение маточно-плацентарного кровотока, резкое ухудшение состояния внутриутробного плода и уменьшение кровоснабжения почек [Зильбер А.П., 1982; Серов В.Н. и др., 1989, 1997; Bassel G.M., 1985].
Выраженный синдром аортокавальной компрессии может развиться накануне родов у 70 % беременных, а у 11 % из них он проявляется в виде «постурального шока». Факторами, способствующими возникновению данного синдрома, являются многоводие, многоплодие, длительная перидуральная анестезия. Клиническая картина при данной патологии характеризуется общей слабостью и затруднением дыхания беременной в положении лежа на спине, причем эти симптомы быстро исчезают при повороте женщины набок.
Мера профилактики данного синдрома — рациональное положение женщины на операционном столе, при котором производят смешение беременной матки влево. Это достигают путем наклона левого края стола на 15° или с помощью валика, который подкладывают под правую ягодицу пациентки: при этом матка перестает оказывать давление на нижнюю полую вену и брюшную аорту. После извлечения плода женщину переводят в горизонтальное положение.
Однако если сдавление нижней полой вены продолжается более 10 мин, то требуется провести интенсивную инфузионную терапию, направленную на восстановление центральной и периферической гемодинамики (в первую очередь введение реовазоактивных препаратов). Ни в коем случае не следует вводить катехоламины, так как они приводят к выраженной гипертензии и перегрузке кровообращения, которые проявляются острой сердечной недостаточностью.
Тромбоэмболические осложнения
Известно, что после кесарева сечения в 10—15 раз возрастает риск развития тромбоэмболических осложнений [Серов В.Н. и др., 1982, 1997; Айламазян Э.К., 1985; Репина М.А., 1986]. Факторами, способствующими их возникновению, являются хроническая венозная недостаточность, варикозное расширение вен нижних конечностей, перенесенные ранее тромбозы и тромбоэмболии, различные виды шока (при которых развивается ДВС-синдром), массивные гемотрансфузии, сочетание беременности со злокачественными опухолями матки, яичников, поджелудочной железы. Наиболее грозным и опасным для жизни осложнением является тромбоз сосудов головного мозга и легочной артерии.
Тромбоз сосудов мозга проявляется внезапной головной болью, помрачением сознания, спастическими парезами, вялыми параличами, очаговой симптоматикой (гемиплегия), мозговой комой. Начальными симптомами данного осложнения могут быть эпилептиформные припадки, кратковременная потеря сознания.
При тромбоэмболии легочной артерии отмечаются одышка, сухой кашель, возбуждение, боли в груди, кровохарканье. При осмотре больных выявляют цианоз губ, тахипноэ, поверхностное дыхание, тахикардию, аускультативно выслушиваются хрипы в легких.
Основными методами диагностики данного осложнения являются рентгенологическое исследование легких, ЭКГ, ангиопульмонография. Рентгенологически устанавливают наличие треугольной тени инфаркта (расположенной верхушкой к корню легкого, а основанием — к периферии), исчезновение нормального сосудистого рисунка периферических ветвей облитерированной артерии, приподнятую диафрагму на стороне поражения, наличие плеврального выпота. При электрокардиографическом исследовании выявляют признаки перегрузки правых отделов сердца: изменение комплексов S1—Q3— Т3, появление P-pulmonale, инверсия зубца T (в отведениях V1 и V2).
При ангиопульмонографии обнаруживают внутрисосудистый дефект наполнения, облитерацию периферических ветвей легочной артерии, отсутствие сосудистого рисунка на различных участках легочной ткани. Диагностику всех тромбоэмболических осложнений облегчает исследование системы гемостаза, при котором выявляют выраженную хронометрическую и структурную гиперкоагуляцию, гиперагрегацию тромбоцитов, уменьшение содержания антитромбина III.
При тромбоэмболии легочной артерии рекомендуют проводить тромболитическую терапию (стрептаза, стрептокиназа в дозе 2 000 000—3 500 000 ЕД в течение 2—3 сут) под контролем системы гемостаза. В дальнейшем эффект лечения закрепляют с помощью прямых (гепарин) и непрямых (пелентан, фенилин) антикоагулянтов и антиагрегантов (ацетилсалициловая кислота, курантил). Мерами профилактики тромбоэмболии в акушерской практике являются эффективное лечение заболеваний, протекающих с хронической формой ДВС-синдрома, предупреждение коагулопатических кровотечений; специфическая и неспецифическая профилактика у всех послеоперационных больных; гемостазиологический контроль в группах высокого риска.
Эмболия околоплодными водами
Данное осложнение представляет опасность для жизни, так как является одной из основных причин возникновения шока и выраженных нарушений гемостаза [Бакщеев Н.С., 1977; Серов В.Н. и др., 1989, 1997]. Факторами, предрасполагающими к развитию осложнения, служат длительный гипертонус матки на фоне неадекватной стимуляции родовой деятельности, отслойка плаценты, многоплодная беременность, разрыв матки, зияние сосудов плацентарной площадки в ходе выполнения кесарева сечения.
В типичных ситуациях эмболия околоплодными водами развивается остро, обычно в I или II периоде родов, значительно реже — в последовом или раннем послеродовом периоде. При проникновении околоплодных вод в кровоток матери отмечаются зябкость, озноб, повышенная потливость, возбуждение, кашель, рвота, судороги.
Затем развиваются главные симптомы — загрудинные боли, цианоз, острая сердечно-сосудистая недостаточность, кровотечение и кровоточивость, кома. Большинство больных умирают в течение 2—4 ч (летальность достигает 80 %) на фоне необратимых изменений, обусловленных кардиогенным и геморрагическим шоком.
Важнейшим диагностическим мероприятием, без которого невозможно проведение эффективной интенсивной терапии эмболии околоплодными водами, является исследование системы гемостаза. При появлении первых клинических признаков эмболии обнаруживают гиперкоагуляцию и гиперагрегацию тромбоцитов и I фазу ДВС-синдрома. При дальнейшем развитии патологического процесса выявляют гипокоагуляцию, обусловленную коагулопатией и тромбоцитопенией потребления: гипофибриногенемию и тромбоцитопению, увеличение времени свертывания цельной крови; на тромбоэластограмме определяется резко выраженная хронометрическая и структурная гипокоагуляция, а нередко фиксируется просто прямая линия, что свидетельствует об абсолютной несвертываемости крови.
Основными мероприятиями в терапии эмболии околоплодными водами являются борьба с дыхательной недостаточностью, купирование проявлений шока, предупреждение и лечение геморрагических осложнений. С этой целью осуществляют ИВЛ, вводят электролиты, плазмозаменяющие препараты, нативную и свежезамороженную донорскую плазму, раствор альбумина, переливают теплую донорскую кровь. При резко выраженном фибринолизе используют трасилол, контрикал, гордокс.
Основными мерами профилактики данного тяжелого осложнения следует считать адекватную терапию возникших осложнений беременности, рациональное ведение родов, своевременное выполнение абдоминального родоразрешения с учетом показаний и противопоказаний, правильным выбором метода операции и необходимой предоперационной подготовкой.
А.Н. Стрижаков, В.А.Лебедев
Опубликовал Константин Моканов
Источник
ДВС-синдром (синдром диссеминированного внутрисосудистого свертывания крови) – это нарушение в функционировании системы гемостаза, которое проявляется в первую очередь усиленным формированием тромбов в мелких сосудах.
Данная патология является актуальной для самых разных областей медицины. Диагностикой и лечением ДВС-синдрома занимаются акушеры, реаниматологи, хирурги. Встречается патология как у взрослых, так и у детей, в том числе, новорожденных. Зачастую коагулопатии (нарушения в процессе свертывания крови) имеют врожденный характер, но могут развиваться в течение жизни. ДВС-синдром у новорожденных является одной из форм коагулопатии.
Механизм развития нарушения достаточно сложен, патология может иметь множество симптомов. По этой причине врачи сталкиваются с определенными трудностями при постановке диагноза. ДВС-синдром имеет свойство усугублять течение иных заболеваний, но самостоятельной болезнью при этом не является.
Содержание:
- Тромбоз: когда норма, а когда отклонение?
- ДВС-синдром – каковы причины?
- ДВС-синдром: стадии и формы
- Симптомы ДВС-синдрома
- Диагностика ДВС-синдрома
- Лечение ДВС-синдрома
Тромбоз: когда норма, а когда отклонение?
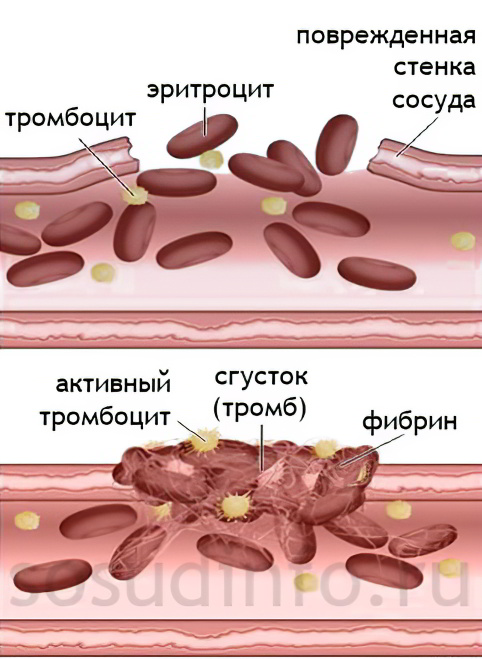
На протяжении всей жизни человек получает различные травмы, начиная от незначительных царапин и заканчивая серьезными ранениями. Организм имеет собственный механизм защиты, направленный на остановку крови. Для этого в поврежденной области она начинает сворачиваться, формируя тромб.
В целом, организм обладает двумя системами, имеющими кардинальное противоположное предназначение. Одна система называется свертывающей, а вторая противосвертывающей. Если они работают без каких-либо нарушений, то в организме поддерживается баланс. При возникновении угрожающей ситуации, например, при травме, кровь сворачивается, препятствуя массивному кровотечению. При отсутствии каких-либо повреждений кровь находится в жидком состоянии.
Чтобы в месте повреждения сосуда сформировался тромб, организм должен запустить множество сложнейших реакций. В них принимает участие белок под названием фибриноген, который присутствует в плазме крови, а также тромбоциты, фактор свертывания и различные ферменты. В результате, образовавшийся сгусток закрывает дефект на сосудистой стенке и не дает крови изливаться наружу.
Если повреждения сосуда не произошло, то кровь по сосудам циркулирует в жидком состоянии, не давая тромбам формироваться. За это отвечают антитромботические механизмы, которые осуществляются благодаря веществам, имеющим название антикоагулянты. Они включают в себя белки плазмы, эндогенный гепарин и протеолитические ферменты. Если фибриноген начинает скапливаться в том или ином месте сосуда, то быстрый ток крови «разбивает» его и тромб не образуется. Этот механизм носит название фибринолиза. В нем также участвуют ферменты, которые продуцируют лейкоциты, тромбоциты и иные клетки крови. Мелкие частицы фибрина в дальнейшем просто будут уничтожены макрофагами и лейкоцитами.
Если происходит сбой в тех или иных системах гемостаза, либо у человека развивается какое-либо заболевание, механизмы, регулирующие работу свертывающей и противосвертывающей системы, дают сбой. При этом в организме начинают формироваться тромбы, повышается риск развития массивного кровотечения. Именно такие нарушения лежат в основе развития ДВС-синдрома. Они являются крайне опасными для здоровья человека и несут в себе угрозу жизни.
ДВС-синдром – каковы причины?

ДВС-синдром – это не заболевание, а следствие тех или иных нарушений в организме.
Поэтому на его развитие оказывают влияние ряд состояний:
Инфекционные заболевания, сопровождающиеся сепсисом, либо тяжелое течение вирусной или бактериальной инфекции.
Шок любой этиологии: на фоне полученной травмы, на фоне отравления организма, на фоне инфекции.
Состояние, граничащее с летальным исходом – клиническая смерть.
Операции по поводу трансплантации органов, по поводу установки протеза клапана сердца. Серьезные травмы.
Нахождение человека на аппарате исукственного кровообращения во время проведения операции.
Раковые поражения внутренних органов. В плане развития ДВС-синдрома особую опасность представляют лейкозы.
В акушерской практике ДВС-синдром развивается на фоне массивного кровотечения во время родов, при ранней отслойке плаценты, при эмболии околоплодными водами.
Во время беременности ДВС-синдром может сопутствовать тяжелому токсикозу, резус-конфликту, внематочной беременности и не только.
Болезни сердечно-сосудистой системы.
Воспаления внутренних органов, сопровождающиеся нагноением.
ДВС-синдром может развиться при клинической смерти, при проведении реанимационных мероприятий. На фоне терминальных состояний ДВС-синдром либо развивается, либо разовьется в ближайшее время, если не будут предприняты определенные терапевтические меры.
У здорового новорожденного ребенка, который появился в положенные сроки, ДВС-синдром диагностируют очень редко. Он может сопутствовать гипоксии новорожденных, имеющей тяжелое течение, нарушениям в работе органов дыхания, эмболии околоплодными водами. В последнем случае симптомы ДВС-синдрома будут диагностированы как у женщины, так и у ребенка.
К наследственным коагулопатиям относят гемофилию и болезнь Виллебранда. При этом у ребенка наблюдается усиленная кровоточивость. Тромбогеморрагический синдром у детей диагностируют очень редко. Спровоцировать его могут инфекционные заболевания и тяжелые травмы.
ДВС-синдром: стадии и формы
В зависимости от того механизма, который спровоцировал развитие ДВС-синдрома, различают следующие его стадии:
Стадия гиперкоагуляции. При этом в крови увеличивается концентрация тромбопластина, который способствует ее повышенной свертываемости. В результате у человека начинают формироваться тромбы.
Коагулопатия потребления. В крови повышается уровень факторов свертывания, в ответ на это организм усиливает фибринолитическую активность, чтобы не допустить закупорки сосудов тромбами.
Гипокоагуляция. В этот период наблюдается нехватка в организме тромбоцитов, так как организм израсходовал их запасы во время предшествующих стадий. Данная ситуация приводит к тому, что кровь сворачивается плохо.
Стадия восстановления. Итак, любая серьезная травма или кровотечение, или иной поражающий фактор, влечет за собой повышенный и неконтролируемый расход тромбоцитов и иных компонентов крови, отвечающих за ее свертывание. Это вызывает их дефицит и дальнейшую гипокоагуляцию с повышенной кровоточивостью. При условии, что в этот период пациенту будет оказана качественная медицинская помощь, у него наступит фаза восстановления.
Тяжесть поражения обуславливается тем, что тромбы формируются во всех мелких сосудах, что влечет за собой поражение большинства тканей органов и систем.
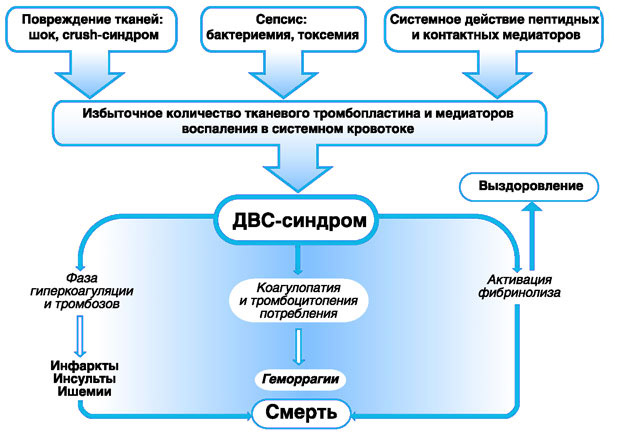
В зависимости от характера симптомов ДВС-синдрома и от тяжести их течения, различают следующие его формы:
Острая форма. Длительность ДВС-синдрома в острой форме может составлять от нескольких часов до нескольких дней. Чаще всего данное нарушение сопутствует травмам, сепсису, оперативным вмешательствам, гемотрансфузии при массивных кровопотерях.
Подострая форма. Длительность этой формы ДВС-синдрома может составлять несколько недель. Она чаще всего сопутствует хроническим заболеваниям инфекционного генеза и аутоиммунным процессам.
Хроническая форма. Эта форма ДВС-синдрома может длиться на протяжении нескольких лет. Чаще всего ее диагностируют терапевты, наблюдающие пациентов с болезнями печени, почек, сердца, сосудов, а также с сахарными диабетом. По мере прогрессирования основного заболевания, будут усиливаться симптомы ДВС-синдрома.
Рецидивирующая форма.
Скрытая форма.
Иногда ДВС-синдром может развиваться буквально в течение нескольких минут. Такую форму патологии называют молниеносной. Чаще всего с таким вариантом ДВС-синдрома сталкиваются врачи акушерской практики.
Симптомы ДВС-синдрома
Если ДВС-синдром имеет подострое или хроническое течение, то диагностировать его по симптомам может быть весьма проблематично. Острая фаза, напротив, сопровождается выраженными клиническими проявлениями, которые выражаются кожными высыпаниями и усиленным кровотечением. При этом выставить диагноз не составляет труда.
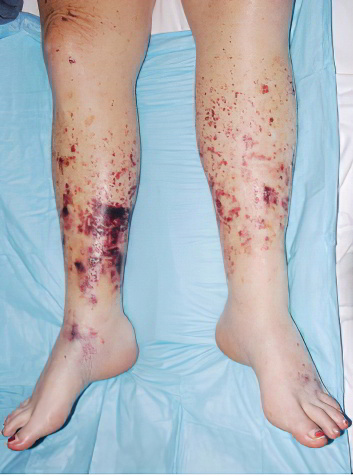
Так как на фоне ДВС-синдрома тромбы формируются в мелких сосудах, то пострадают в первую очередь такие органы, как: печень, легкие, кожа и головной мозг. Именно в них капиллярная сетка развита сильнее, чем в остальных органах. Прогноз на восстановление зависит от тяжести течения ДВС-синдрома.
К основным симптомам, позволяющим заподозрить ДВС-синдром, относят:
Появление геморрагической сыпи на коже. Возможно возникновение очагов некроза на лице, на руках и ногах.
Одышка. Она возникает в результате поражения легких. По мере нарастания дыхательной недостаточности возможна остановка дыхания с отеком легких.
Накопление фибрина в мелких сосудах почек приводит к сбоям в их работе, вплоть до развития почечной недостаточности. Это проявляется задержкой мочи и нарушением электролитного баланса в организме.
Неврологические расстройства являются следствием поражения головного мозга.
Также для ДВС-синдрома характерно появление носовых кровотечений, маточных кровотечений, появление гематом в области мягких тканей и внутренних органов.
Если рассматривать симптомы ДВС-синдрома в целом, то они сводится к появлению тромбозов и кровоизлияний, а также к нарушениям в работе большинства органов, которые являются жизнеобеспечивающими.
Диагностика ДВС-синдрома
Диагностика ДВС-синдрома невозможна только на основании его клинических проявлений. Выполнение лабораторных исследований является обязательным диагностическим мероприятий. Они дают возможность не только подтвердить наличие ДВС-синдрома, но также определить его стадию и форму.
Базовым методом исследования является коагулограмма крови, которая дает возможность обнаружить уменьшение количества тромбоцитов, рост фибриногена (на начальной стадии развития патологии) или его падение (на последующих этапах развития ДВС-синдрома). Также коагулограмма позволит определить увеличение времени свертывания крови и прочие нарушения.
Если человек погиб, то возможно проведение посмертной диагностики ДВС-синдрома. Для этого его ткани отправляют на гистологическое исследование. В них будут обнаружены форменные элементы крови, которые скапливаются в капиллярах, а также тромбы, закупоривающие их. Внутренние органы человека подвергаются множественным кровоизлияниям, покрыты участками некроза.
При подозрении на ДВС-синдром, необходимо контролировать показатели крови, так как на начальных стадиях развития патологии они могут быть в пределах нормы. Также нужно следить за нарушениями электролитного баланса в организме, за уровнем мочевины и креатинина в крови, за диурезом и pH крови.
Лечение ДВС-синдрома
Единой схемы, которую можно было бы применять для лечения любой формы ДВС-синдрома, просто не существует. Однако опираясь на стадии развития патологического процесса, врачи разработали определенные подходы к проведению терапии.
Для начала следует установить причину ДВС-синдрома.
В зависимости от этого, могут быть реализованы следующие подходы:
Назначение антибиотиков, если ДВС-синдром развивается на фоне гнойных состояний.
Восполнение крови при массивной кровопотере.
Стабилизация работы сердца и сосудов, артериального давления при развитии шокового состояния.
Оказание адекватной акушерской помощи.
Проведение обезболивания при развитии шока на фоне травмы или иных повреждений.
Чтобы устранить симптомы и проявления ДВС-синдрома, необходимо проводить следующую терапию:
Лечение антикоагулянтами. С этой целью чаще всего используют Гепарин, который позволяет нормализовать процессы свертывания крови, не дает формироваться тромбам, ускоряет процесс их растворения. В результате, работа органов и тканей нормализуется.
Назначение фибринолитиков и антифибринолитиков, что зависит от стадии ДВС-синдрома. Чтобы восполнить нехватку факторов свертываемости крови, пациенту назначают инфузионную терапию. Для этого используют замороженную плазму. Ее можно вводить с Гепарином, с препаратом Гордокс или Контрикал, которые препятствуют процессам гиперкоагуляции.
Улучшение текучести крови, назначение лекарственных средств для нормализации микроциркуляции крови в сосудах. Для достижения этих целей используют Аспирин, Трентал, Курантил и реологические растворы, например, Волювен и Реополиглюкин.
Проведение экстракорпоральной детоксикации. При этом пациенту проводят гемодиализ, плазмаферез, цитаферез.
Иногда решение о выборе терапевтической схемы приходится принимать очень быстро, так как на спасение жизни человека имеются считанные секунды. Обязательно нужно учитывать стадию развития ДВС-синдрома, так как в одно время показаны одни препараты, а в другой момент времени они могут быть категорически противопоказаны. Параллельно следует контролировать состояние свертывающей системы крови, ее электролитный и кислотно-щелочной баланс.
Также нельзя допускать, чтобы человек терпел боль, нужно проводить противошоковые мероприятия. На первой стадии развития патологического состояния пациенту вводят Гепарин.
В реанимацию доставляют всех больных, у которых имеется риск развития тромбогеморрагического синдрома, либо он уже диагностирован. Если этот синдром достиг 3 стадии, то вероятность летального исхода составляет 70%. Хроническое течение тромбогеморрагического синдрома всегда завершается гибелью больного.
Чтобы не допустить развития ДВС-синдрома, нужно своевременно его диагностировать и подбирать адекватную ситуации терапию. Чем раньше будет нормализован гемостаз, тем быстрее человек восстановится.
Видео: лекция А.И. Воробьева о ДВС-синдроме:
Автор статьи: Шутов Максим Евгеньевич | Гематолог
Образование:
В 2013 году закончен Курский государственный медицинский университет и получен диплом «Лечебное дело». Спустя 2 года окончена ординатура по специальности «Онкология». В 2016 году пройдена аспирантура в Национальном медико-хирургическом центре имени Н. И. Пирогова.
Наши авторы
Источник
