Кордарон индуцированный тиреотоксикоз код по мкб
Амиодарон-индуцированные тиреопатии (АмИТ, АИТ) – это группа патологий щитовидной железы, вызванных продолжительным приемом противоаритмического препарата амиодарона. Течение часто бессимптомное, иногда развиваются слабые и умеренные признаки гипертиреоза (раздражительность, чувство жара, тахикардия, тремор) или гипотиреоза (зябкость, слабость, сонливость, быстрая утомляемость). Диагностика включает анализы крови на тироксин, трийодтиронин и тиреотропный гормон, сцинтиграфию и УЗИ с допплерографией щитовидной железы. При гипотиреозе назначается гормональная заместительная терапия, при тиреотоксикозе – тиреостатики или глюкокортикоиды.
Общие сведения
Амиодарон относится к антиаритмическим лекарственным средствам, широко применяется в кардиологической практике при лечении тяжелых аритмий, предсердной и желудочковой экстрасистолии, WPW-синдрома, аритмии при коронарной и сердечной недостаточности. В числе побочных эффектов медикамента отмечаются гипер- и гипотиреоз или амиодарон-индуцированные тиреопатии. Синонимичные названия расстройств данной группы – амиодарон-индуцированные тиреоидиты, кордарон-индуцированные тиреопатии. Распространенность патологии среди пациентов, принимающих препарат, составляет около 30%. Гипертиреоз чаще регистрируется в регионах с йододефицитом, там его частота достигает 12%. Эпидемиология гипотиреоза выше в областях с умеренным потреблением йода, колеблется от 6 до 13%.
Амиодарон-индуцированные тиреопатии
Причины АИТ
Амиодарон на 39% состоит из йода, является бензофурановым производным, по молекулярной структуре схожим с гормоном тироксином. Во время лечения этим препаратом организм ежедневно получает от 7 до 21 г йода при средней физиологической потребности 200 мкг/сут. Длительный прием амиодарона способствует нарушению обмена тиреоидных гормонов и тиреотропина, что проявляется гипо- или гипертиреозом. Характерная особенность данного лекарственного средства – способность накапливаться в печени и жировой ткани. Период его полувыведения из организма в среднем составляет 53-55 дней, поэтому амиодарон-индуцированные тиреопатии могут развиваться спустя 1-2 месяца после завершения курса терапии. В группе риска находятся женщины от 35-40 лет, люди пожилого и старческого возраста, а также лица с дисфункциями ЩЖ.
Патогенез
Под действием амиодарона изменяется метаболизм йодированных гормонов, регуляция их уровня гипофизом через ТТГ. Препарат нарушает превращение тироксина в трийодтиронин в тиреотропоцитах путем ингибирования фермента дейодиназы-II. Фермент дейодирует внутреннее кольцо тироксина, обеспечивает его конверсию в трийодтиронин, регулирует уровень метаболически инертной фракции Т3, поддерживает концентрацию этого гормона в нервной ткани. Амиодарон снижает чувствительность гипофиза к воздействию йодсодержащих гормонов. По этой причине у большинства пациентов в начале лечения обнаруживается легкое повышение тиреотропина при нормальном количестве тироксина и трийодтиронина – эутиреоидная гипертиреотропинемия.
С учетом патогенеза различают три вида амиодарон-индуцированных тиреопатий. При амиодарон-индуцированном тиреотоксикозе I типа гормональные изменения связаны с избыточным поступлением йода. Заболевание часто возникает на фоне предрасположенности к многоузловому зобу и функциональной автономности ЩЖ. Кордарон-индуцированные тиреопатии II типа более распространены, обусловлены токсическим влиянием препарата на тироциты. Развивается специфическая форма тиреоидита с деструктивным тиреотоксикозом. Третий вариант тиреопатии – гипотиреоз. Он диагностируется у лиц, в крови которых присутствуют антитела к тиреоидной пероксидазе, поэтому в качестве патогенетического механизма предполагается провокация аутоиммунного тиреоидита избытком йода.
Симптомы АИТ
Существует три варианта клинической картины тиреопатий, спровоцированных приемом амиодарона. При индуцированном гипотиреозе ярко выраженная симптоматика отсутствует. Большинство пациентов не замечает каких-либо изменений в самочувствии. Некоторые сообщают о появлении дневной сонливости и слабости, быстром нарастании утомления при выполнении привычной работы, периодическом возникновении зябкости. Объективно наблюдается снижение температуры тела, артериальная гипотония, замедление пульса, отечность, нарушения менструального цикла.
АмИТ 1 типа проявляется картиной развернутого гипертиреоза. Больные становятся раздражительными, беспокойными, тревожными, испытывают трудности с концентрацией внимания и запоминанием информации, выглядят забывчивыми, рассеянными. Развивается тремор, появляются приливы жара в теле, усиливается потоотделение и жажда. Пациенты тяжело переносят жару и духоту, теряют вес, плохо спят по ночам. АмИТ 2 типа часто имеет стертые симптомы, поскольку применение амиодарона устраняет признаки дисфункции сердечно-сосудистой системы, характерные для тиреотоксикоза. Зачастую клиническая картина представлена лишь мышечной слабостью и снижением массы тела.
Осложнения
Последствия терапии амиодароном обычно носят обратимый характер, после отмены медикамента функциональность ЩЖ возвращается к норме. Стойкие осложнения обусловлены воздействием избыточного количества гормонов Т3 и Т4 на сердце: ухудшается течение имеющихся аритмий, учащаются стенокардические приступы, появляется и усугубляется сердечная недостаточность. Тиреотоксикоз приводит к гиперчувствительности мышечных клеток сердца к воздействию адреналина, норадреналина, дофамина, что увеличивает риск желудочковых аритмий. Йодсодержащие гормоны оказывают непосредственное влияние на кардиомиоциты, изменяя их электрофизиологические свойства и провоцируя фибрилляцию предсердий. При длительном течении АмИТ первого типа возможно развитие дилатационной кардиомиопатии.
Диагностика
При подозрении на тиреопатию пациентов, принимающих амиодарон, направляют на консультацию к врачу-эндокринологу. На начальном этапе обследования специалист анализирует анамнез, уточняет продолжительность приема антиаритмического препарата, его дозировку, наличие патологий ЩЖ. Жалобы больных отсутствуют либо соответствуют картине гипо- или гипертиреоза. Для подтверждения диагноза и дифференциации различных типов тиреопатий применяются следующие методики:
- Тиреосцинтиграфия. Исследование радиоизотопами йода (сцинтиграфия щитовидной железы) назначается больным с тиреотоксикозом. Для АИТ-1 свойственен нормальный или усиленный захват препарата, при АИТ-2 обнаруживается сниженное накопление йода в железистой ткани.
- Эхография. По результатам УЗИ щитовидной железы и допплерографии при тиреопатиях типа 1 диагностируются признаки многоузлового зоба или аутоиммунного поражения железы с нормальным либо повышенным кровотоком. У больных с тиреопатиями типа 2 кровоток часто сниженный или не определяется.
- Анализ крови (гормоны и антитела). При гипотиреозе показатели Т4 заметно снижены, титр АТ-ТПО повышен. АмИТ 1 диагностируется по повышенному уровню Т3, Т4, ТТГ при развернутой клинической картине. Особенность АмИТ-2 – значительное повышение уровня Т4 (от 60 пмоль/л), умеренное повышение свободного Т3 в сочетании со слабовыраженной симптоматикой или на фоне бессимптомного течения.
Лечение АИТ
Тактика ведения пациента совместно определяется кардиологом и эндокринологом. Этиотропным направлением терапии является отмена амиодарона, однако во многих случаях это невозможно, поскольку прекращение приема препарата провоцирует желудочковую аритмию, сопряжено с риском развития жизнеугрожающих состояний. Задачей терапии становится нормализация уровня гормонов Т4 и Т3. Выбор методов зависит от формы заболевания:
- Гипотиреотические АмИТ. Манифестный гипотиреоз корректируется заместительной гормонотерапией. Больным назначаются препараты тироксина. Продолжительность лечения варьируется с учетом компенсаторных возможностей железы, выраженности аутоиммунного компонента, возможности отмены амиодарона.
- АмИТ I. Проводится лечение тиреостатиками. Из-за избыточного поступления йода для подавления производства гормонов показаны большие дозы лекарственных средств.
- АмИТ II. При деструктивных процессах в щитовидной железе используются глюкокортикостероиды, например, преднизолон. Продолжительность курса – до 3 месяцев.
- Смешанные АмИТ. При сочетании двух форм тиреотоксикоза наблюдается тяжелое течение болезни, требующее одновременного применения тиреостатиков и глюкокортикоидов. В процессе лечения устанавливают преобладающий тип тиреопатии, один из препаратов отменяют.
При неэффективности консервативного лечения тиреотоксикоза, спровоцированного амиодароном, необходимы радикальные меры, нацеленные на подавление гормональной функции ЩЖ. Выполняется тотальная тиреоидэктомия (хирургическое удаление железы). Пациентам с тяжелыми сердечными патологиями, являющимися противопоказанием к оперативному вмешательству, назначается радиойодтерапия, вызывающая гибель тиреоцитов.
Прогноз и профилактика
Исход амиодарон-индуцированных тиреоидитов в большинстве случаев благоприятный, особенно если существует возможность отмены противоаритмического лекарства. Гипотиреоз успешно компенсируется гормональной терапией, тиреотоксикоз – тиреостатиками, глюкокортикоидами. Для профилактики данного состояния больным, принимающим кордарон, один раз в полгода необходимо проводить исследование крови для определения уровня тиреотропного гормона, тироксина, трийодтиронина. Результаты лабораторных тестов позволяют эндокринологу оценить, насколько функциональна щитовидная железа, рассчитать риск развития тиреопатии.
Источник
Кордрон-индуцированный тиреотоксикоз, АИТ, НТГ, ЖДА…
Здравствуйте, уважаемые консультанты!
Прошу помочь разобраться.
Мой родственник (69 лет, 170 см, вес последние годы — 48 кг) пришёл от эндокринолога-тиреоидолога с кучей новых диагнозов и назначений. (Был направлен к нему из районной поликлиники).
Хотелось бы понять, насколько это серьёзно, насколько можно быть уверенным в точности диагнозов, что лечить в первую очередь. А то, признаться, некоторые новые рекомендации пугают — на фоне старых проблем. Может, лучше дообследоваться, прежде чем всё это выполнять?
Цитирую по карточке:
Кордарон-индуцированный тиреотоксикоз. АИТ. НТГ. Гипокальцеемия. Железодефицитная анемия.
(Все диагнозы — новые! Кордарон он принимал давно, перестал, как минимум, полгода назад, а то и все полтора, точно пока выяснить не удалось).
Рекомендовано: 1) тирозол 10 мг 2 р/день; 2) исключить сахар, мёд, соки и т.п. 3) феррум лек (жевательные) 1 т. 2 р/день длительно; 4) Натекаль Д3 или Ca D3 никомед форте 1т 2 р/день постоянно.
Основные результаты анализов (в скобках — нормы лаборатории)
4 июня:
!<< ТТГ 0,06 (0,27-4,20)
> Т4 св. 26,50 (12,00+22,00)
> глюкоза 6,1 (4,10-5,90); а 24 мая 5,9 (4,6-6,4)
< кальций 2,24 (2,25-2,75)
фосфор 1,42 (0,87-1,45)
< железо 9,69 (12,50-32,20)
> мочевина 7,66 (2,80-7,20), а 24 мая 5,1 (2,9-7,5)
< креатинин 64,70 (72,00-127,00)
Для сравнения: в июне 2011 глюкоза 5,19, железо 9,43, кальций 2,31 (2,20-2,65).
30 мая
гемоглобин 12,8 (12,6-17,4)
гематокрит 37,9% (37,0-51,0)
> СОЭ (по Вестергрену) 29 (<20)
> С-реактивный белок 8,3 (0,0-5,0)
УЗИ щитовидки прочитать могу не всё, поэтому в виде картинки. Там рядом и некоторые другие анализы. Обращаю внимание на фосфаты в ОАМ от 14 мая.
Сопутствующие заболевания:
Атеросклероз, синдром Лэриша (было несколько операций); гастрит, дуоденит; стриктура правого мочеточника, нефростома правой почки, хр. пиелонефрит, МКБ (ХПН нет!) аденома простаты (простатит-?); ИБС, мерцательная аритмия; глаукома.
Принимает постоянно: торвакард 20 мг, дюфалак, омник либо омник окас, снотворное релаксон либо имован. Иногда: свечи «глицерин». Изредка: но-шпа (при болях в животе), каптоприл (при редких повышениях АД), гл. капли фотил. Месяц-два назад принимал витапрост, цистон. Ещё раньше — омепразол, энзистал, недолго —альмагель.
А/д уже давно обычно ~90/60, изредка повышение до 160-170/70, (хотя несколько лет назад была гипертония), пульс обычно за 80.
Жалоб много разных, попробую кратко. (Живём в одной квартире, так что пишу не только с его слов):
Бессонница (снотворное уже почти не помогает), проблемы с животом, то голодные боли, то боли после еды; часто нет аппетита; бывают запоры, бывает понос. Боли в ногах (ходит с трудом и недолго), онемение, иногда приступами ощущения приливов крови к ногам, потом выше, к животу, к голове, иногда с учащением пульса. Небольшие отёки на ступнях. Головные боли. Раздражительность, перепады настроения.
В начале июня температура поднималась до ~37,3, потом — стала к вечеру подниматься почти до 38, предположили обострение пиелонефрита, с 10-го мая пропил 5 дней аугментин (эндокринолог сказала, что продолжать не надо).
В конце мая беспокоила полиурия до 3 л/сут. (с плотностью 1006), иногда повышенная жажда (по этому поводу и был направлен к эндокринологу). Прошла после совета пить _только_ при жажде: тогда количество уменьшилось до 1450 мл (с 6 до 18 — 590 мл, с 18 до 6 — 860 мл), пл. 1010-1016 (по Зимницкому). Иногда он пьёт больше, опасаясь засорения нефростомы — предполагаю, что причина полиурии могла быть и в этом.
Последнее время отходит белая мокрота в больших количествах.
Что особенно беспокоит в назначениях. 1) Запрет сладкого. Он и так мало ест, иногда из-за болей в животе. Раньше хоть сладким чаем можно было поддерживать организм… 2) Препараты железа и кальция могут влиять на пищеварение — а с этим и без них довольно плохо…
Прошу прощения, что длинно — короче не умею…
В картинках: 1) УЗИ щитовидки 15 июня; 2) биохимия от 4 июня; 3) ОАК и др. от 30 мая; 4) ОАМ от 30 мая; 5) ОАМ от 14 мая.
С уважением и надеждой на ответ,
Игорь
Источник
В статье представлены новости Европейской тиреоидологической ассоциации 2018 г. Освещены особенности ведения пациентов с амиодарон-ассоциированной дисфункцией щитовидной железы (гипотиреоз, тиреотоксикоз).

Введение
Амиодарон — это производное бензофурана, йодсодержащий препарат, особенно эффективный в терапии наджелудочковых аритмий [1]. Из-за высокого содержания йода и фармакологических свойств (подавление периферического монодейоденирования тироксина, Т4) препарат вызывает дисфункцию ЩЖ и изменение показателей, свидетельствующее об изменении ее функции. Приблизительно у 15–20% пациентов, получавших лечение амиодароном, развивается тиреотоксикоз (амиодарон-
индуцированный тиреотоксикоз, АИТ) или гипотиреоз (амиодарон-индуцированный гипотиреоз, АИГ) [2]. Тип дисфункции ЩЖ частично зависит от приема йода, так, АИГ
более часто встречается в йод-насыщенных областях,
АИТ — в йод-дефицитных [2]. Диагноз, классификация и тактика при амиодарон-индуцированной дисфункции ЩЖ, а именно АИТ, часто сложны [3, 4]. Не обнаружено ни одного специфического предиктора амиодарон-ассоциированной дисфункции ЩЖ [5], хотя женский пол и антитела к антитиреоидной тиреопероксидазе прогнозируют АИГ [6].
Патогенез изменений ЩЖ при лечении амиодароном и тактика лечения ее дисфункции
Как амиодарон влияет на анализы, оценивающие функцию ЩЖ, у эутиреоидных пациентов?
У большинства пациентов, начавших получать амиодарон (обычно 200 мг/сут), отмечается эутиреоз, даже если используются большие дозы (400 мг/сут) [6]. Однако у всех пациентов, получавших лечение амиодароном, наблюдаются ранние (<3 мес.) или поздние (>3 мес.) изменения уровней сывороточных тиреоидных гормонов в анализах. Высокое содержание йода в амиодароне повышает концентрацию неорганического йода в плазме крови в 40 раз, выделение йода с мочой — до 15 тыс. мкг за 24 ч. Из-за эффекта Вольфа — Чайкова ЩЖ адаптируется к перегрузке йодом путем подавления органификации йода и снижения уровней гормонов ЩЖ. Последний эффект — основная причина повышения концентрации сывороточного тиреотропного гормона (ТТГ). Кратковременное лечение амиодароном (400 мг/сут в течение 3 нед.) снижает скорость продукции тироксина (Т4) и скорость метаболизма Т4 [6]. Амиодарон также подавляет внутриклеточный перенос Т4 и активность йодтирониндейодиназы 2-го типа в гипофизе, с последующим снижением продукции внутриклеточного трийодтиронина (Т3) и связывания тиреоидного гормона с его родственным рецептором в гипофизе [7]. Однако эти гипофизарные эффекты также проявляются в хронических стадиях в течение длительного лечения амиодароном и, скорее всего, менее важны для изменения уровня ТТГ, чем эффект Вольфа — Чайкова. Позже эффект Вольфа — Чайкова проходит [8], и происходит нормализация сывороточной концентрации Т4 и ТТГ. В эту фазу уровни Т4, свободного Т4 (свT4) и превращенного Т3 (пТ3) повышаются, в то время как уровни сывороточных общего Т3 и свободного Т3 (свT3) снижаются из-за подавления активности печеночной йодидтирониндейодиназы 1-го типа [9, 10].
Повышение концентрации сывороточного пТ3 обычно намного больше, чем понижение концентрации Т3 в сыворотке [11]. Упомянутые выше изменения сывороточных Т4, Т3 и пТ3 наблюдались рано во время лечения амиодароном и сохранялись в течение длительного лечения. После 3-х мес. терапии достигалось устойчивое состояние, при котором уровень сывороточного ТТГ возвращался к исходным значениям [12]. Нормализация сывороточного ТТГ, скорее всего, связана с повышенной скоростью продукции Т4 и уменьшением скорости метаболизма [6, 13]. Изменения скорости выработки Т4 и скорости метаболизма подавляют блокаду образования Т3, таким образом, повышая уровень сывороточного Т3 в низко нормальном диапазоне [13]. С кумулятивной дозой амиодарона уровни сывороточного общего Т4, свТ4 и пТ3 остаются у верхней границы нормы или слегка повышенными, в то время как уровни сывороточного Т3 (биохимически активного гормона) находятся в нормальном диапазоне у нижней границы. Такой биохимический профиль пациентов, получающих лечение амиодароном, считается эутиреоидным.
Лечить ли всех пациентов с АИГ? Надо ли отменять амиодарон у этих пациентов?
Распространенность АИГ у пациентов, получавших лечение амиодароном, может достигать 26% (субклинический гипотиреоз) и 5% (манифестный гипотиреоз) [14]. Хотя АИГ может развиваться у пациентов с нормальной ЩЖ и отсутствием аутоиммунной реакции, он чаще всего развивается у пациентов со скрытым хроническим аутоиммунным тиреоидитом, преобладает у женщин, а также в йод-насыщенных областях [2, 15, 16]. Клинически симптомы АИГ не отличаются от симптомов гипотиреоза другой этиологии, но стоит упомянуть, что тяжелый гипотиреоз может способствовать повышению чувствительности желудочков к жизнеугрожающим аритмиям [17].
АИГ не требует отмены амиодарона. Лечение левотироксином натрия (ЛН) рекомендовано во всех случаях манифестного гипотиреоза, в то время как этого можно избежать при субклинических формах, особенно у пожилых людей, но необходимо часто оценивать тиреоидный статус для выявления возможного прогрессирования гипотиреоза (рис. 1).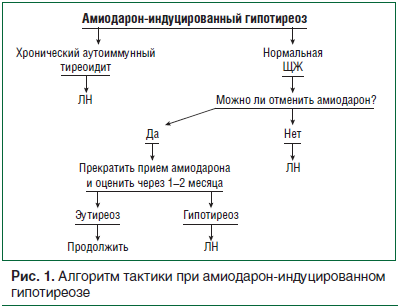
Сколько типов АИТ может быть выделено и каковы диагностические критерии?
АИТ 1-го типа — это форма йод-индуцированного гипертиреоза, обусловленная чрезмерным, бесконтрольным синтезом тиреоидных гормонов автономно функционирующей ЩЖ в ответ на йодную нагрузку, которая обычно развивается при наличии исходно узлов ЩЖ или латентной болезни Грейвса [1, 2, 18]. АИТ 2-го типа —
это деструктивный тиреоидит, который развивается при нормальной ЩЖ [1, 2, 18]. Смешанная/недифференцированная форма также устанавливается, когда у пациента присутствуют оба типа. АИТ 2-го типа преобладает в йод-дефицитных областях [1, 2, 18], и это наиболее часто встречающаяся форма АИТ [19]. Диагноз АИТ обычно предусматривает повышение сывороточных уровней cвТ4 и свТ3 и снижение уровня сывороточного ТТГ [20]. Антитиреоидные антитела, так же как и антитела к антитиреоидной тиреопероксидазе, обычно положительные при АИТ 1 и отрицательные при АИТ 2 [1], хотя их наличие необязательно для установления диагноза АИТ 1 [21].
С помощью УЗИ можно быстро оценить объем ЩЖ, узловые образования, паренхиматозные эхогенные структуры и васкуляризацию. В целом большинство данных показывают, что стандартное УЗИ ЩЖ имеет низкое диагностическое значение. УЗИ с эффектом Допплера представляет собой неинвазивную оценку васкуляризации ЩЖ в реальном времени [18], является хорошей помощью в диагностике деструктивной формы АИТ 2 (отсутствие гиперваскуляризации вместе с высокими уровнями гормонов ЩЖ (табл. 1) [22].
Всегда ли АИТ — чрезвычайная ситуация?
АИТ может быть опасным состоянием, т. к. может обострять имеющуюся кардиальную патологию. АИТ ассоциирован с повышением уровня заболеваемости и смертности, особенно у пожилых пациентов с нарушенной функцией левого желудочка [23–25]. Таким образом, в большинстве случаев, а именно у пожилых пациентов, требуются срочное восстановление и поддержание эутиреоза [26]. Пациентам с АИТ должно проводиться срочное лечение в любое время из-за повышенных рисков заболеваемости и смертности, в частности, у пожилых и/или при наличии дисфункции левого желудочка. Тотальная тиреоидэктомия должна быть выполнена без промедления у пациентов с АИТ с ухудшением функции сердца и у тех пациентов, у которых тиреотоксикоз не поддается терапии. Это заключение может быть сделано мультидисциплинарной бригадой в составе эндокринолога, кардиолога, анестезиолога и хирурга с большим опытом.
Может ли терапия амиодароном быть продолжена в некоторых случаях АИТ?
Не существует ни единого мнения, ни достоверных данных касательно решения продолжать или прекращать терапию амиодароном у пациентов с АИТ. Это решение должно быть индивидуальным, с учетом стратификации рисков, принятым совместно кардиологами и эндокринологами [1, 27].
В рандомизированных клинических исследованиях все 26 пациентов с АИТ 2, получавших лечение тиамазолом (метимазолом) и преднизолоном или преднизолоном и перхлоратом натрия, достигли эутиреоза на 8–14 нед., невзирая на амиодарон [28]. Похожие результаты получили в небольшом проспективном исследовании 13 больных с АИТ 2 [29]. В Японии изучали 50 пациентов с АИТ 2, которые продолжали получать амиодарон, рецидивирующий АИТ 2 отмечался только у трех пациентов спустя несколько лет после первого эпизода АИТ [30]. С другой стороны, в большом ретроспективном когортном исследовании у 83 пациентов с АИТ 2 преднизолон восстанавливал эутиреоз у большинства независимо от продолжения или отмены
амиодарона, но продолжающаяся терапия амиодароном повышала процент рецидива тиреотоксикоза, вызывая задержку устойчивого восстановления эутиреоза и более длительное воздействие гормонов ЩЖ на сердце [31]. Если состояние сердца нетяжелое и стабильное, амиодарон можно осторожно отменять, если необходимо, то возможно возобновить после восстановления эутиреоза. Проблема более трудная при АИТ 1 и смешанных/недифференцированных случаях АИТ. Многие эндокринологи предпочитают отменять амиодарон, если это возможно с кардиологической точки зрения [3, 32]. Таким образом, решение, стоит ли продолжать применять амиодарон или отменять, должно приниматься с учетом потенциальной пользы амиодарона при жизнеугрожающих аритмиях, угрозе длительного воздействия избытка гормонов и типа АИТ.
Какова тактика лечения при АИТ 1?
Ввиду преобладающего патогенетического механизма АИТ 1 лучше поддается лечению антитиреоидными препаратами (карбимазол (пролекарство для метимазола), метимазол или пропилтиоурацил), когда медикаментозная терапия целесообразна [12, 33]. В некоторых случаях экстренная или спасительная тиреоидэктомия может быть первоначальным терапевтическим выбором. Йод-насыщенная ЩЖ у пациентов с АИТ малочувствительна к тионамидам, так, с более высокими ежедневными дозами лекарств (40–60 мг метимазола или эквивалентной дозой пропилтиоурацила) требуется более длительный период, чем обычно, для восстановления эутиреоза. Это, очевидно, не идеальная ситуация у пациентов с исходной кардиальной патологией, у которых гипертиреоз должен быть быстро скомпенсирован. Для того чтобы увеличить чувствительность ЩЖ к тионамидам, используется перхлорат калия, который снижает захват йода ЩЖ. Были использованы дозы, не превышающие 1 г/сут, для того, чтобы минимизировать неблагоприятное действие лекарства (особенно на почки и костный мозг). Кроме того, рекомендуется не использовать препарат более чем
4–6 нед. [2]. Перхлорат натрия — альтернативный вариант, т. к. перхлорат калия больше недоступен. Перхлорат натрия доступен в качестве раствора — 21 капля соответствует 300 мг перхлората. Лечение тионамидами может быть продолжено до восстановления эутиреоза, если это допустимо при основном заболевании сердца и сердечно-сосудистой компенсации. После восстановления эутиреоза обычно рекомендуется окончательная терапия гиперфункционирующей ЩЖ [1]. Это позволяет безопасно возобновить и продолжить прием амиодарона, если это необходимо с кардиологической точки зрения. Если прием амиодарона может быть прекращен, радиойодтерапия может быть проведена, когда контаминация йодом окончена, вплоть до 6–12 мес. после прекращения приема амиодарона, нормализации выделения йода с мочой и адекватного уровня поглощения радиоактивного йода. Окончательное лечение АИТ 1 с исходной гиперфункцией ЩЖ не отличается от лечения спонтанного гипертиреоза. При отсутствии доказательств, свидетельствующих о деструктивном тиреотоксикозе, не рекомендуется использование ГК при АИТ 1.
Какова тактика при АИТ 2?
В одном рандомизированном исследовании у 36 пациентов, которые получали амиодарон и метимазол (30 мг/сут), сравнивались прием преднизолона (30 мг/сут) и перхлората натрия (500 мг/сут) или комбинации этих препаратов. При лечении преднизолоном эутиреоз был достигнут у всех пациентов, в то время как 30% пациентов, лечившихся только перхлоратом натрия, нуждались в дополнительном лечении преднизолоном для достижения эутиреоза. Таким образом, преднизолон рассматривается как наиболее эффективный способ лечения этих пациентов [28]. Начальная доза пероральных ГК при АИТ — 2–30 мг/сут преднизолона
(или эквивалентная доза других ГК), снижаемая при достижении клинического и/или биохимического эутиреоза. В некоторых случаях АИТ 2 может требовать длительного периода лечения. Если АИТ 2 представляет собой критическое состояние, спасающая тиреоидэктомия может быть рассмотрена так же, как и при АИТ 1 или смешанных/недифференцированных формах.
Какова тактика при смешанных/недифференцированных формах АИТ?
Различие между АИТ 1, АИТ 2 и смешанными/недифференцированными формами может быть важным для определения дальнейшей тактики лечения [1, 34].
Смешанные/недифференцированные АИТ (даже если не полностью охарактеризованы) встречаются в клинической практике и обусловлены обоими патогенетическими механизмами АИТ 1 (йод-индуцированный гипертиреоз) и АИТ 2 (деструктивный тиреоидит) [1, 34]. Весьма маловероятно, что пациенты с АИТ и морфологически нормальной ЩЖ, отсутствующей васкуляризацией, отрицательными антителами к анти-ТТГ имеют смешанные/недифференцированные формы АИТ. У этих пациентов на основании физикального осмотра, измерения чувствительности антител к анти-ТТГ рецепторам допускают диагноз АИТ 2 и лечение ГК [35]. Различие между АИТ 1 и смешанными/недифференцированными формами АИТ проводить более трудно, обычно это представляет собой диагноз исключения (при наличии узлового зоба). Терапевтический подход в данной ситуации неясен. Если точный диагноз не может быть выставлен, могут быть предложены 2 возможных подхода. В первую очередь начинают с лечения тионамидами (± перхлорат натрия), как и при АИТ 1, при отсутствии биохимического улучшения за относительно короткий период времени (оправданно 4–6 нед.) добавляют ГК с предположением, что в существующей патологии имеет место деструктивный компонент. Альтернативный метод представлен комбинированным лечением (тионамиды и ГК) с самого начала [36]. Проведение тиреоидэктомии обоснованно в случае слабого ответа на комбинированную терапию (рис. 2).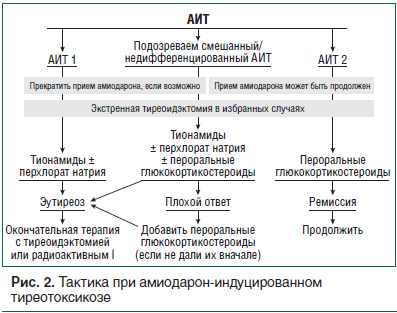
Может ли прием амиодарона быть возобновлен (если необходимо) у пациентов с предшествующим АИТ?
В ретроспективном исследовании, в котором изучалась проблема повторного введения амиодарона при АИТ в анамнезе, из 172 пациентов с АИТ 46 нуждались в повторном курсе амиодарона спустя 2 года в среднем после отмены лекарства. АИТ рецидивировал у 14 из 46 пациентов (30%), у 12 из 46 (26%) развился АИГ, у оставшихся 20 пациентов эутиреоз сохранялся в среднем в течение 6 лет после лечения [37]. У большинства пациентов с рецидивом АИТ (11 из 14) был классифицирован АИТ 1 [38]. Другие неопубликованные исследования, упомянутые в статье Ryana et al. [39], сообщают о рецидиве АИТ или вновь развившемся гипертиреозе после восстановления терапии амиодароном в 9% случаев. Вопрос, применять ли превентивную терапию антитиреоидными препаратами перед возобновлением приема амиодарона, остается без ответа ввиду отсутствия доказательств.
Заключение
В то время как АИГ легко лечится, АИТ представляет собой диагностическую и терапевтическую сложность. Большинство пациентов с АИТ 2 (деструктивным тиреоидитом) успешно лечатся ГК, им может не понадобиться отмена амиодарона. Лечение АИТ 1 (смешанных/недифференцированных форм) — намного более сложная задача из-за устойчивости йодонасыщенной железы к антитиреоидным препаратам. С учетом сложности диагностической дифференциации между АИТ 1 и смешанными/недифференцированными формами часто используется комбинированное лечение.
Источник
