Патология глаза при псевдоэксфолиативном синдроме

Статья посвящена псевдоэксфолиативному синдрому как фактору риска развития синдрома «сухого глаза»
Введение
В последние годы вопросы диагностики, профилактики и лечения синдрома «сухого глаза» (ССГ) приобретают все большую актуальность. В настоящее время это состояние вышло за рамки отдельной нозологической формы, распространенность ССГ составляет среди общей популяции 35% [1], а среди пациентов офтальмологического профиля – 45%, увеличиваясь с возрастом [2]. Определен спектр основных заболеваний глаз, имеющих тесную патогенетическую связь с ССГ, не ослабевает значимость общих расстройств организма, нередко сопровождающихся его развитием. Однако наряду с общеизвестными нозологическими формами ССГ осложняется еще целый ряд заболеваний органа зрения, традиционно не учитывающихся практикующими офтальмологами.
Псевдоэксфолиативный синдром (ПЭС), представляющий собой системную патологию с преимущественным поражением органа зрения, характеризуется избыточной продукцией и накоплением в различных структурах глаза патологического экстрацеллюлярного материала [3]. Псевдоэксфолиативные отложения обнаружены и в поверхностных тканях глаз, изменения которых нередко ассоциированы с развитием ССГ [4]. Опубликован ряд исследований, касающихся изменений функциональных и морфологических показателей прероговичной слезной пленки у пациентов с ПЭС [5–7], однако их единичный характер, наряду с высокой распространенностью ПЭС в Центральной России [8] и клинической значимостью ПЭС и ССГ, обусловливают необходимость дальнейшего углубленного изучения этого вопроса.
Цель исследования
Оценить влияние ПЭС на развитие и клиническое течение ССГ.
Материал и методы
В рамках поперечного исследования «случай – контроль» обследовано 120 пациентов (240 глаз) с ПЭС различной степени выраженности, составивших основную группу, и 120 лиц (240 глаз) без признаков ПЭС (контрольная группа). Основная и контрольная группы были сопоставимы по возрастно-половой структуре (табл. 1).
Выборка формировалась сплошным методом по мере госпитализации больных для планового хирургического лечения катаракты в профильные отделения. Критериями исключения являлись: глаукома, любые операции и травмы глаз в анамнезе, патологические процессы органа зрения, затрудняющие диагностику ПЭС (воспалительные заболевания сосудистого тракта, изменения роговицы и т. п.), общие заболевания (аутоиммунные, сахарный диабет), а также местное и общее использование медикаментозных средств, способных вызвать снижение стабильности слезной пленки и угнетение слезопродукции.
Всем пациентам проводилось стандартное офтальмологическое обследование, включавшее визометрию, биомикроскопию, тонометрию по Маклакову, офтальмоскопию. Диагноз ПЭС устанавливался при наличии псевдоэксфолиативных отложений по зрачковому краю радужки и/или на передней капсуле хрусталика (в условиях максимально достижимого медикаментозного мидриаза). Степень выраженности ПЭС оценивали по классификации Е.Б. Ерошевской (1997). Функциональные методы диагностики ССГ включали определение времени разрыва слезной пленки (ВРСП) (проба Норна) и величины суммарной слезопродукции (тест Ширмера I с использованием тест-полосок фирмы Bausсh & Lomb, Германия).
Статистическая обработка данных осуществлялась с использованием пакета прикладных программ Statistica 8.0 (StatSoftInc., США). Анализ выборок на соответствие закону нормального распределения проверяли критерием Колмогорова – Смирнова. Результаты представлены в таблицах в виде медианы (Me), верхнего и нижнего квартилей (Q25%; Q75%), а также в формате М±σ (где М – среднее значение, σ – стандартное отклонение среднего значения), что позволило сопоставить полученные данные с данными ранее опубликованных исследований. Выборки не подчинялись закону нормального распределения на уровне значимости p<0,05, в связи с чем достоверность различий групп оценивали с помощью Z-аппроксимации непараметрического U-критерия Манна – Уитни. Сравнение групп по качественным признакам проводилось с использованием критерия χ2 (метод Пирсона), при анализе взаимосвязи между признаками использовали непараметрический ранговый r-коэффициент корреляции Спирмена. Критический уровень значимости при проверке статистических гипотез принимался равным <0,05.
Результаты
Результаты функциональных проб в основной группе статистически значимо отличались от показателей контрольной группы. ВРСП и показатель суммарной слезопродукции (тест Ширмера I) у пациентов с ПЭС были снижены в сравнении с таковыми у лиц без признаков заболевания (табл. 2). Различия сохранялись как среди мужчин, так и среди женщин после стратификации исследуемых групп по полу (p<0,001 для обоих тестов). Доля глаз с клинически значимым снижением ВРСП (менее 10 с) в основной группе почти в 2 раза превысила аналогичные данные в контрольной группе (78,3% и 42,1% соответственно). Значение пробы Ширмера I менее 15 мм имело место в 92,1% глаз с ПЭС и 82,9% глаз в группе сравнения, менее 5 мм – в 7,1% и 2,9% соответственно.
При биомикроскопии частота обнаружения параллельных нижнему веку конъюнктивальных складок (конъюнктивохалазис, LIPCOF) при ПЭС значительно превышала показатель в группе сравнения. Данный признак определялся в 73,8% глаз с ПЭС против 52,9% глаз в контрольной группе (p=0,000002, χ2=22,428) (рис. 1).

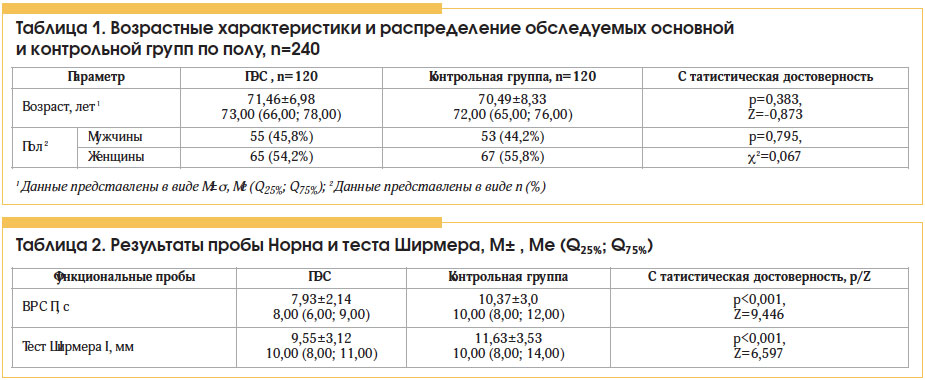
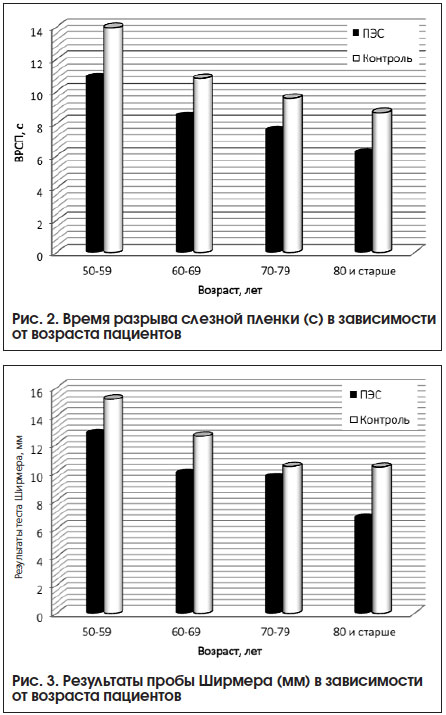
С увеличением возраста исследуемых наблюдалась тенденция к уменьшению ВРСП как в основной, так и в контрольной группе (коэффициент корреляции r=0,557 и r=0,502 соответственно; p<0,001). Статистически значимые различия показателей у пациентов с наличием ПЭС и без ПЭС сохранялись в каждой возрастной группе (p<0,001) (рис. 2). Аналогичная тенденция наблюдалась при использовании пробы Ширмера I (рис. 3) (коэффициент корреляции между результатами теста и возрастом обследуемых r=0,456 и r=0,461 соответственно; p<0,001).
Исследована зависимость стабильности прероговичной слезной пленки от степени выраженности псевдоэксфолиативного процесса. С возрастанием интенсивности псевдоэксфолиативных отложений, сопровождающихся более выраженными дистрофическими изменениями переднего отдела глаза, ВРСП сокращается. При ПЭС I степени этот показатель составил 9,0±1,74 с; 9,00 (8,00; 10,00), при II степени – 7,77±1,79 с; 8,00 (7,00; 9,00), при III стадии заболевания – 6,76±2,09 с; 6,50 (5,00; 7,00) (p1,2=0,002, Z=3,309; р2,3=0,0004, Z=3,515).
Результаты пробы Ширмера I также находились в обратной зависимости от стадии ПЭС, снижаясь с 10,81±2,59; 10,00 (9,00; 12,00) при ПЭС I степени до 9,43±2,51; 9,00 (8,00; 10,00) при II степени и 8,65±3,26; 9,00 (7,00; 11,00) при III степени выраженности синдрома (p1,2=0,025, Z=2,236; р2,3=0,106, Z=1,619).
Данные литературы свидетельствуют о том, что при электронно-микроскопических исследованиях конъюнктивы парных глаз, клинически не вовлеченных в процесс, признаки ПЭС выявляются в 100% случаев. Следовательно, термины «односторонний» или «двусторонний» ПЭС не совсем верны, и речь надо всегда вести об ассиметричном поражении [9, 10]. В случаях, когда клинически ПЭС определялся только с одной стороны, показатель ВРСП на пораженном глазу был статистически значимо меньше. Значение пробы Норна составило 8,5±2,1 с; 8,0 (7,0; 10,0) на глазу с клинической манифестацией ПЭС и 9,9±1,7 с; 10,0 (9,0; 10,0) – на парном (p=0,001; Z=3,335). Средние значения теста Ширмера I на глазах с клинически определяемым заболеванием также оказались несколько ниже – 10,7±2,42 мм; 10,0 (9,0; 12,0) в сравнении с 11,6±2,42 мм; 11,0 (9,0; 10,0) на парном глазу, впрочем, не достигая статистически достоверных различий (p=0,139; Z=1,481). Следует отметить, что показатели ВРСП и теста Ширмера I в основной группе на глазах без клинической манифестации ПЭС хотя и были ниже, чем в контрольной группе, также не достигали статистически значимых различий (p=0,403; Z=-0,836 и p=0,924; Z=0,010 соответственно).
Обсуждение
К настоящему времени установлено, что псевдоэксфолиативный процесс может поражать большинство тканей глаза. ПЭС ассоциирован со значительным количеством заболеваний и патологических состояний органа зрения, в т. ч. с глаукомой, катарактой, нарушением гематоофтальмического барьера, дистрофическими изменениями переднего отдела глаза [3]. Использование электронной микроскопии позволило обнаружить псевдоэксфолиативный материал в конъюнктиве век и глазного яблока [10]. В ряде опубликованных ранее работ показано, что наличие ПЭС может коррелировать с изменениями функциональных показателей слезы, характерных для ССГ. Обоснованием этого факта можно считать данные, касающиеся изменения морфологии бокаловидных клеток конъюнктивы на фоне ПЭС, что, в свою очередь, может оказать влияние на муциновый слой прероговичной слезной пленки [6].
В данном исследовании установлено снижение показателей ВРСП и суммарной слезопродукции в группе пациентов с ПЭС в сравнении с контрольной группой, что позволяет отнести псевдоэксфолиативный процесс к факторам риска развития ССГ. Полученные данные говорят об ухудшении функциональных показателей слезы с увеличением возраста обследуемых, что соответствует физиологическим особенностям организма пожилого человека, однако в каждой возрастной группе сохранялись статистически значимые различия между больными с ПЭС и группой сравнения.
Результаты исследования свидетельствуют о прямой зависимости между степенью выраженности ПЭС и характером угнетения ВРСП и результатами теста Ширмера I. Это подтверждается снижением изучаемых показателей по мере увеличения стадии заболевания, а также их значимым ухудшением в глазах с наличием ПЭС в сравнении с парными глазами без признаков отложения псевдоэксфолиативного материала при клинически одностороннем процессе.
ПЭС – фактор, значительно увеличивающий риск развития и прогрессирования катаракты и глаукомы. Хирургия катаракты сама по себе может вызвать развитие ССГ либо усугубить течение уже имеющегося процесса. Глаукома требует длительного использования местной гипотензивной терапии, способной вызвать развитие ССГ [11–15]. В этой связи необходимо учитывать предрасположенность к ССГ у лиц с ПЭС при выборе препарата для медикаментозной терапии и тактики хирургического лечения данных групп больных [16, 17].
Заключение
Полученные данные свидетельствуют об изменениях функциональных показателей суммарной слезопродукции и стабильности прероговичной слезной пленки у пациентов с ПЭС. Это может рассматриваться как факт предрасположенности данной категории больных к развитию ССГ. Установлена зависимость изменений слезопродукции и ВРСП от степени выраженности ПЭС. С учетом частоты возникновения у таких больных глаукомы и, соответственно, перспективы использования местных гипотензивных средств, способных вызвать либо усугубить течение ССГ, очевидны необходимость дополнительного обследования этой категории пациентов и адекватный выбор терапии, а также своевременное назначение препаратов «искусственной слезы».
Источник
Псевдоэксфолиативной глаукомой (ПЭГ), принято называть достаточно распространенную разновидность открытоугольной глаукомы, которая сопровождается развитием тяжелых дистрофических изменений в средах глаза со скоплением в зоне хрусталика и ресничного тела белых отложений.
Этим заболеванием в большей степени страдают женщины. Риск глаукомы увеличивается после возникновения псевдоэксфолиативного синдрома.
Примерно в 25% случаев ПЭГ у пациентов выявляется офтальмогипертензия. Частота данного заболевания у лиц с глаукомой напрямую связана с распространенностью в регионе проживания псевдоэксфолиативного синдрома. Методов профилактики ПЭГ не существует.
Механизм развития заболевания
Факторами развития псевдоэксфолиативной глаукомы являются деструктивные процессы, происходящие в базальной мембране хрусталикового эпителия, трабекул, цилиарного тела или радужки.
Активация данных процессов, приводит к выработке псевдоэксфолиативного материала. Этот, сероватого оттенка материал, состоит из фибрилл, при грануляции, откладывающихся на конъюнктиве и стекловидном теле. Такими отложениями перекрывается межтрабекулярное пространство и отток внутриглазной жидкости блокируется. Это становится причиной увеличения уровня внутриглазного давления.
Классификация ПЭГ
Специалисты-офтальмологи имеют разные взгляды на развитие данного заболевания, что и отразились в существующих ее классификациях. Отечественные ученые, склонны рассматривать ПЭГ, как один из видов первичной открытоугольной глаукомы. При этом, основным фактором развития заболевания признается псевдоэксфолиативный синдром (ПЭС).
В зарубежных источниках, глаукому на фоне ПЭС называют вторичной и не ограничивают открытым углом.
Мировая и российская научная офтальмология не продвинулись дальше попыток применения ПЭС классификационных схем.
Наиболее логичную, клинически обоснованную классификацию заболевания, предложили немецкие офтальмологи. В ее основе – выявление изменений, которые появляются на передней хрусталиковой капсуле. Согласно этой классификации, отдельно выделяются:
- Подозрение на ПЭС.
- Клинически определенный псевдоэксфолиативный синдром.
К первому пункту относится стадия раннего, скрытого ПЭС. В этот период выявляются отложения псевдоэксфолиативного материала на передней камере гомогенным слоем, получившим определение «матового стекла». Скрытый ПЭС сопровождается появлением задних синехий.
Дальнейшее развитие болезни приводит к стадии «мини-ПЭС», которая заканчивается формированием классического синдрома. Этот период характеризуется локальным возникновением нарушений прекапсулярного слоя, появляющихся, как правило, в верхней хрусталиковой зоне.
Благодаря электронной микроскопии удалось определить и доклиническую стадию заболевания.
Более адаптированной к практике представляется классификация, предложенная проф. Е. Б. Ерошевской. Она учитывает характер и выраженность атрофии в радужке, а также объем эксфолиативных отложений. Согласно ей:
- 1 стадия заболевания – это легкая атрофия радужки, с незначительными наслоениями по краю зрачка, а также передней капсулы хрусталика.
- 2 стадия заболевания – выраженные накопления, перераспределение пигмента и атрофия пигментной зрачковой каймы.
- 3 стадия заболевания – значительная атрофия пигментной зрачковой каймы и радужки, отложения приобретают форму целлофановой пленки.
Необходимо упомянуть, что характеристики ПЭС, не ограничиваются биомикроскопией. Четвертая стадия ПЭС была установлена по итогам ультразвуковых исследований, опираясь на данные об интенсивности эксфолиативных отложений, их локализации, состояния волокон цинновой связки, а также наличия иных типов структурных изменений переднего сегмента глаза.
Симптомы заболевания
При псевдоэксфолиативной глаукоме больные могут ощущать следующее:
- Нарастающую к вечеру усталость глаз.
- Полноту и давление в глазах.
Кроме того, отмечается болезненность в глазном яблоке, появление красных кругов перед глазами при взгляде на яркий свет, «пелена» на глазах.
При возникновении приступа, из-за повышения давления начинаются головные боли. При прогрессировании глаукомы ухудшается периферическое зрение, что влечет за собой необратимое снижение остроты зрения всей области зрительного поля. Эти патологические изменения, в итоге приводят к слепоте.
Диагностика заболевания
Диагностика заболевания начинается со сбора анамнеза с учетом жалоб больного на ухудшение зрения, возникновение «пелены» перед глазами, чувство давления. Для подтверждение диагноза, проводят детальное исследование с применением таких методов, как:
- Рефрактометрия;
- Определение остроты зрения;
- Тонография;
- Биомикроскопия радужки, роговицы, а также отделов передней камеры глаза;
- Эластотонометрия;
- Тонометрия с определением внутриглазного давления;
- Гониоскопия с обследованием угла передней камеры;
- Офтальмоскопия;
- Периметрия.
Диагноз считается подтвержденным, если тонометрия выявляет повышенное внутриглазное давление, а визуально устанавлено наличие псевдоэксфолиативных отложений на радужке, трабекулах, хрусталике.
Лечение ПЭГ
Терапия псевдоэксфолиативной глаукомы преследует цель торможения прогрессирования процесса или снижения его скорости, так как полностью ликвидировать процесс невозможно.
Наши врачи, которые сохранят Вам зрение при глаукоме:
В лечении заболевания применяют следующие методы:
- Хирургический;
- Лазерный;
- Медикаментозное лечение.
Консервативное лечение предусматривает назначение следующих групп препаратов:
- Для снижения секреции внутриглазной жидкости (Тимоптик, Бетоптик, Окупресс-Е);
- Для повышающие оттока внутриглазной жидкости по увеосклеральному каналу (Ксалатин, Траватан и пр.);
- Средства с комбинированным действием (Фотил), содержащие пилокарпин и тимолол;
- Ингибиторы карбоангидразы, для снижения выработки глазной влаги (Трусопт, Азатон).
Лазерное лечение применяют при невозможности медикаментозной терапии (непереносимость препаратов) или ее неэффективности. Это направление обычно включает:
- Лазерную трабекулопластику;
- Лазерную иридэктомию;
- Лазерную десцеметогониопунктуру.
Хирургическую операцию назначают в случае отсутствия результатов медикаментозного и лазерного лечения ПЭГ. В этом случае может быть назначена операция, призванная облегчить отток внутриглазной жидкости или вмешательство, в результате которого, выработка влаги сократится.
Раннее обнаружение и своевременная терапия данного заболевания, в большинстве случаев позволяет стабилизировать снижение зрения.
В медицинском центре «Московская Глазная Клиника» все желающие могут пройти обследование на самой современной диагностической аппаратуре, а по результатам – получить консультацию высококлассного специалиста. Клиника открыта семь дней в неделю и работает ежедневно с 9 ч до 21 ч. Наши специалисты помогут выявить причину снижения зрения, и проведут грамотное лечение выявленных патологий.
Уточнить стоимость той или иной процедуры, записаться на прием в “Московскую Глазную Клинику” Вы можете по телефонам в Москве 8 (800) 777-38-81, 8 (499) 322-36-36 (ежедневно с 9:00 до 21:00) или воспользовавшись формой онлайн-записи.
Источник
Псевдоэксфолиативный синдром относится к дистрофическим заболеваниям и редко диагностируется у пациентов в возрасте до 45 лет. При этом недуге на передних отделах глазного яблока, соприкасающихся с внутриглазной жидкостью, начинает откладываться экстрацеллюлярное вещество. Псевдоэксфолиативный синдром глаза нередко ведёт к дистрофии радужной оболочки, возникновению катаракты и глаукомы хронической формы. Именно поэтому при его диагностировании требуется срочно приступить к лечению.
Характеристика заболевания
Псевдоэксфолиативный синдром – офтальмологическая патология, спровоцированная обменно-дистрофическими изменениями в глазном яблоке и дегенеративными процессами в радужной оболочке. При этом поражении на хрусталике образуется тончайшая плёнка из отложений, которая подворачивается под хрусталик. Опасность недуга заключается в том, что при отсутствии лечения он может стать причиной развития глаукомы и катаракты, а также спровоцировать помутнение хрусталика. Как показывает медицинская практика, избежать необратимых последствий можно только при своевременном обращении к специалисту. Если болезнь будет диагностирована в запущенном состоянии, предотвратить осложнения будет фактически невозможно.
В ходе многочисленных клинических исследований было выявлено, что развитие болезни связано с возрастом пациента. В группу риска попадают люди старше 50. После этого возраста вероятность развития недуга составляет около 30%.
Причины развития
Несмотря на многочисленные клинические исследования, этиология заболевания до сих пор не изучена до конца. Считается, что спровоцировать отложение белково-фиблярных и пигментных структур на хрусталике могут следующие факторы:
- разрушение и дисфункция капилляров глаза вследствие дистрофических процессов;
- структурные изменения тканей глаза;
- травмирование глазных органов;
- внутриглазные инфекционные заболевания;
- ослабление защитных сил местного иммунитета;
- негативное воздействие на органы зрения ультрафиолета;
- расстройства ЦНС, ведущие к ухудшению кровотока в капиллярах цилиарного тела;
- патологические биохимические процессы;
- генетическая предрасположенность.
В группы риска по развитию этого недуга попадают люди, злоупотребляющие курением, а также пациенты, страдающие от сердечно-сосудистых заболеваний, гипертонии и атеросклероза.
Симптомы
Опасность псевдоэксфолиативного синдрома заключается в том, что на начальных этапах он протекает практически бессимптомно, из-за чего болезнь обычно диагностируется в запущенном состоянии. Симптоматика становится заметной ближе к третьей стадии, на которой начинается разрушение связочного аппарата хрусталика. Большинство пациентов при этом жалуются на появление отложений в переднем углу глаза и ухудшение зрительной функции. Если не обратиться в клинику, болезнь будет прогрессировать и станет причиной развития глаукомы.
На этом этапе могут наблюдаться следующие симптомы:
- ухудшение зрения одного глаза (более чем в 75% случаев болезнь поражает сначала левый глаз, и только через несколько лет возникают двусторонние изменения);
- расплывчатость и раздвоение предметов;
- появление черных точек перед глазами;
- сложности во время чтения.
При ПЭС во время проведения комплексной диагностики офтальмолог заметит помутнение хрусталика, появление отложений в углу глаза и пигментирование трабекулярных клеток.
Способы диагностики
Выявить заболевание на начальном этапе практически невозможно. Единственное обследование, в ходе которого можно заподозрить развитие ПЭС, – ультразвуковая биомикроскопия.
На более поздних этапах диагностирование псевдоэксфолиативного синдрома проводится при помощи:
- глазная биомикроскопия. Позволяет рассмотреть отложения на поверхностных оболочках переднего отдела глазного яблока;
- гониоскопия. Визуальное исследование передней камеры глаза;
- ультразвуковое исследование. УЗИ позволяет обнаружить деструктивные нарушения и изменение размеров переднего и заднего сегмента глаза;
- ультразвуковая биомикроскопия. При помощи этого обследования можно обнаружить даже микроскопические точечные включения на оболочке глаза;
- визометрия. Методика, использующаяся для определения качества зрения.
При подозрении на ПЭС для выявления общей клинической картины пациенту могут назначить дополнительные консультации невропатолога, ревматолога и других узкопрофильных специалистов.
Методы лечения
Цель лечения при псевдоэксфолиативном синдроме – минимизировать риск развития дальнейших осложнений. На ранних стадиях пациентам выписывают медикаменты следующих фармкатегорий:
- антиоксиданты. Подобные препараты разрушают активные формы кислорода, которые негативно влияют на ткани глазного яблока;
- антигипоксанты. Улучшают обменные процессы и регенерацию клеток;
- гипотензивные средства. Выписываются при повышенном внутриглазном давлении и признаках офтальмогипертензии;
- поливитаминные комплексы. При глазных заболеваниях особенно полезен ретинол, токоферол и витамин B6. Чаще всего витамины назначаются в форме глазных капель.
Если болезнь обнаружена в запущенном состоянии и сопровождается множественными осложнениями, медикаментозная терапия не принесёт эффекта. В этом случае единственный шанс сохранить зрение – проведение лазерного или хирургического вмешательства. Наиболее эффективным методом лечения псевдоэксфолиативного синдрома является лазерная трабекулопластика. Однако необходимо понимать, что через 3–4 года болезнь может вновь дать о себе знать.
Специалисты предупреждают, что даже замена хрусталика не поможет полностью устранить проблему. Именно поэтому пациенту придётся постоянно принимать лекарственные средства, помогающие поддержать зрительную функцию.
Прогноз и профилактика
При ПЭС прогноз для пациента зависит от того, на каком этапе была выявлена болезнь, а также от степени поражения структур глаза. При своевременной диагностике и грамотно подобранном лечении вероятность сохранения зрительной функции и предотвращения осложнения достаточно высока. Но если недуг будет обнаружен в запущенном состоянии, предотвратить развитие глаукомы и катаракты будет невозможно.
Что касается профилактических мер, то они до сих пор не разработаны. Именно поэтому всем людям, вне зависимости от состояния здоровья и возраста, рекомендуется каждые 6 месяцев посещать офтальмолога, который сможет своевременно заметить деструктивные изменения и назначить подходящую схему лечения.
Псевдоэксфолиативный синдром – опаснейшая офтальмологическая патология, которая нередко приводит к серьёзным осложнениям. Поскольку недуг крайне сложно поддаётся лечению, намного разумнее постараться предотвратить его развитие. Всё, что для этого требуется, – регулярно посещать офтальмолога и своевременно лечить заболевания глаз.
Источник
