Синдром печеночно клеточной недостаточности патофизиология
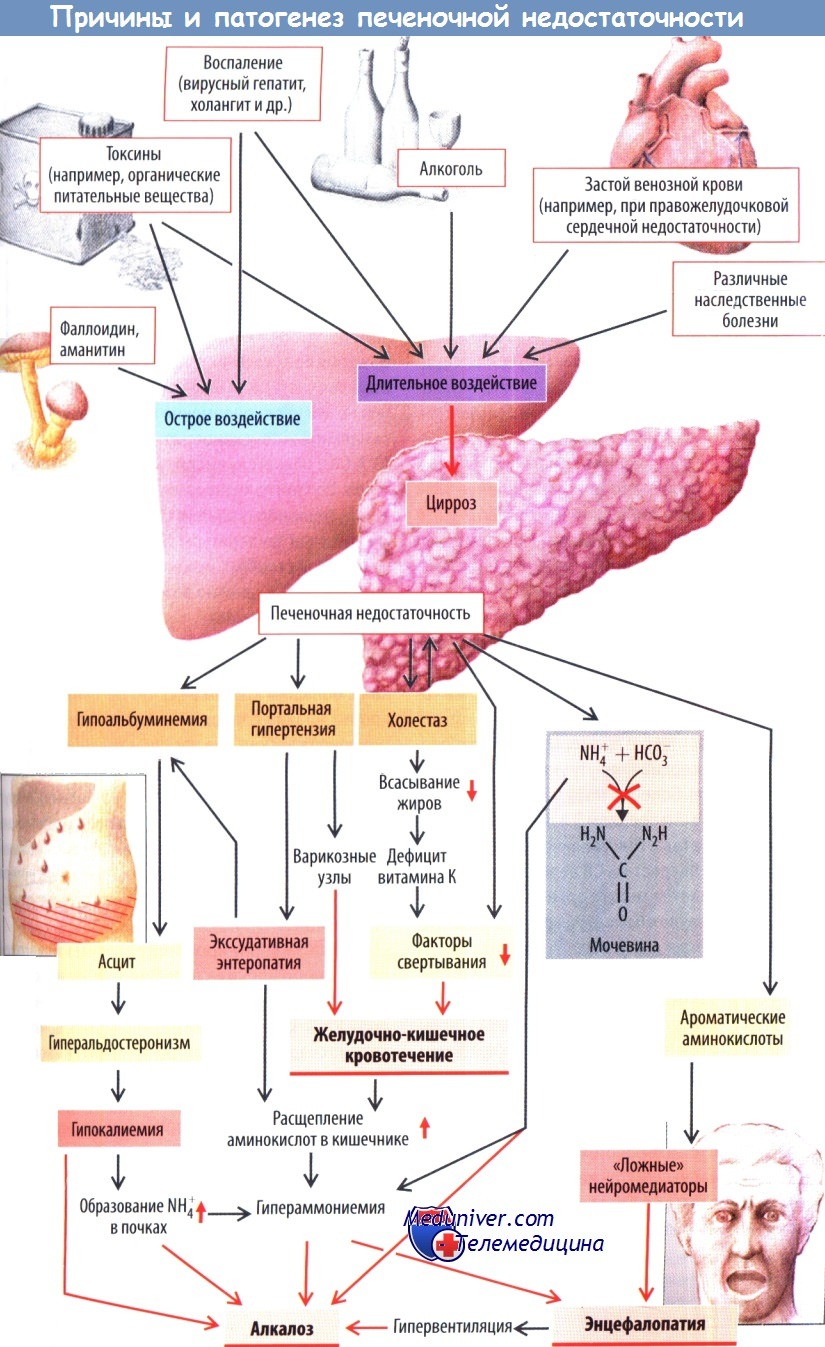
Патофизиология острой печеночной недостаточности.Нарушение углеводного обмена. Печень теряет способность синтезировать глюкозу из жиров и белков, т. е. нарушается глюконеогенез, поддерживающий определенный уровень глюкозы в крови. Запасы синтезируемого из глюкозы гликогена значительно снижаются. При этом ни глюкагон, ни адреналин не вызывают увеличения гликемии из-за отсутствия запасов гликогена. Кроме того, нарушение ресинтеза глюкозы из молочной кислоты приводит к развритию лактат-ацидоза. Нарушение жирового обмена.Количество гликогена в печени обратно пропорционально количеству жира. При снижении гликогена в печени активируется гипоталамо-гипофизарно-адренокортикалъная система, которая влияет на жировые депо. Жир поступает в печень на короткое время, включается (с участием холина) в состав фосфолипидов и в таком виде поступает в кровь. При недостатке холина синтез фосфолипидов и жиров становится невозможным, жиры начинают задерживаться в печени, откладываются там, что в конечном итоге приводит к жировой инфильтрации, а затем и жировой дистрофии печени, которая является универсальной реакцией на ее повреждение. При поражении печени в ней усиливается образование ацетоновых тел (кетонемия и ацидоз), нарушается обмен холестерина (синтез, эстерификация, выделение в желчь и в кровь). Нарушение белкового обмена.При поражении печени снижается срштез альбуминов, а- и бета-глобулинов, протромбина, фибриногена, образуются патологические белки – парапротеины. Развитию и прогрессированию отеков способствует гиперальдостеронемия (нарушение разрушения гормона в печени), которая увеличивает реабсорбцию ионов натрия и выведение рюнов калия почками, снижая при этом диурез и задерживая в организме воду. Аммиак, ослабляя тормозные процессы в ЦНС, способствует возникновению гиперкинезов и судорог. В высоких концентрацих аммиак раздражает дыхательный центр и усиливает одышку, а возникающий при этом респираторный алкалоз снижает мозговой кровоток, уменьшает потребление кислорода мозгом, нарушает энергетический обмен, что в конечном итоге приводит к отеку мозга.
Патогенез геморрагического синдрома.При поражении печени вначале снижается синтез VII, затем II, IX, X, а при тяжелой печеночно-клеточной недостаточности – и I, V, VIII факторов свертывания крови. Повышенное потребление факторов свертывания крови возникает в результате выделения в кровь из поврежденных клеток печени тромбопластиночных факторов, ведущих к образованию тромбоцитарных тромбов и активации фибринолитической системы. Обеспечение этих процессов требует повышенного количества I, II, V, VII, IX, XI факторов, что приводит к развитию коагулопатии потребления и, как следствие, тромбогеморрагическому синдрому. Патогенез синдрома холемии.Выделяемая в течение суток желчь (500-1000 мл) в кишечнике эмульгирует жиры, активирует липазы панкреатического сока, способствует всасыванию жирорастворимых витаминов и жирных кислот, усиливает перистальтику кишечника. Патогенез гепаторенального синдрома.Гепаторенальный синдром включает развитие патологии печени и функциональную почечную недостаточность. Последняя провоцируется острой гиповолемией, назначением избыточных доз диуретиков. Усугубляющими факторами могут быть дегидратация, назначение НСПВС, натриевой соли пенициллина. Непосредственной причиной функциональной почечной недостаточности является внутрипочечная вазоконстрикция и ишемия. Причем, если пораженная печень не в состоянии инактивироватъ избыток катехоламинов, простагландинов, ангиотензина и других вазоактавных соединений, сосудистый спазм и ишемия почечной ткани существенно усиливается. Синдром проявляется выраженной азотемией, отсутствием угрожающего повышения концентрации калия в крови, увеличением осмолярности мочи, снижением натриурии (менее 10 ммоль/л). Патогенез печеночной энцефалопатии.Патогенез печеночной энцефалопатии объясняется метаболической теорией, в основе которой лежит нарушение детоксикационной функции печени и влияние токсических соединений на ЦНС. Шунтируемая кровь, содержащая конечные продукты распада белков, минуя печень, попадает в системный кровоток. Аммиак, низкомолекулярные жирные кислоты (у-аминомасляная кислота), серотонин, ложные медиаторы (тирамин, октапрамин и др.), действуя на головной мозг, вызывают нарушение энергетического метаболизма, передачу нервных импульсов и тем самым приводят к развитию печеночной энцефалопатии. – Также рекомендуем “Клиника острой печеночной недостаточности.” Оглавление темы “Печеночная недостаточность.”: |
Источник
Печеночно-клеточная недостаточность.Печеночно-клеточная недостаточность возникает при массивном некрозе паренхимы печени, в результате вирусного гепатита, острых отравлений гепатотоксичными ядами, перевязки печеночной артерии вблизи печени, при хроническом холестазе, когда значительно нарушаются ее гомеостатическая и барьерная функции. Развитие массивного некроза печени подтверждается быстро прогрессирующим уменьшением ее размеров – так называемым синдромом “таяния печени”: печень становится дряблой, тестоватой, перестает пальпироваться нижний край, уменьшается и исчезает зона печеночной тупости. В крови накапливается большое количество церебротоксических веществ, которые нарушают энергетический барьер и передачу нервных импульсов, синтезируются ложные нейромедиаторы, серотонин, в связи с угнетением гликонеогенеза развивается гипогликемия. Метаболический ацидоз, связанный с накоплением молочной и пировиноградной кислот (нарушение проницаемости клеточных мембран и отек мозга), вызывает гипервентиляцию и респираторный алкалоз, который в свою очередь нарушает мозговой кровоток, усугубляя гипоксию ткани мозга. Диагноз отека мозга устанавливается клинически по наличию признаков раздражения мозговых оболочек, гиперемии и потливости лица, судорожных подергиваний, глазодвигательных расстройств, прогрессирующих нарушений дыхания, артериальной гипертензии. У больных печеночно-клеточной недостаточностью уровень прокоагулянтов (протромбин, фибриноген), холиэстеразы, холестерина, альбумина в сыворотке крови снижается, причем уменьшение каждого показателя рассматривается как индикатор гепатодепрессии. Характерна выраженная гипербилирубинемия преимущественно за счет роста конъюгированной формы фермента. Желтуха является проявлением степени повреждения гепатоцитов и указывает на неблагоприятный исход.
Биохимическим отражением цитолиза является повышенная активность аминотрансфераз, достигающих высокого уровня при быстрой деструкции печеночной ткани. Более высокий подъем АсАТ по сравнению с АлАТ считается неблагоприятным признаком. Отмечается гипермия конечностей, скачущий пульс, капиллярная пульсация. Сердечный выброс увеличен, что клинически выражается тахикардией, усиленным сердечным толчком, систолическим шумом. Артериальная гипотензия усугубляет нарушение кровотока в печени и обусловливает развитие ОПН, а также способствует нарушению психического статуса. Примечательно, что коррекция артериальной гипотензии адреномиметаками приводит лишь к кратковременному эффекту. ОПСС снижается, артериовенозная разница по кислороду и доставка кислорода уменьшаются. Вазолилятация при печеночно-клеточной недостаточности способствует прогрессированию гипоксии тканей. Снижение ОЦК в результате дилятации артериол под воздействием оксида азота активирует симпатоадреналовую и ренин-альдостероновую системы, что приводит к задержке натрия и воды и способствует развитию асцита. При массивном некрозе печени кома, развивающаяся в первые дни заболевания, отличается особой скоротечностью. Такой вариант печеночно-клеточной недостаточности получил название фульминантной. Наиболее характерными симптомами печеночно-клеточной недостаточности являются “печеночный” запах изо рта, желтуха, уменьшение размеров печени, кровоточивость и прогрессирующие признаки энцефалопатии. “Печеночный” запах изо рта можно сравнить с запахом недавно вскрытого трупа или с мышиным запахом. При остром поражении печени “печеночный” запах, распространяющийся на всю палату, где находится больной, расценивается как предшественник комы. Желтуха у больных с острой печеночной недостаточностью, как правило, бьюает интенсивной, особенно в период развития комы. На коже лица могут появляться малиново-красные сливающиеся пятна, причем их интенсивность зачастую коррелирует с тяжестью комы. Геморрагический синдром проявляется кровоизлияниями в области склер, под кожу локтевых сгибов, на голенях, ягодицах. Отмечаются кровоизлияния в местах инъекций. Носовые кровотечения наблюдаются редко. Критические состояния, связанные с кровотечениями, нарушением электролитного баланса, использованием седативных средств, наркотических аналгетиков, также способствуют прогрессированию печеночной энцефалопатии и комы.
– Также рекомендуем “Печеночная энцефалопатия. Причины печеночной энцефалопатии.” Оглавление темы “Печеночная недостаточность.”: |
Источник
ГЛАВА 25. ПАТОЛОГИЯ ПЕЧЕНИ
Печень
– один из основных органов, обеспечивающих гомеостаз организма.
Различные формы патологии печени проявляются признаками недостаточности
функций печени (печёночной недостаточности) или синдрома желтухи.
ПЕЧЁНОЧНАЯ НЕДОСТАТОЧНОСТЬ
Печёночная
недостаточность – стойкое снижение или полное выпадение одной,
нескольких или всех функций печени, приводящее к нарушению
жизнедеятельности организма.
КЛАССИФИКАЦИЯ
По
различным критериям (масштаб повреждения, происхождение, скорость
возникновения, обратимость повреждений) выделяют несколько видов
печёночной недостаточности.
• По происхождению:
♦ Печёночноклеточная
(паренхиматозная). Является результатом первичного повреждения
гепатоцитов и недостаточности их функции.
♦ Шунтовая
(обходная). Обусловлена нарушением тока крови в печени и, в связи с
этим, её сбросом (минуя печень) по портокавальным анастомозам в общий
кровоток.
• По скорости возникновения и развития:
♦ Молниеносная, или фульминантная. Развивается в течение нескольких часов.
♦ Острая. Развивается в течение нескольких суток.
♦ Хроническая. Формируется в течение нескольких недель, месяцев или лет.
• В зависимости от обратимости повреждения гепатоцитов:
♦ Обратимая.
Исчезновение признаков печёночной недостаточности наблюдается при
прекращении воздействия патогенного агента и устранении последствий
этого воздействия.
♦ Необратимая
(прогрессирующая). Развивается в результате продолжающегося влияния
причинного фактора или неустранимости патогенных изменений, вызванных
им.
ЭТИОЛОГИЯ
Причины развития недостаточности печени могут быть собственно пе- чёночными (гепатогенными) и внепечёночными (негепатогенными).
•
Внепечёночные: гипо- и дисвитаминозы, нарушения кровообращения,
гипоксия, хроническая почечная недостаточность, эндокринопатии.
•
Печёночные: наследственная патология печени, дистрофии, гепатиты,
циррозы, расстройства внутрипечёночного кровообращения, холестаз,
паразитарные поражения, опухоли.
Дистрофии печени
наиболее часто развиваются под действием химических веществ (например,
антибиотиков, наркотиков, бензола, этанола, нитрокрасок, ядовитых
грибов).
Гепатиты
Гепатит – воспаление печени. Обычно гепатиты возникают в результате вирусной инфекции или интоксикации.
Вирусные гепатиты –
группа полиэтиологичных вирусных воспалительных поражений печени.
Характеризуются развитием диффузного воспалительного процесса в
печёночной ткани с астеновегетативными и общетоксическими проявлениями,
желтухой, гепатоспленомегалией и рядом внепечёночных поражений (артриты,
узелковые периартерииты, гломерулонефриты и т.д.). В настоящее время
выделяют восемь типов возбудителей вирусного гепатита, обозначаемых
заглавными латинскими буквами, соответственно, от A до G и вирус TTV. Циррозы печени –
хронически протекающие патологические процессы в печени,
характеризующиеся прогрессирующим повреждением и гибелью гепатоцитов, а
также развитием избытка соединительной ткани (фиброзом). Проявляются
недостаточностью функций печени и нарушением кровотока в ней.
Нарушения кровообращения
Наибольшее
клиническое значение имеет развитие портальной гипертензии – стойкого
повышения давления в сосудах системы воротной вены выше нормы (выше 6 мм
рт.ст.). Наиболее частые причины:
♦ цирроз печени;
♦ шистосомоз;
♦ опухоли печени;
♦ гемохроматоз;
♦ блокада
притока крови по портальным сосудам (например, в результате сдавления,
окклюзии, аневризм, тромбозов ствола воротной или селезёночной вены);
♦ препятствие
оттоку крови от печени (например, при сердечной недостаточности; при
тромбозе, эмболии, сдавлении нижней полой вены).
Длительно текущая портальная гипертензия нередко приводит к дистрофии печени и её недостаточности.
ПАТОГЕНЕЗ
Воздействие
фактора, повреждающего гепатоциты, формирует развет- влённую сеть
взаимозависимых и взаимопотенцирующих изменений. Ведущие звенья
патогенеза печёночной недостаточности следующие:
♦ модификация и деструкция мембран гепатоцитов;
♦ активация иммунопатологических процессов;
♦ развитие воспаления;
♦ активация свободнорадикальных реакций;
♦ активация гидролаз.
Перечисленные
факторы вызывают массированное разрушение клеток печени, что приводит к
дополнительному потенцированию воспалительных, иммунопатологических и
свободнорадикальных реакций. Всё это приводит к снижению массы
функционирующей печёночной паренхимы и развитию печёночной
недостаточности.
ПРОЯВЛЕНИЯ
Расстройства обмена веществ
• Белки
♦ Нарушение
синтеза гепатоцитами альбуминов, проявляющееся гипоальбуминемией и
диспротеинемией. Гипоальбуминемия способствует развитию отёков и
формированию асцита.
♦ Торможение синтеза белков
системы гемостаза (проконвертина, проакцелерина, фибриногена,
протромбина, факторов Кристмаса и Стюарта-Прауэр, антикоагулянтных
белков C и S), что приводит к гипокоагуляции белков крови, развитию
геморрагического синдрома.
♦ Снижение эффективности реакций дезаминирования аминокислот.
♦ Подавление
в гепатоцитах орнитинового цикла синтеза мочевины из токсичного для
организма аммиака и повышение его концентрации в крови.
• Липиды
♦ Нарушение
синтеза в печёночных клетках ЛПНП и ЛПОНП, а также ЛПВП нередко
сопровождается развитием липидной дистрофии печени (жирового гепатоза).
♦ Повышение в плазме крови уровня холестерина.
• Углеводы
♦ Подавление гликогенеза и глюконеогенеза.
♦ Снижение эффективности гликогенолиза.
Указанные
расстройства проявляются низкой резистентностью организма к нагрузке
глюкозой: гипогликемией натощак и гипергликемией вскоре после приё- ма
пищи, особенно углеводной.
• Витамины. При
печёночной недостаточности развиваются гипо- и дисвитаминозы (за счёт
нарушения высвобождения из продуктов питания и всасывания в кишечнике
жирорастворимых витаминов; снижения эффективности трансформации
провитаминов в витамины; торможения образования коферментов из
витаминов).
• Минеральные вещества (железо, медь, хром). Например, при гемохроматозе в ткани печени накапливается железо, развиваются гепатомегалия и цирроз.
Нарушение дезинтоксикационной функции печени
характеризуется снижением эффективности процессов обезвреживания в
печени: эндогенных токсинов (фенолов, скатолов, аммиака, путресцина,
кадаверинов, низкомолекулярных жирных кислот, сульфатированных
аминокислот и др.) и экзогенных ядовитых веществ (например,
ядохимикатов, ЛС, токсинов грибов и микробов).
Нарушение желчеобразования и желчевыделения проявляется развитием желтух и нарушений пищеварения.
Печёночная кома
При прогрессирующей печёночной недостаточности развивается кома.
Причины печёночной
комы: интоксикация организма в связи с повреждением и гибелью
значительной массы печени (при печёночнокле- точной, или паренхиматозной
коме) или сбросе крови из системы портальной вены в общий кровоток,
минуя печень (при шунтовой, или обходной коме).
Патогенез. Основные
факторы патогенеза печёночных ком: гипогликемия, ацидоз, дисбаланс
ионов, эндотоксинемия, расстройства кровообращения, полиорганная
недостаточность.
ЖЕЛТУХА
Желтуха
– избыточное содержание в крови, интерстициальной жидкости и тканях
компонентов жёлчи, обусловливающее желтушное окрашивание кожи, слизистых
оболочек и мочи.
Все виды желтух объединены одним
признаком – гипербилирубинемией, от которой зависит степень и цвет
окраски кожи: от светло-лимонной до оранжево-жёлтой, зелёной или
оливково-жёлтой (пожелтение кожи и склер начинается при концентрации
билирубина более 26 ммоль/л).
Метаболизм билирубина
•
Высвобождение гема из гемоглобина, миоглобина и цитохромов. Более
80% гема образуется в результате разрушения эритроцитов и около 20% –
миоглобина и цитохромов.
• Трансформация протопорфирина гема в биливердин. Происходит под влиянием микросомальных оксидаз гепатоцитов.
•
Окисление биливердина с образованием непрямого билирубина.
Непрямой билирубин, циркулирующий в крови, связан с альбуминами и
поэтому не фильтруется в почках и отсутствует в моче.
• Транспорт непрямого билирубина в гепатоциты, где он образует комплекс с белками и глутатион-S-трансферазами.
•
Диглюкуронизация билирубина в гепатоцитах с образованием
растворимого в воде конъюгированного билирубина. Прямой билирубин не
связан с альбумином. В связи с этим он активно («прямо») взаимодействует
с диазореактивом Эрлиха, выявляющим этот пигмент.
• Экскреция конъюгированного билирубина в желчевыводящие пути.
• Трансформация конъюгированного билирубина:
♦ в
уробилиноген (в верхнем отделе тонкого кишечника), всасывающийся в
тонком кишечнике и попадающий по системе воротной вены в печень, где он
разрушается в гепатоцитах;
♦ в стеркобилиноген (в
основном в толстом кишечнике), большая часть которого выделяется с
экскрементами, окрашивая их; другая часть всасывается в кровь
геморроидальных вен, попадает в общий кровоток и фильтруется в почках (в
норме придавая моче соломенно-жёлтый цвет).
КЛАССИФИКАЦИЯ ЖЕЛТУХ
По
этиопатогенезу различают механическую, паренхиматозную и гемолитическую
желтухи. В клинической практике существует множество терминов,
относящихся к разным заболеваниям, сопровождающимися желтухой. Все
желтухи в зависимости от происхождения подразделяют на две группы:
печёночные и непечёночные.
• Печёночные желтухи (паренхиматозные и энзимопатические) возникают при первичном повреждении гепатоцитов.
•
Непечёночные желтухи первично не связаны с повреждением
гепатоцитов. К ним относятся гемолитические (надпечёночные) и
механические (подпечёночные) желтухи.
Паренхиматозные желтухи
ЭТИОЛОГИЯ
♦ Инфекционные причины: вирусы, бактерии, плазмодии.
♦ Неинфекционные
причины: органические и неорганические гепатотоксические вещества
(например, четырёххлористый углерод, этанол, парацетамол и др.),
гепатотропные АТ и цитотоксические лимфоциты, новообразования.
СТАДИИ ПАРЕНХИМАТОЗНОЙ ЖЕЛТУХИ
Характер
и выраженность нарушений функций печени зависит от степени альтерации и
массы повреждённых гепатоцитов. Характер расстройств желчеобразования и
желчевыведения и степень их выраженности на разных этапах (стадиях)
патологического процесса различны.
Первая стадия (преджелтушная)
Причины: в
гепатоцитах снижается активность ферментов, разрушающих уробилиноген;
повреждение мембран гепатоцитов, снижение активности
глюкуронилтрансферазы.
Проявления: уробилиногенемия и уробилиногенурия, увеличение содержания «печёночных» ферментов в крови.
Вторая стадия (желтушная)
Причины. Для
желтушной стадии характерно дальнейшее усугубление альтерации
гепатоцитов и их ферментов. Это приводит к нарушению работы
«билирубинового конвейера». Расстройство этого механизма, в совокупности
с повреждением мембран клеток, обусловливает нарушение
однонаправленного транспорта билирубина. Проявления: выход
прямого билирубина в кровь и развитие билирубинемии, фильтрация прямого
билирубина почками и его экскреция с мочой, попадание компонентов жёлчи в
кровь и развитие холемии.
Третья стадия
Причины: прогрессирующее
уменьшение активности глюкуронилтрансферазы гепатоцитов приводит к
нарушению трансмембранного переноса конъюгированного билирубина в
гепатоциты и торможению процесса глюкуронизации билирубина.
Проявления
♦ Нарастание уровня непрямого билирубина в крови.
♦ Уменьшение содержания в крови прямого билирубина (как результат подавления реакции глюкуронизации).
♦ Снижение концентрации стеркобилиногена в крови, моче и экскрементах.
♦ Уменьшение
содержания уробилиногена в крови и, как результат – в моче. Является
результатом малого поступления прямого билирубина в желчевыводящие пути и
кишечник.
♦ Усугубление повреждения структур и
ферментов гепатоцитов с нарастанием холемии, сохранением ферментемии и
гиперкалиемии, прогрессированием печёночной недостаточности, что чревато
развитием комы.
Энзимопатические желтухи
Различают энзимопатические желтухи наследуемые (первичные) и приобретённые (вторичные)
•
Первичные энзимопатии развиваются при генных дефектах ферментов и
белков, обеспечивающих метаболизм пигментного обмена в гепатоцитах.
Существует несколько нозологических форм, относящихся к этой группе
желтух: синдром Жильбера (семейная негемолитическая желтуха), синдром
Дабина-Джонсона, синдром Криглера-Найяра, синдром Ротора и другие.
•
Приобретённые (вторичные) нарушения свойств ферментов,
участвующих в метаболизме жёлчных пигментов и синтезе компонентов
мембран гепатоцитов развиваются вследствие интоксикации организма
(например, этанолом, четырёххлористым углеродом, парацетамолом,
хлорамфениколом), инфекционных поражений печени (например, вирусами);
повреждений гепатоцитов АТ, цитотоксическими лимфоцитами и макрофагами.
Внепечёночные желтухи ГЕМОЛИТИЧЕСКАЯ ЖЕЛТУХА
Причины
♦ Внутри- и внесосудистый гемолиз эритроцитов.
♦ Гемолиз эритроцитов и их предшественников в костном мозге.
♦ Синтез неконъюгированного билирубина из негемоглобинового гема в печени, костном мозге.
♦ Образование избытка неконъюгированного билирубина при инфаркте органов, скоплении крови в тканях, органах, полостях тела.
Проявления
♦ Признаки повреждения гепатоцитов: симптомы печёночной недостаточности, присоединение паренхиматозной желтухи.
♦ Признаки гемолиза эритроцитов: анемия, гемическая гипоксия, гемоглобинурия, уробилиногенемия и уробилиногенурия, повы-
шение в крови концентрации неконъюгированного билирубина, увеличение концентрации стеркобилиногена в крови, моче, кале.
МЕХАНИЧЕСКАЯ ЖЕЛТУХА
Этиология
Механическая
желтуха развивается при стойком нарушении выведения жёлчи по жёлчным
капиллярам (что приводит к внутрипечёноч- ному холестазу), по жёлчным
протокам и из жёлчного пузыря (с развитием внепечёночного холестаза).
Причинные факторы:
♦ Закрывающие желчевыводящие пути изнутри (например, конкременты, опухоли, паразиты).
♦ Сдавливающие
жёлчные пути снаружи (например, новообразования головки поджелудочной
железы или большого дуоденального сосочка; рубцовые изменения ткани
вокруг желчевыводящих путей; увеличенные лимфатические узлы).
♦ Нарушающие тонус и снижающие моторику стенок желчевыводящих путей (дискинезии).
Патогенез. Указанные
факторы обусловливают повышение давления в жёлчных капиллярах,
перерастяжение (вплоть до микроразрывов) и повышение проницаемости
стенок желчеотводящих путей, диффузию компонентов жёлчи в кровь. При
этом развивается билиарный гепатит.
Проявления механической желтухи
Для механической (подпечёночной, застойной, обтурационной) желтухи характерно развитие холемии и ахолии.
• Синдром холемии (желчекровия)
– комплекс расстройств, обусловленных появлением в крови компонентов
жёлчи, главным образом жёлчных кислот (гликохолевой, таурохолевой и
др.), прямого билирубина и холестерина. Признаки холемии:
♦ Высокая
концентрация конъюгированного билирубина в крови (с развитием желтухи)
и, как следствие – в моче (придает моче тёмный цвет).
♦ Избыток
холестерина поглощается макрофагами и накапливается в виде ксантом (в
коже кистей, предплечий, стоп) и ксантелазм (в коже вокруг глаз).
♦ Зуд кожи вследствие раздражения жёлчными кислотами нервных окончаний.
♦ Артериальная
гипотензия вследствие снижения базального тонуса ГМК артериол,
уменьшение адренореактивных свойств рецепторов сосудов и сердца,
повышения тонуса блуждающего нерва под действием жёлчных кислот.
♦ Брадикардия вследствие прямого тормозного влияния жёлчных кислот на клетки синусно-предсердного узла.
♦ Повышенная
раздражительность и возбудимость пациентов в результате снижения
активности тормозных нейронов коры больших полушарий под действием
компонентов жёлчи.
♦ Депрессия, нарушение сна и бодрствования, повышенная утомляемость (развивается при хронической холемии).
Синдром ахолии –
состояние, характеризующееся значительным уменьшением или прекращением
поступления жёлчи в кишечник, сочетающееся с нарушением полостного и
мембранного пищеварения. Признаки ахолии:
♦ Стеаторея
– потеря организмом жиров с экскрементами в результате нарушения
эмульгирования, переваривания и усвоения жира в кишечнике (обусловлена
дефицитом жёлчи).
♦ Дисбактериоз.
♦ Кишечная
аутоинфекция и интоксикация вследствие отсутствия бактерицидного и
бактериостатического действия жёлчи. Это способствует активации
процессов гниения и брожения в кишечнике и развитию метеоризма.
♦ Полигиповитаминоз
(в основном, за счёт дефицита витаминов A, D, E и K). Дефицит
жирорастворимых витаминов приводит к нарушению сумеречного зрения,
деминерализации костей с развитием остеомаляции и переломов, снижение
эффективности системы антиоксидантной защиты тканей, развитию
геморрагического синдрома.
♦ Обесцвеченный кал вследствие уменьшения или отсутствия жёл- чи в кишечнике.
Источник